5 домашних химических экспериментов. Химические опыты в домашних условиях для детей
Как пробудить интерес ребенка к научным знаниям — например, к химии? Стоит испробовать практический подход. Теория суха и легко забывается, а знания, подтвержденные удачно проведенным экспериментом, надолго осядут в сознании.
В результате серии экспериментов «Клеящие вещества» родители вместе с ребенком могут создать клеящий карандаш, попутно многое узнав о химических свойствах знакомых нам веществ. Никаких эффектных взрывов и искр, зато опыты научно обоснованы и легко проводятся в домашних условиях.
Эксперимент 1
Нам понадобится: вода, сахар, сода, соль, кукурузный крахмал, бумага.
Эксперимент поможет разобраться, как делается клей и что именно придает ему такое свойство, как липкость. Для начала попросите детей вспомнить и подумать, какие продукты, имеющиеся на вашей кухне, оставляют после себя липкие следы? На каждой кухне найдутся порошкообразные ингредиенты, что произойдет, если разбавить их с водой? Что бы узнать, нужно попробовать! Смешайте с водой сахар, соду, соль, кукурузный крахмал или аналогичные образцы. Удастся ли этими растворами склеить пару листов бумаги?
Удастся ли этими растворами склеить пару листов бумаги?
Эксперимент 2
В предыдущем эксперименте мы узнали, что при смешивании крахмала с водой образуется липкое вещество. Крахмал является природным сырьем. Как же узнать где есть крахмал, а где его нет?
Итак, в этом эксперименте используется два образца: положительный образец, содержащий кукурузный крахмал, и отрицательный образец, содержащий вещество, которое по виду похоже на кукурузный крахмал (например, сахарная пудра).
Перед началом эксперимента предложите детям подумать о том, какие продукты могут содержать крахмал. Они могут проверить свои предположения, используя метод определения, приведенный ниже.
Необходимые материалы:
- Раствор Люголя (раствор йода/раствор иодида калия).
- Одноразовые пипетки.
- Лабораторные пробирки или небольшие стеклянные емкости, в которых можно смешивать исследуемые вещества с раствором Люголя (вполне подойдет и кухонная утварь — например, рюмки).

- Кукурузный крахмал и сахарная пудра для контрольных образцов.
- Пищевые продукты, содержащие крахмал, например, картофель, заранее замоченные зерна пшеницы, кукурузная мука.
- Пищевые продукты, не содержащие крахмал, например, огурцы.
Используйте лопатку, чтобы поместить небольшое количество кукурузного крахмала в лабораторную пробирку. Добавьте 2 мл (1/2 чайной ложки) воды, осторожно встряхните пробирку. Затем добавьте в пробирку 4 капли раствора Люголя. Что произошло? В образцах, содержащих крахмал, раствор примет характерную синюю окраску.
Присутствует ли крахмал в вашем клеевом карандаше? Теперь вы можете сами проверить это.
Пришло время узнать в каких же продуктах содержится крахмал. Предложите своему ребенку заполнить следующую таблицу:
| Продукт | Инструкции | Крахмал | Нет крахмала |
| Картофель | Капните 4 капли раствора Люголя на половинку картофелины. |
||
| Огурец | Отрежьте несколько ломтиков огурца и капните на них несколько капель раствора Люголя. | ||
| Рис | Раздробите несколько зерен риса и поместите их в пробирку. Добавьтее несколько капель раствора Люголя. | ||
| Кукуруза | Раздробите несколько зерен кукурузы в ступке, поместите их в пробирку. Добавьтее несколько капель раствора Люголя. |
Эксперимент 3
Итак, мы узнали, что в картошке крахмал есть, а в огурцах — нет. Как же его теперь оттуда, из картошки, достать?
Полезным отправным пунктом может стать наблюдение того факта, что вода становится мутной, если в нее несколько часов положить продукты, содержащие крахмал. Это становится особенно заметным, если в воде замочить зерна риса. Мутность означает, что из продукта в воду перешло некое вещество.
Необходимые материалы:
- 3-6 картофелин (в зависимости от размера).
- 150 г кукурузной муки.
- Старые кухонные полотенца.
- 4 пластмассовых чашки среднего размера.
- 1-2 терки.
- 2 фарфоровых тарелки или термостойких кристаллизатора.
- Мерный стакан.
- Вода.
- Выберите один из продуктов (3-6 картофелин или 150 г кукурузной муки), измельчите его на терке, если это необходимо (в пластмассовой или металлической чашке).
- Добавьте 300 мл воды к измельченным продуктам в чашке и перемешайте стеклянной палочкой.
- Накройте вторую чашку кухонным полотенцем, вылейте смесь на полотенце и отожмите воду (жидкость). Соберите жидкость в чашку.
- Поместите оставшуюся смесь в первую чашку, повторите этапы 2 и 3, но используйте только 200 мл воды.
 Подождите пять минут и осторожно слейте воду. Оставьте белый осадок на дне чашки.
Подождите пять минут и осторожно слейте воду. Оставьте белый осадок на дне чашки. - Переложите осадок на тарелку и поместите ее в духовой шкаф при температуре 180°C на 20 минут. После этапа сушки на тарелке останется плотное вещество беловатого цвета: крахмал.
Эксперимент 4
В первом эксперименте, мы узнали, что при соединении крахмала с водой образуется клейкое вещество. Но это вещество еще непригодно для использования в качестве клея. Для этого с полученной смесью необходимо проделать еще несколько действий.
Во-первых, из этого эксперимента дети узнают, что при нагревании с водой крахмал превращается в желеобразную клейкую пасту. Во-вторых, они узнают, что для хорошего клея нужна правильная консистенция.
Спросите своего ребенка, как он думает: что нужно сделать с крахмалом, чтобы он стал более клейким?
Необходимые материалы:
- Крахмал, полученный в эксперименте ранее, или готовый кукурузный крахмал (свой, конечно, использовать гораздо интереснее).

- 1-2 огнеупорных стеклянных стакана или кастрюли.
- Плита или духовой шкаф.
- 1-2 стеклянных палочки или ложки для перемешивания.
- Термометр.
Для приготовления крахмальной пасты необходимо смешать 1 г (1/4 чайной ложки) крахмала с 5 мл (чайной ложкой) воды и нагревать при температуре около 80°C, пока смесь не начнет прилипать к палочке или к ложке. Крахмал набухает при нагревании. Набухание вызвано тем, что растворитель (вода) поглощается под воздействием силы капиллярности, а затем испаряется. Примерами из повседневной жизни могут служить приготовление пудинга или густых соусов.
Итак, у нас есть крахмальная паста. Можем ли мы начать склеивать ей различные поверхности? Почти!
Эксперимент 5
Держитесь, мы почти закончили!
Что же отделяет нас от настоящего клея? Попробуем сделать следующее:
- Поместите крахмальную пасту на кончике лопатки в лабораторную пробирку, добавьте 5 мл воды, закройте пробирку пробкой.

- Встряхивайте пробирку в течение примерно 30 секунд.
- Повторите процесс с веществом, из которого изготовлен клеевой карандаш.
Скажите, в чем была разница? Не было у вас ощущения, что материал, из которого изготовлен клей-карандаш, вспенился совсем как мыло?
Что же, попробуем приготовить крахмальную пасту, но на этот раз — с добавлением мыльной стружки.
Необходимые материалы:
- Крахмал, полученный в процессе эксперимента, или готовый кукурузный крахмал.
- Кусок мыла, по возможности без отдушки.
- 1-2 огнеупорных стеклянных стакана или кастрюли.
- Плита или духовой шкаф.
- 1-2 стеклянных палочки или ложки для перемешивания.
- Термометр.
Измельчите примерно четверть куска мыла, используя терку для картофеля.
В стакане объемом 150 мл тщательно растворите 1 г (1/4 чайной ложки) натертого мыла в 14 мл (чайная ложка) воды; в результате должна получиться мыльная пена.
Добавьте 4 г (чайную ложку) крахмала к мыльному раствору и тщательно перемешайте с помощью стеклянной палочки.
Нагрейте смесь на плитке до температуры 80°C, периодически перемешивая стеклянной палочкой.
Что у вас получилось? Можно ли как-то поменять свойства получившийся массы?
Повторите этапы со второго по четвертый, используя 2 г (1/2 чайной ложки), 3 г (3/4 чайной ложки) и 4 г (чайную ложку) мыла.
Варьируя количество мыла, можно приготовить клей абсолютно любой консистенции.
Итак, мы только что приготовили настоящий клей-карандаш. Остальные опыты маленькие экспериментаторы смогут провести на бесплатных занятиях «Мира Исследователей «Хенкель». Узнать о месте и времени проведения занятий, а также записать своего ребенка на них можно на сайте программы.
МДОУ «Детский сад № 82» город Ярославль
Опыты дома
Думаете, химию и физику дети начинают изучать только в школе? А вот и нет! Детям в возрасте 3-7 лет можно предложить занимательные игры – основы химии и физики. Многие из представленных опытов можно проводить в домашних условиях. Это касается как простых химических опытов, так и занимательных физических экспериментов. Проводя опыты дома, не забудьте о мерах предосторожности, особенно если за опытами будут наблюдать дети. Все эксперименты носят обучающий характер, несмотря на использовании в них, зачастую, простых обыденных предметов, например, опыты с атмосферным давлением, холодной и горячей водой, газировкой и т.д. Ведь они не перестают быть научными и при этом интересными, занимательными и прикольными.
Многие из представленных опытов можно проводить в домашних условиях. Это касается как простых химических опытов, так и занимательных физических экспериментов. Проводя опыты дома, не забудьте о мерах предосторожности, особенно если за опытами будут наблюдать дети. Все эксперименты носят обучающий характер, несмотря на использовании в них, зачастую, простых обыденных предметов, например, опыты с атмосферным давлением, холодной и горячей водой, газировкой и т.д. Ведь они не перестают быть научными и при этом интересными, занимательными и прикольными.
Простая наука на YouTube
Занимательная химия для детей
Набор юного химика:
- Небольшие прозрачные стаканчики, можно одноразовые
- Стакан для воды
- Ложка или деревянная палочка для размешивания
- Вода
- Пшено или любая другая крупа
- Песок
- Мука
- Соль
- Сахар
Позвольте ребенку самостоятельно наливать в стаканчики с ингредиентами воду и размешивать содержимое ложкой или палочкой.
Что же получается в итоге?
Что будет, если смешать воду с солью?
Соль растворится! И вода станет соленой. Если ребенок попробует воду на вкус, убедится в этом лично.
С сахаром тоже выходит интересная штука…
А как насчет песка или пшена? Оказывается, с пшеном ничего не произойдет, оно так и останется на дне стаканчика.
С песком получится замечательная грязь!
А с мукой — тесто! Добавляем больше муки — получаем более густое тесто. Из муки с водой, сахаром и солью можно даже испечь блинчики.
При этом все манипуляции ребенок выполняет самостоятельно, а мама лишь комментирует его действия и помогает, если что-то не выходит.
Такие занятия химией для детей 2-3 лет способствуют развитию мелкой моторики при размешивании ингредиентов и дают малышу полезную информацию об окружающем мире.
Ребенок узнает, что:
- есть вещества, которые растворяются в воде, а есть твёрдые нерастворимые предметы;
- вода в сочетании с другими веществами меняет цвет и прозрачность;
- вода с солью приобретает солёный вкус, а с сахаром — сладкий (обязательно проговаривайте: «это сладкое», «это соленое»).

Не менее увлекательным занятием для юных химиков станет и уборка стола после опытов. Вручите маленькому экспериментатору чистую влажную тряпочку и пускай трет стол сколько душе угодно. Не забудьте после этого похвалить ребенка за уборку!
Опыты дома «Сидим дома» совет от старшего воспитателя Светланы Владимировны
«Опыты с водой!» дома совет от старшего воспитателя Светланы Владимировны
Опыты с водой «Дождь в баночке» практическое занятие от воспитателя группы Звездочка» Инны Александровны
Опыты дома советы от воспитателя группы «Колокольчик» Виктории Викторовны
Кулинарные опыты с детьми
Чем занять ребенка, когда идет уже третья неделя самоизоляции, а все мультики пересмотрены и игры переиграны?
Давайте испечем вместе с детьми печенье!!! Смотри сюда
Нам потребуется :
230 гр муки (+ на подсыпку стола)
100 гр сахара
полпакетика разрыхлителя теста (6 гр)
2 яйца
1 пачка творога (180 гр)
100 гр сливочного масла
Выпекаем в духовке при 180 гр около 10 минут.
Похвастайтесь результатами совместного творчества – пришлите свое фото с готовым печеньем или сфотографируйте процесс его приготовления и пришлите на электронную почту детского сада. Мы обязательно разместим все фотографии на сайте детского сада!!!
50 химических проектов, которые удивят детей!
Химические проекты кажутся волшебством , не так ли? Если вы вспомните некоторые из ваших любимых научных проектов, те, которые вы любите пробовать со своими детьми, или те, которые поражали ВАС в детстве, скорее всего, большинство из них связано с химией.
Теперь я знаю, что у многих из нас химия ассоциируется с лабораторными халатами, химическими стаканами и специальными ингредиентами, но реальность такова, что есть так много химических проектов, которые вы можете сделать, используя очень простые, легкодоступные ингредиенты, которые часто можно найти в вашей собственной кладовой. А поскольку в этих типах простых химических проектов используются относительно безопасные ингредиенты, они идеально подходят для детей младшего возраста, т. е. дети дошкольного и младшего школьного возраста! На самом деле, я думаю, что для маленьких детей очень важно иметь положительную ассоциацию с химией с раннего возраста, которая воспитывает любовь к этой отрасли науки.
е. дети дошкольного и младшего школьного возраста! На самом деле, я думаю, что для маленьких детей очень важно иметь положительную ассоциацию с химией с раннего возраста, которая воспитывает любовь к этой отрасли науки.
Когда большинство детей, наконец, знакомятся с химией в школе, это происходит на уровне старшей школы, где предмет быстро становится сложным; мы надеемся, что предоставление детям возможности повеселиться в раннем возрасте, смешивая смеси и наблюдая за химическими реакциями, поможет сохранить их интерес в более сложные дни учебы.
Этот пост представляет собой ОГРОМНУЮ подборку проектов по химии, которые отлично подойдут для научной ярмарки, демонстраций в классе или домашних занятий с детьми. Прежде чем мы начнем, давайте немного поговорим о том, что такое химия, а для родителей я также включил раздел, посвященный тому, как выполнять химические проекты дома. Если вы классный руководитель, вы можете пропустить этот раздел и перейти прямо к проектам здесь.
Что такое химия?
Химия — это отрасль науки, которая изучает материю (все, что имеет массу и занимает пространство) и ее свойства, а также то, как различные вещества (особенно молекулы и их атомы) взаимодействуют, комбинируются и изменяются, образуя новые вещества.
Вот несколько важных определений, которые следует знать при работе над проектами по химии:
- Элемент Вещество, которое нельзя разделить ни на какие другие вещества. Известно 120 элементов.
- Атом Мельчайшая частица элемента
- Молекула Группы атомов, соединенных химической связью.
- Ион Атом или молекула, обладающая электрическим зарядом
Хотя большинство людей думают о химии исключительно с точки зрения химических реакций, химия также охватывает изучение состояний вещества, а также плотности веществ.
Пять разделов химии:
- Аналитическая химия
- Физическая химия
- Органическая химия
- Неорганическая химия
- Биохимия
Узнайте больше о том, что охватывает каждое направление, здесь.
Как делать химические проекты дома
Многие химические проекты можно выполнять дома, используя простые материалы, и это отличный способ привить детям любовь к науке! Я искренне верю, что вау-фактор в проекте привлекает и вдохновляет детей учиться дальше. Если вы хотите попробовать химические проекты дома, вот несколько советов и мер предосторожности:
Безопасность превыше всего Несмотря на то, что в большинстве проектов в этом списке используются безопасные, легкодоступные материалы, их следует использовать с соблюдением мер предосторожности и под присмотром взрослых. Почему? Иногда возникающая химическая реакция может вызвать раздражение кожи или глаз, может быть вредным при проглатывании, или просто становится липкой или грязной, и взрослые должны быть под рукой, чтобы контролировать использование . Также имейте в виду, что в этом списке есть несколько проектов, в которых используются материалы, небезопасные для детей. Эти проекты предназначены только для демонстрации и имеют пометку 9.0004 соответственно.
Эти проекты предназначены только для демонстрации и имеют пометку 9.0004 соответственно.
- Используйте предметы домашнего обихода для химии. Кислоты и щелочи), но есть много других замечательных ингредиентов для химии, которые можно найти на вашей кухне, включая сахар, соль, дрожжи, лимоны, средство для мытья посуды, молоко, Kool-Aid, капусту, желатин и пищевые красители, и это лишь некоторые из них… прежде чем заказывать какие-либо материалы в Интернете, попробуйте несколько проектов с предметами первой необходимости.
- Стоит вложений Если вы обнаружите, что у вас есть несколько молодых химиков, вы можете инвестировать в несколько расходных материалов, чтобы сделать химические проекты безопасными и более «лабораторными». Вот несколько расходных материалов, в которые стоит инвестировать:
- Безопасность Очки
- Перчатки
- Пипетки
- Большие пластиковые стаканы
- Подготовка к беспорядку не будет беспокоиться о том, чтобы испачкаться.
 Внутренний дворик, место для завтрака или гараж — отличный выбор.
Внутренний дворик, место для завтрака или гараж — отличный выбор. - Просторная рабочая зона Обязательно подготовьте большой стол, чтобы у всех было достаточно места для работы и/или просмотра проектов, не сталкиваясь друг с другом.
- Доступ к воде Уборка всегда проще, когда вода наготове! Выберите место рядом со шлангом или магазинной раковиной.
- Смыть из шланга В зависимости от проекта я предлагаю провести очень грязные химические реакции снаружи. Таким образом, разливы можно будет легко смыть из шланга.
- Малярный брезент и подносы Если вы не можете выйти на улицу, большой пластиковый малярный брезент — отличный способ удержать разливы и грязь. Я также настоятельно рекомендую делать проекты на подносах или противнях. Приподнятые края помогают удерживать шипучие напитки, их легко выгружать и мыть.
- Станция сброса Держите поблизости ведро, которое будет служить станцией сброса жидких реакций.
 Принесите его вокруг стола и сбросьте на каждой станции.
Принесите его вокруг стола и сбросьте на каждой станции. - Подумайте об утилизации Уксус убивает траву! Кусочки слизи забивают канализацию! Обязательно подумайте, куда вы можете безопасно сливать жидкости.
Следующие проекты по химии для детей отсортированы по темам: химические реакции, кислоты и основания, реакции углерода, хроматография, коллоиды и растворы, полимеры и кристаллы.
Обратите внимание, что многие из этих проектов можно отнести к двум или более категориям в этом посте, поскольку они демонстрируют различные научные и химические процессы. Я классифицировал их только один раз в этом списке.
Химические проекты с химическими реакциями Что такое химическая реакция?
Химические реакции происходят, когда химические связи в веществе либо разрушаются, либо создаются. Другими словами, связи в молекуле разрываются во время химической реакции, и атомы перестраиваются, создавая новые молекулы.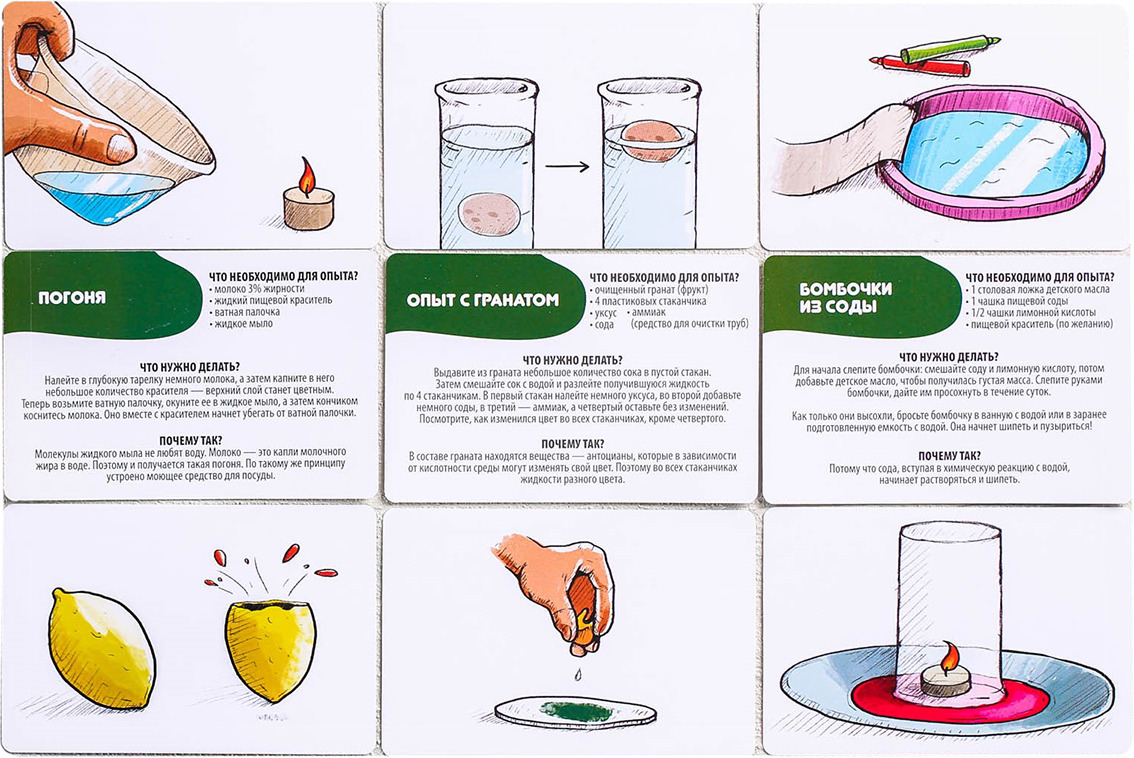 Интересно, что количество исходных атомов в ходе реакции не меняется, они просто перестраиваются.
Интересно, что количество исходных атомов в ходе реакции не меняется, они просто перестраиваются.
Простым способом объяснить детям химические реакции является использование следующей аналогии: атомы подобны буквам, молекулы подобны словам. Химия — это как разбирать слова и переставлять буквы, чтобы образовать новое слово.
Подробнее о химических реакциях читайте здесь.
Проекты химических реакций: 1. Молочная краска 2. Цитрусовая батарея 3. Зубная паста для слонов 9 0004 4. Лавовые лампы плотности Для заполнения лавовой лампы плотности пластиковая бутылка со следующими жидкостями: прозрачный кукурузный сироп, вода с несколькими каплями пищевого красителя и слой растительного масла. Не забудьте оставить место в верхней части бутылки. Подождите, пока жидкость не осядет, затем добавьте таблетку спирта повышенной крепости. Наблюдайте, как щелочная сельтерская вода и вода реагируют и пузырятся сквозь слой масла. Чтобы увидеть это в пошаговом видео, посмотрите это видео (Pssst, это один из наших студентов!!!)
Чтобы увидеть это в пошаговом видео, посмотрите это видео (Pssst, это один из наших студентов!!!)
Налейте воду в три прозрачных пластиковых стаканчика, затем добавьте в каждый синий, красный и желтый пищевой краситель. Приготовьте также дополнительную чашку с неокрашенной водой. Дайте ребенку пустой лоток для кубиков льда и пипетки, и пусть он создаст разные цвета, смешивая в разных соотношениях два разных основных цвета в каждом отделении для кубиков льда. Вторичные цвета — это новые цвета, созданные из двух основных цветов. Это простое изображение того, как работают химические реакции.
7. Химические часы 8. Выдуйте шарики с дрожжами и сахаром 9. Блестящие монетки- Собрать грязные испорченные копейки.
- Наливайте различные кислые жидкости в неглубокие контейнеры.
 Попробуйте уксус, сальсу, сок лимона и лайма.
Попробуйте уксус, сальсу, сок лимона и лайма. - Добавьте чайную ложку соли в каждый контейнер и перемешайте.
- Положите горсть монет в каждый контейнер и оставьте на 5 минут.
- Выньте их из раствора и промойте в мыльной воде. Дайте высохнуть на отдельных бумажных полотенцах.
- Сравните результаты! Какие из них самые блестящие? Какие скучные? Кто-нибудь стал зеленым?
Кислоты вызывают коррозию и имеют кислый вкус. Жидкости, такие как уксус, лимонный сок и томатный сок, являются кислотами. Пенни сделаны из меди, которая со временем тускнеет (темнеет) под воздействием кислорода. Помещение медных монет в кислоту очистит их от оксида меди, и они снова станут блестящими.
Узнайте о кислотах и щелочах
Большинство жидкостей представляют собой либо кислоту, либо основание. Жидкости с большим количеством ионов водорода в них считаются кислотами. Жидкости с большим количеством гидроксид-ионов являются основаниями. Ученые используют шкалу, называемую шкалой pH, для измерения кислотности или щелочности жидкости. Чем больше ионов водорода в жидкости, тем она более кислая и занимает низкое место по шкале рН. Чем больше ионов гидроксида в жидкости, тем она более щелочная и занимает высокое место по шкале pH. Вы можете увидеть, как это выглядит здесь.
Ученые используют шкалу, называемую шкалой pH, для измерения кислотности или щелочности жидкости. Чем больше ионов водорода в жидкости, тем она более кислая и занимает низкое место по шкале рН. Чем больше ионов гидроксида в жидкости, тем она более щелочная и занимает высокое место по шкале pH. Вы можете увидеть, как это выглядит здесь.
При смешивании кислот и оснований происходят химические реакции, и раствор нейтрализуется.
Кислота и щелочи Проекты: 1. Пищевая сода и уксус Volcano 2. Lemon Volcano 9 0172 3. Научный эксперимент с красочным капустным соком и Кислотно-основной эксперимент с капустой 4. Танцующий рис 5. Зеленые яйца и ветчина 6. Шипучий напиток с лимонной кислотой 7. Пищевая сода и разрыхлитель Научный эксперимент 8. Взрывной мешок s 9. Радужные резиновые яйца 10. Сюрприз Яйца 11. Braw Wizard’s Wizard
Взрывной мешок s 9. Радужные резиновые яйца 10. Сюрприз Яйца 11. Braw Wizard’s Wizard Химические проекты с огнем (углеродные реакции)
Углерод является наиболее важным элементом для жизни. Химические вещества, содержащие углерод, называются органическими соединениями. Углерод имеет две основные формы: первая — твердая форма алмазов и графита, а вторая — нечистая форма, содержащаяся в древесном угле, угле и саже.
ПРЕДУПРЕЖДЕНИЕ О БЕЗОПАСНОСТИ: Наблюдать за углеродными реакциями всегда увлекательно, однако присутствие огня означает, что эти эксперименты должны постоянно находиться под присмотром взрослых!
Проекты Carbon Reactions: 1. Smoking Fingers 2. Fire Snake 3. Silver Яйцо 4.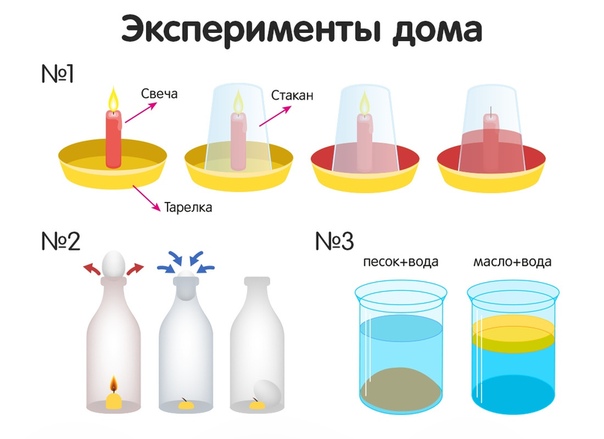 Невидимые чернила
Невидимые чернила Хроматография
Хроматография – это процесс разделения смесей. Мы обычно думаем об этом с точки зрения цвета, отсюда и приставка -цветность, однако в химии это означает просто метод разделения смесей, позволяя им медленно перемещаться относительно друг друга. Это относится как к жидкостям, так и к газам. Это прекрасное подробное объяснение хроматографии.
Хроматография Проекты: 1. Хроматография В этом проекте вы разделите черный цвет на другие цвета. Сложите кофейный фильтр пополам. Сложите пополам еще два раза, пока не получите треугольную форму. Покрасьте кончик кофейного фильтра смываемым черным маркером. Нанесите хороший слой чернил на фильтр. Добавьте небольшое количество воды в пластиковый стаканчик. Поместите черный наконечник кофейного фильтра в чашку. Подождите и наблюдайте. Вернитесь к фильтру через час или два и посмотрите, что произойдет с чернилами.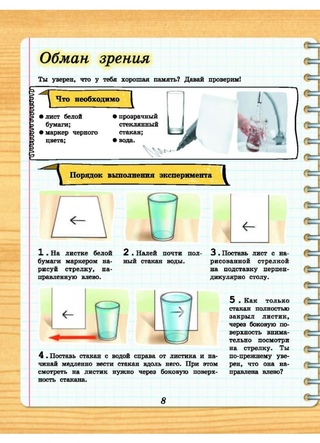 Поскольку кофейный фильтр поглощает воду за счет капиллярного действия, черные чернила проходят через фильтр и разделяются водой на другие цвета. Вы должны увидеть синий, зеленый и даже красный цвет, когда вода отделяет чернила.
Поскольку кофейный фильтр поглощает воду за счет капиллярного действия, черные чернила проходят через фильтр и разделяются водой на другие цвета. Вы должны увидеть синий, зеленый и даже красный цвет, когда вода отделяет чернила.
2.
Цветы для хроматографии3.
Хроматография Art 4. Пакеты для хроматографии9 0017 Коллоиды и растворы/Растворимость
Коллоиды и растворы представляют собой два типа гомогенных смесей.
- Коллоиды представляют собой смеси, в которых мелкие частицы вещества взвешены в другом веществе, но не связаны химически. Они стабильны, хотя и не отделяются. Примерами коллоидов являются желатин, масло, майонез, туман и дым.
- Растворы – это смеси, в которых частицы одного вещества полностью растворены в другом веществе. Растворенное вещество — это растворяемое вещество, а растворитель — это растворяющееся вещество.
 Примером решения является соленая вода.
Примером решения является соленая вода.
Если вам нужна более подробная информация о растворах и коллоидах, перейдите сюда.
Коллоидные проекты: 1. Примеры коллоидов 2. Oobleck 3. Приготовление сливочного масла 4. Желатин с полосками9 0003 Solutions/Solubility Projects:
5. Ледяные скульптуры 6. Мороженое в сумкаРаспечатка научных фактов здесь
7. Skittles Science 8. Волшебные водяные цветы9 0003 9. Распространение Искусство
10. Растворимость краски 11. Bleeding BlossomsПолимеры
Полимер – это вещество, состоящее из длинной цепи молекул. Полимеры обычно представляют собой гибкие материалы, такие как пластик или жевательная резинка.
Полимеры обычно представляют собой гибкие материалы, такие как пластик или жевательная резинка.
Классический полимерный слайм, который ЛЮБЯТ делать дети! Клей уже является полимером, но в сочетании с тетраборатом натрия (бурой) белковые молекулы клея и ионы бората сшиваются, затрудняя движение молекул и образуя липкое, липкое вещество, известное нам как слизь.
Другими полимерами, с которыми вы, вероятно, знакомы, являются пластиковые пакеты, воздушные шары, быстрорастворимый снег и даже порошкообразная субстанция, содержащаяся в подгузниках, которая расширяется при намокании.
Полимерные проекты: 1. Лучший базовый слайм Бонус: узнайте, что стоит за слизью, которую можно распечатать здесь
4.
Эксперимент с волшебным пластиковым пакетом 5. Мгновенные террариумы 6. Как сделать бумагу 7. Протыкание воздушного шара
Мгновенные террариумы 6. Как сделать бумагу 7. Протыкание воздушного шара 90 003 8. Сухое стирание Рисунок и Сухое стирание рисунков
9. Из вторсырья Пластиковые цветыКристаллы
Кристаллы представляют собой материал, образованный повторяющимися молекулами. Существует четыре типа химических связей в кристаллах и, следовательно, четыре категории кристаллов. Это: ковалентные, молекулярные, металлические и ионные кристаллы. Вы можете вырастить кристаллы, смешав перенасыщенный раствор (обычно с солью и водой) и дав ему отстояться с течением времени, чтобы образовались кристаллы. Ознакомьтесь с различными типами легко выращиваемых кристаллов ниже и перейдите сюда, чтобы узнать больше о науке о кристаллах.
Кристаллы Проекты: 1. Классические кристаллы буры 2. Ночной Хрустальный сад 3. Яичные жеоды 4. Хрустальные ветроуловители 5. Хрустальные пейзажи 6. Карамельные жеоды 7. Кристаллы соли Заключение и многое другое
Классические кристаллы буры 2. Ночной Хрустальный сад 3. Яичные жеоды 4. Хрустальные ветроуловители 5. Хрустальные пейзажи 6. Карамельные жеоды 7. Кристаллы соли Заключение и многое другое Хорошо, ребята , вам не кажется, что у вас есть хорошие идеи для изучения химии с детьми? Многие из них станут отличными проектами научной ярмарки. Обязательно начните с них как с темы, затем начните задавать вопросы, формировать гипотезы и проводить эксперименты.
Должен признаться, что во взрослом возрасте я действительно влюбился в химические проекты. Работая с детьми в лагере, после школы и со своими детьми дома, у меня была возможность попробовать забавные химические проекты, и я обнаружил, что люблю наблюдать за химическими реакциями И реакциями на лицах детей и прохожих во время демонстрации или проекта!
Если у вас есть дети, которые влюбляются в эту область науки, пожалуйста, ознакомьтесь с невероятной серией книг Elements , Molecules и Reactions Теодора Грея (см. серию в нашем списке научных идей Amazon здесь). Книги потрясающие, информативные, простые для понимания и, подождите… забавные!
серию в нашем списке научных идей Amazon здесь). Книги потрясающие, информативные, простые для понимания и, подождите… забавные!
Еще одним ценным ресурсом для детей, которые любят химию, является коробка подписки Mel Science’s Chemistry. Они отправляют вам бесплатно стартовый набор со всеми необходимыми материалами, а затем каждый месяц вы получаете новый химический эксперимент, доставленный к вашей двери! Это отличный продукт, потому что многие специальные химические ингредиенты трудно найти, а эти наборы упрощают получение необходимых материалов! Посмотрите здесь:
Вы увлечены воспитанием творческих детей?
Присоединяйтесь к более чем 22 179 родителям и педагогам, которые хотят общаться с детьми и развивать их творческий процесс с помощью волшебных, простых проектов, которые вы можете делать ВМЕСТЕ.
Подпишитесь на нашу рассылку, чтобы получать идеи для проектов, а также предложения для некоторых наших творческих продуктов.
Если вы хотите ознакомиться с нашей политикой конфиденциальности перед подпиской, перейдите сюда.
8 простых химических экспериментов, которые ваши дети могут провести дома
Химия — увлекательный предмет. И есть ли лучший способ учиться, чем с помощью научных экспериментов?
Вот 8 практических научных экспериментов для детей во время школьных каникул. Эти эксперименты отлично подходят для детей старшего возраста или с помощью мамы или папы. Их можно приготовить дома из продуктов, которые уже есть под рукой.
Безопасность: Это занятие требует использования ножа, ядовитых химикатов и горячей воды. Попросите взрослого помочь вам. Всегда следуйте рекомендациям по безопасности продуктов, которые вы используете.
Всё, что мы едим и пьём, содержит кислоты, а то, что мы используем для уборки, является основным. Это связано с тем, что основные вещества имеют неприятный вкус, но чистящее средство обычно должно быть основным, чтобы удалить грязь и жир.
Кислотные или щелочные вещества вызывают жжение в глазах, поэтому детский шампунь сделан нейтральным.
Кислоты представляют собой очень распространенную группу химических соединений, многие из которых встречаются в природе. Кислоты могут быть сильными и слабыми.
Лимонная кислота, которая естественным образом содержится в лимонах, является слабой кислотой. Соляная кислота (используется для пайки) и серная кислота (аккумуляторная кислота) являются очень сильными кислотами.
Основания (часто называемые щелочами) представляют собой еще одну группу химических соединений, химические свойства которых отличаются от свойств кислот. Когда основания и кислоты добавляются вместе, они нейтрализуют свойства друг друга.
Мы описываем, являются ли вещества кислотными, щелочными или нейтральными, используя шкалу, называемую шкалой рН. Шкала рН колеблется от нуля до 14. Вещество с рН:
Кислоты и основания можно обнаружить с помощью группы химических соединений, называемых кислотно-щелочными индикаторами. Одним из первых известных природных индикаторов был тип лишайника, называемый лакмусом. (Лишайники — это наросты, похожие на растения, которые часто встречаются на камнях и коре деревьев.) Лакмус становится красным в присутствии кислоты или синим в присутствии основания.
Одним из первых известных природных индикаторов был тип лишайника, называемый лакмусом. (Лишайники — это наросты, похожие на растения, которые часто встречаются на камнях и коре деревьев.) Лакмус становится красным в присутствии кислоты или синим в присутствии основания.
Большинство индикаторов, используемых сегодня для обнаружения кислот и щелочей, созданы руками человека. Однако многие растительные пигменты, такие как краснокочанная капуста, которую вы использовали, содержат химические вещества, действующие как кислотно-щелочные индикаторы.
Узнайте больше о газах, создав фонтанчик для безалкогольных напитков из леденцов/конфет. Какой приятный способ узнать больше о химии!
Вам потребуется
- Рулет с леденцами/конфетами (хорошо подойдут мятные леденцы/конфеты)
- Бутылка безалкогольного напитка 2 л
- Бумага или трубочка для леденцов/конфет
- Открытая площадка
Что делать
Занимайтесь этим на открытом воздухе.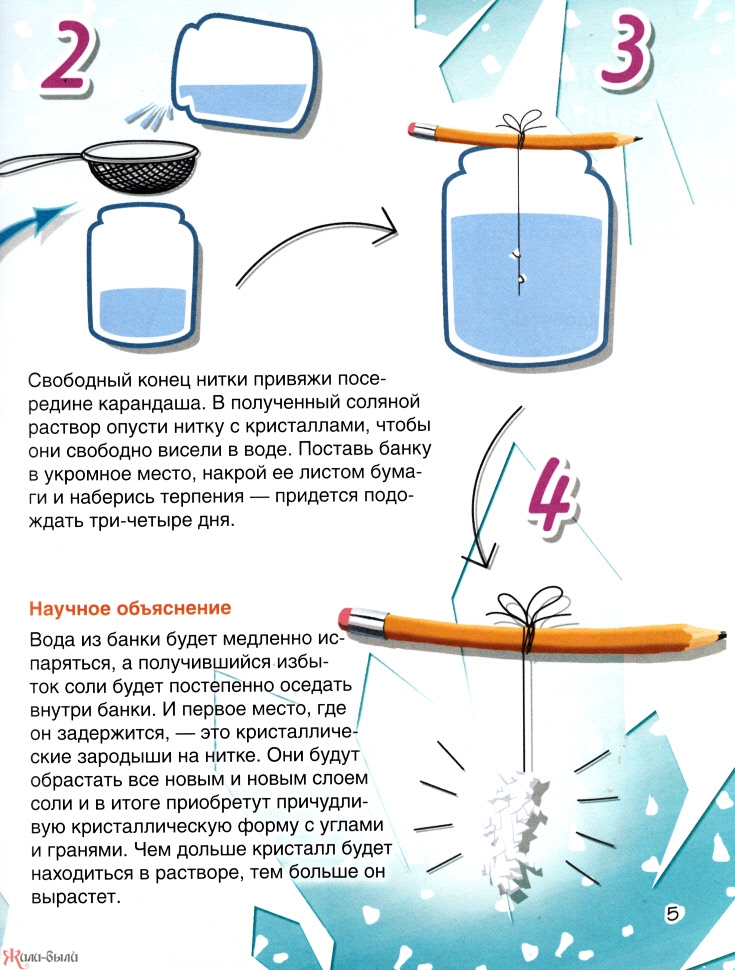
- Откройте бутылку с безалкогольным напитком и поставьте бутылку на землю, чтобы она не опрокинулась.
- Сверните бумагу в цилиндр, ширина которого достаточна для того, чтобы леденцы проходили сквозь него.
- Поместите палец на дно рулона и попросите друга положить леденцы в бумажную трубку.
- Держите трубку с леденцами прямо над бутылкой и уберите палец, чтобы все леденцы упали прямо внутрь. Вам нужно бросить все леденцы в бутылку одновременно.
- Как только вы это сделаете, отойдите от бутылки как можно быстрее.
Советы
- Диетический безалкогольный напиток работает так же хорошо и менее липкий, так как не содержит сахара.
- Апельсиновый безалкогольный напиток не всегда работает. Так же как и Соло, так как он легко шипит.
- Поэкспериментируйте с различными видами леденцов – в этом упражнении использовались мятные конфеты Kool Mints. Попробуйте Mentos или другие леденцы, покрытые сахаром.

- Поэкспериментируйте с безалкогольным напитком комнатной температуры или из холодильника.
Что происходит?
Безалкогольный напиток пенится, потому что в бутылку под давлением нагнетается углекислый газ.
Пока вы не откроете бутылку, газ в основном остается растворенным в жидкости и не может расширяться, образуя пузырьки, которые газ будет делать, когда газ не находится под давлением.
Если встряхнуть бутылку, а затем открыть ее, газ вырвется со свистом, забрав с собой немного безалкогольного напитка. Добавление чего-либо в безалкогольный напиток приводит к образованию и выходу большего количества пузырьков.
Попробуйте размешать безалкогольный напиток ложкой, он станет менее шипучим.
Леденцы очень быстро обеспечивают большую площадь поверхности, что означает, что пузырьки газа образуются очень быстро в огромных количествах.
Вам нужны негладкие поверхности, чтобы газ мог образовываться.
И песок, и сахар имеют одинаковый эффект при добавлении в безалкогольный напиток.
Когда вы смотрите на стакан с безалкогольным напитком, обычно вы видите лишь несколько потоков пузырьков, исходящих из определенных точек на стекле, где поверхность неровная.
Иногда вы видите поток пузырей, исходящий из середины, и если вы внимательно присмотритесь, то часто сможете увидеть пылинку с пузырьками, вырывающуюся из ее конца.
Место, где начинают формироваться пузырьки, называется центром зарождения.
Когда леденец растворяется, он образует сотни точек зародышеобразования, которые представляют собой крошечные ямки на поверхности леденца, где могут образовываться дополнительные пузырьки углекислого газа.
Когда весь этот газ высвобождается, он подбрасывает все содержимое бутылки вверх, создавая невероятный взрыв безалкогольного напитка.
Сделайте бомбочки для ванны своими рукамиСледуйте этим инструкциям, чтобы сделать бомбочки для ванны своими руками и узнать о науке, развлекаясь в ванне!
Вам понадобится
пищевой краситель/краситель
лепестки цветов или блестки для тела
масло сладкого миндаля
ароматическое масло, такое как масло лаванды
10 столовых ложек двууглекислой соды
3 столовые ложки лимонной кислоты
2 большие миски
1 большой противень для маффинов
1 небольшая стеклянная банка
резиновые перчатки
ложка
Что делать
Смажьте стенки и дно большой формы для маффинов небольшим количеством миндального масла.

Поместите лимонную кислоту и соду в большую миску. Хорошо перемешайте ингредиенты, чтобы получилась базовая смесь.
Зачерпните примерно полстакана этой смеси и положите ее в другую миску. Из этого количества получится одна-две бомбочки для ванны (в зависимости от размера отверстий в лотке для маффинов). Вы также можете использовать старые пластиковые контейнеры или что-нибудь, что будет держать форму.
Добавьте лепестки цветов или глиттер для тела в базовую смесь.
В небольшой стеклянной баночке смешайте 6 капель ароматического масла, 5 чайных ложек масла сладкого миндаля и примерно 10 капель пищевого красителя.
Постепенно влейте масляную смесь в полстакана базовой смеси. Надев резиновые перчатки, быстро перемешайте все вместе. Смесь готова, когда она держится в руках и не слишком крошится.
Выложите смесь ложкой в форму для маффинов. Плотно прижмите его.

Вы можете использовать оставшуюся смесь с другими видами ароматических масел или пищевых красителей, чтобы сделать больше бомбочек для ванн.
Оставьте бомбы в лотке на несколько дней.
Аккуратно переверните бомбочки для ванны, чтобы извлечь их из формочек.
Набери ванну, запрыгни и сбрось бомбу. Смотри, это шипит!
Что происходит?
Когда бомбочка для ванны растворяется в воде, происходит химическая реакция между лимонной кислотой и бикарбонатом натрия. Результат называется цитратом натрия. В ходе реакции выделяется углекислый газ. Это вызывает «шипение», которое вы видите, как в газированной воде.
В ходе этой реакции высвобождается масло сладкого миндаля. Он образует тонкий слой на вашей коже, который может помочь увлажнить ее. Лавандовое масло для аромата.
Подождите, в библиотеке Reading Eggs есть еще книги о научных экспериментах!
Узнайте, что нового здесь Как приготовить щербетСледуйте этим инструкциям, чтобы создать кислотно-щелочную реакцию во рту!
Вам понадобится
- сахарная пудра
- лимонная кислота
- сода двууглекислая
- ароматизированные/ароматизированные желейные кристаллы
- чайная ложка
- десертная ложка
- маленькая чаша для смешивания
- маленькая сумка с защелкой.

Что делать
Для приготовления щербета вам потребуется:
- добавить 1 чайную ложку без горки кристаллов лимонной кислоты в чашу
- добавьте в миску 1 чайную ложку без горки соды
- Теперь добавьте 3 десертные ложки сахарной пудры с горкой
- добавить не менее 2 десертных ложек без горки кристаллов желе (или больше по вкусу)
- положите небольшое количество, около половины чайной ложки на язык
- после дегустации вам может понадобиться изменить ингредиенты. Если он слишком горький, добавьте больше сахара, если шипения недостаточно, вам может понадобиться добавить либо соду, либо лимонную кислоту. Убедитесь, что вы добавляете только в небольших количествах, помните, что вы всегда можете добавить больше, но очень трудно удалить часть.
Что происходит?
Вы только что вызвали кислотно-щелочную реакцию во рту. Когда вы смешиваете кислоту (в данном случае лимонную кислоту) и щелочь (бикарбонат соды) со слюной, они смешиваются вместе, образуя газ в виде множества крошечных пузырьков.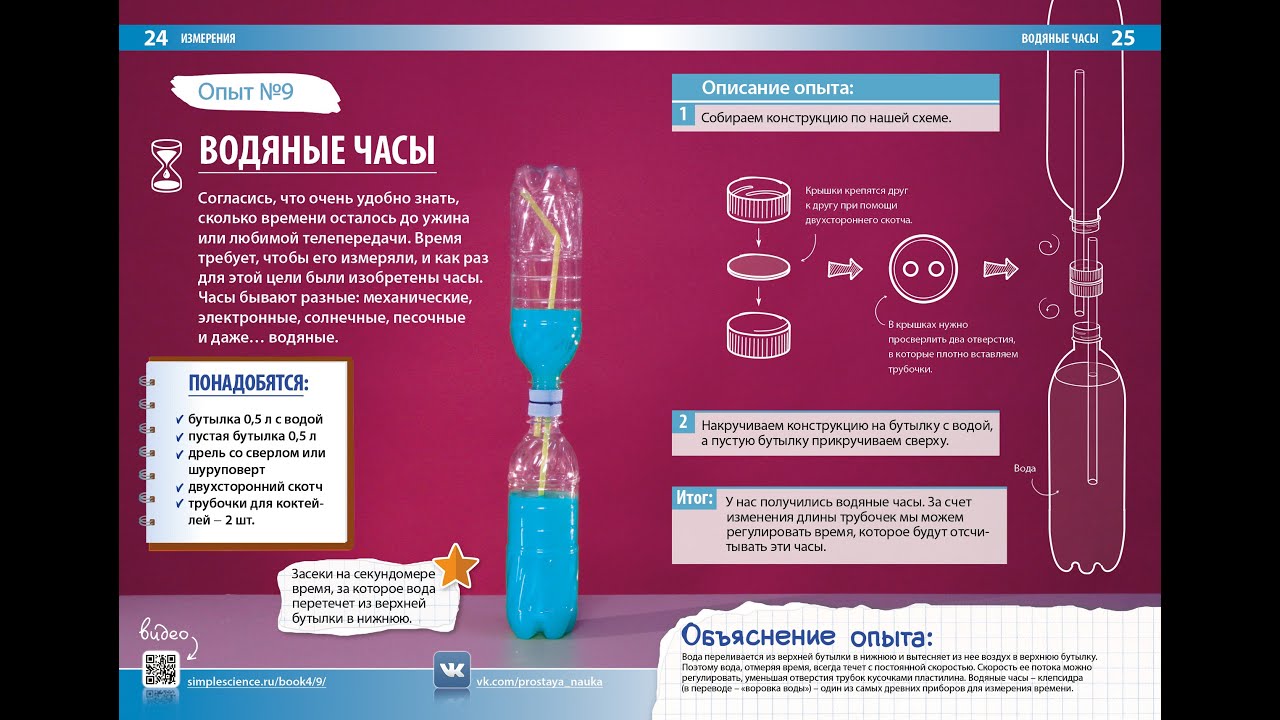
Это называется кислотной реакцией, и именно она придает щербету шипение. На самом деле вы чувствуете ощущение пузырьков углекислого газа на языке. Это те же пузырьки, что и в газированных напитках.
Сахарная пудра необходима для придания сладости, так как лимонная кислота и бикарбонатная сода довольно кислые. Лимонная кислота — одна из кислот, содержащихся в лимонах, апельсинах и лаймах. Именно поэтому их называют «лимонными фруктами».
Другая кислота в лимонах и других цитрусовых фруктах называется аскорбиновой кислотой. Это широко известно как витамин С. Кристаллы желе просто добавляют аромат.
Резиновое яйцоСледуйте этим инструкциям, чтобы заставить яйцо подпрыгивать, изучая химические реакции.
Вам понадобится
- сваренное вкрутую яйцо со скорлупой
- стакан уксуса.
Что делать
Чтобы яйца подпрыгивали, вам потребуется:
- Поместите яйцо в уксус – вы должны увидеть, как на яйце начнут образовываться пузыри.

- Оставьте яйцо в покое хотя бы на сутки. Вы должны увидеть замечательную форму пены.
- Выньте яйцо из уксуса и промойте его водой. Скорлупа сотрется.
- Ткните яйцо пальцем и осторожно сожмите его.
Что происходит
Уксус или разбавленная уксусная кислота «съедает» карбонат кальция в яичной скорлупе, оставляя только внутреннюю оболочку или кожу яйца. Поскольку карбонат кальция делает скорлупу твердой, яйцо, пропитанное уксусом, кажется мягким и эластичным.
При соединении карбоната кальция (яичной скорлупы) и уксусной кислоты (уксуса) происходит химическая реакция с выделением углекислого газа. Вот почему вы видите пузыри.
Химическая реакция продолжается около суток, пока не будет израсходован весь карбонат кальция в яйце. Карбонат кальция содержится в яичной скорлупе, морских раковинах, известняке и многих других материалах.
Давайте подробнее рассмотрим химическую реакцию. Формула карбоната кальция CaCO 909. 07 3 , а уксусная кислота — CH 2 COOH.
07 3 , а уксусная кислота — CH 2 COOH.
Итак, реакция такова: CaCO 3 + CH 2 COOH -> Ca 2+ (в виде соли) + H 2 O + 2CO 2 .
Ионы кальция (Ca 2+ ) свободно плавают в растворе. Ионы — это атомы или молекулы, которые имеют электрический заряд из-за потери или приобретения электронов.
Области применения
Известняк представляет собой осадочную породу, состоящую в основном из карбоната кальция. Обычно он белый, но может быть окрашен примесями; оксид железа делает его коричневым, желтым или красным, а углерод делает его синим, черным или серым. Текстура варьируется от грубой до тонкой.
Большинство известняков образовались в течение тысячелетий из скелетов морских беспозвоночных. Важными разновидностями известняка являются мергель, мел, оолит, травертин, доломит и мрамор.
Кислотный дождь вызывает реакцию, подобную той, что описана в этом упражнении. Один из видов кислотных дождей может происходить из-за загрязнения воздуха, вызванного сжиганием топлива, содержащего атомы серы, которые при сгорании выделяют сернистый газ.
Один из видов кислотных дождей может происходить из-за загрязнения воздуха, вызванного сжиганием топлива, содержащего атомы серы, которые при сгорании выделяют сернистый газ.
Когда диоксид серы смешивается с дождем, он превращается в слабую серную кислоту. Когда кислотный дождь падает на известняк, он медленно распадается, как это сделала яичная скорлупа. Люди используют известняк в зданиях и статуях.
Вот почему со временем кислотные дожди повреждают здания и статуи.
Если вы соберете небольшие образцы камней и бросите их в уксус, вы можете увидеть появление пузырьков, как на яйце. Наличие пузырьков указывает на то, что в образце может присутствовать карбонат кальция.
Карбонат кальция реагирует с кислотами с образованием углекислого газа, который мы наблюдаем в виде пузырьков. Это называется «кислотный тест». «Кислотный тест» — один из многих тестов, которые геологи используют для определения подлинности образца горной породы.
Создание кристалловВам понадобится
- Сахар
- Соль
- Бикарбонат натрия
- Теплая вода
- 3 пипетки
- 3 ложки
- 3 пластиковых контейнера или миски
- Мерный стакан
- 3 маленьких пластиковых стаканчика
- Маркер
Что делать
- Пометьте контейнеры словами «сахар», «соль» и «биуглеводы».

- Налейте полстакана теплой воды в емкость с надписью «сахар».
- Добавьте в воду ложку сахара и размешайте до растворения. Продолжайте добавлять сахар, пока он не перестанет растворяться.
- Повторите шаги 2 и 3, но с солью вместо сахара.
- Снова повторите шаги 2 и 3, но на этот раз с содовой вместо сахара или соли.
- Пометьте маленькие пластиковые стаканчики «сахар», «соль» и «биуглеводы».
- Используйте отдельные пипетки, чтобы добавить несколько капель раствора из каждого контейнера в соответствующий стаканчик. №
- Поставьте чашки в теплое солнечное место и оставьте до испарения жидкости. Что ты видишь?
Вы можете попробовать это упражнение и с другими кристаллическими веществами.
Что происходит?
Когда твердое вещество (или «растворенное») растворяется в воде до тех пор, пока растворение не прекращается, раствор считается «насыщенным». Количество вещества, растворяющегося в воде, увеличивается с температурой. Когда раствор снова остывает до комнатной температуры, растворенного вещества в воде становится больше, чем обычно — раствор становится «перенасыщенным».
Когда раствор снова остывает до комнатной температуры, растворенного вещества в воде становится больше, чем обычно — раствор становится «перенасыщенным».
При испарении воды растворенное вещество выпадает из раствора в виде кристаллов. Это пример кристаллизации. Вы заметите, что каждый осадок образует немного разные кристаллы: они могут быть разных размеров и формы. Размер и форма кристалла зависят от ряда факторов, включая химическую формулу, температуру и давление. Как правило, кристаллы, которые образуются медленно, имеют тенденцию быть больше, чем кристаллы, которые образуются быстро.
СлизьВам понадобится
- Кукурузная мука
- Пищевой краситель
- Маленькая чаша для смешивания
- Пластиковая ложка
- Вода
Что делать
- Насыпьте немного кукурузной муки в чашу миксера.
- Добавьте небольшое количество воды, пока кукурузная мука не превратится в очень густую пасту.

- Чтобы придать слизи желаемый цвет, тщательно размешайте в смеси около пяти капель пищевого красителя.
- ОЧЕНЬ медленно перемешайте слайм. Это не должно быть сложно сделать.
- ОЧЕНЬ быстро перемешайте слайм. Это должно быть почти невозможно.
- Теперь бейте свою слизь ДЕЙСТВИТЕЛЬНО сильно и быстро. Должно быть ощущение, что ты бьешь по твердому телу.
Смесь кукурузной муки и воды можно хранить в холодильнике в течение нескольких дней. Если кукурузная мука осядет, вам нужно перемешать ее, чтобы она снова хорошо работала.
Что происходит
Все, что течет, называется жидкостью. Это означает, что и газы, и жидкости являются жидкостями.
Говорят, что жидкости, такие как вода, которые легко текут, имеют низкую вязкость, тогда как жидкости, такие как холодный мед, которые не так легко текут, имеют высокую вязкость.
Слизь из кукурузной муки — это особый тип жидкости, который не подчиняется обычным правилам поведения жидкости. Когда на шлам оказывается давление, его вязкость увеличивается, а шлам из кукурузной муки становится гуще.
Когда на шлам оказывается давление, его вязкость увеличивается, а шлам из кукурузной муки становится гуще.
В какой-то момент слизь теряет свою текучесть и ведет себя как твердое тело. Слизь из кукурузной муки является примером жидкости, загущающей при сдвиге.
Противоположное происходит в жидкостях, разжижающих сдвиг; они становятся более жидкими, когда вы их перемешиваете или встряхиваете. Например, когда зубная паста находится на зубной щетке, она довольно густая, поэтому вы можете перевернуть зубную щетку вверх дном, и зубная паста не упадет.
Но если он был таким густым, когда вы пытались выдавить его из тюбика, вы никак не могли с этим справиться. К счастью, зубная паста становится более жидкой, когда вы выдавливаете ее из тюбика. К другим разбавляющим сдвиг жидкостям относятся:
- кровь
- краска
- чернила для шариковой ручки
- лак для ногтей
Несмотря на то, что существует множество жидкостей, разжижающихся и загущающихся при сдвиге, никто не имеет четкого представления о том, почему они ведут себя так, а не иначе.
Взаимодействия между атомами в жидкостях настолько сложны, что даже самые мощные в мире суперкомпьютеры не могут смоделировать происходящее. Это может стать настоящей проблемой для тех, кто проектирует машины, использующие разбавляющие сдвиг жидкости, потому что трудно быть уверенным, что они будут работать.
Сопливая слизьВам понадобится
- 1 столовая ложка неароматизированного желатина (из супермаркетов)
- ½ стакана золотого сиропа или глюкозы
- 1 столовая ложка соли
- Горячая вода
- Пищевой краситель
- Жаропрочная чаша
Что делать
- Поместите желатин и соль в миску.
- Добавьте ½ стакана сиропа.
- Добавьте ½ стакана горячей воды. Настало время добавить пищевой краситель, если вы хотите, чтобы сопли были отвратительно-зелеными или желтыми.
- Все смешать и охладить в холодильнике 30 минут.
- Проведите вилкой по сопливой смеси, чтобы посмотреть, как она выглядит.
 Ваша слизь будет становиться все гуще и гуще по мере остывания, если она слишком густая, вы можете добавить больше воды.
Ваша слизь будет становиться все гуще и гуще по мере остывания, если она слишком густая, вы можете добавить больше воды.
Что происходит?
Вы только что сделали реалистичную модель собственных соплей. Слизь состоит из воды, эпителиальных (поверхностных) клеток, мертвых лейкоцитов (лейкоцитов), муцинов (крупных белков) и неорганических солей. Ваша домашняя слизь содержит воду, соль и белки (желатин — это животный белок, обычно изготавливаемый из говяжьей или свиной кожи и копыт), почти как настоящая слизь.
Желатин растворяется в горячей воде, образуя густой раствор, но не растворяется (не растворяется) в холодной воде. При охлаждении частицы набухают, превращаясь в желеобразную слизь.
Применение
Слизь играет важную роль в организме. В вашем носу он задерживает пыль и все остальное нежелательное в воздухе. Слизь высыхает вокруг частиц, которые затвердевают, и это означает, что она может быстро выйти из вашего тела, когда вы сморкаетесь.


 Подождите пять минут и осторожно слейте воду. Оставьте белый осадок на дне чашки.
Подождите пять минут и осторожно слейте воду. Оставьте белый осадок на дне чашки.


 Внутренний дворик, место для завтрака или гараж — отличный выбор.
Внутренний дворик, место для завтрака или гараж — отличный выбор. Принесите его вокруг стола и сбросьте на каждой станции.
Принесите его вокруг стола и сбросьте на каждой станции. Попробуйте уксус, сальсу, сок лимона и лайма.
Попробуйте уксус, сальсу, сок лимона и лайма. Примером решения является соленая вода.
Примером решения является соленая вода.






 Ваша слизь будет становиться все гуще и гуще по мере остывания, если она слишком густая, вы можете добавить больше воды.
Ваша слизь будет становиться все гуще и гуще по мере остывания, если она слишком густая, вы можете добавить больше воды.