Функции вегетативной нервной системы
Вегетативная нервная система выполняет ряд функций:
Управляет деятельностью внутренних органов, кровеносных и лимфатических сосудов, осуществляя иннервацию гладкомышечных клеток и железистого эпителия.
Регулирует обмен веществ, приспосабливая его уровень к снижению или повышению функции органа. Тем самым осуществляет адаптационно-трофическую функцию, в основе которой лежит транспорт аксоплазмы — процесс непрерывного движения различных веществ от тела нейрона по отросткам в ткани. Одни из них включаются в обмен веществ, другие активируют метаболизм, улучшая трофику ткани.
Координирует работу всех внутренних органов, поддерживая постоянство внутренней среды организма.
Центры вегетативной нервной системы разделяют на сегментарные и надсегментарные (высшие вегетативные центры).
Сегментарные центры
Мезенцефалический отдел в среднем мозге — добавочное ядро (Якубовича), nucleus accessorius, и непарное срединное ядро глазодвигательного нерва (III пара).

Бульбарный отдел в продолговатом мозге и мосту — верхнее слюноотделительное ядро, nucleus salivatorius superior, промежуточно-лицевого нерва (VII пара), нижнее слюноотделительное ядро, nucleus salivatorius inferior, языкоглоточного нерва (IX пара) и дорсальное ядроблуждающего нерва (X пара), nucleus dorsalis n. vagi.
Оба этих отдела объединяются под названием краниального и относятся к парасимпатическим центрам.
Тораколюмбальный отдел — промежуточно-боковые ядра, nuclei intermediolaterales, 16-ти сегментов спинного мозга (С 8, Th1-12, L1-3). Они являются симпатическими центрами.
Сакральный отдел — промежуточно-боковые ядра, nuclei intermediolaterales, 3-х крестцовых сегментов спинного мозга (S2-4) и относятся к парасимпатическим центрам.

Высшие вегетативные центры (надсегментарные) объединяют и регулируют деятельность симпатического и парасимпатического отделов, к ним относятся:
Ретикулярная формация, ядра которой формируют центры жизненно-важных функций (дыхательный и сосудодвигательный центры, центры сердечной деятельности, регуляции обмена веществ и т.д.). Проекция дыхательного центра соответствует средней трети продолговатого мозга, сосудодвигательного центра — нижней части ромбовидной ямки. Нарушение функции ретикулярной формации проявляется вегетативно-сосудистыми расстройствами (кардио-васкулярные, вазомоторные). Кроме того страдают интегративные функции, которые необходимы для формирования целесообразного адаптивного поведения.
Мозжечок, принимая участие в регуляции двигательных актов, одновременно обеспечивает эти анимальные функции адаптационно-трофическими влияниями, которые через соответствующие центры приводят к расширению сосудов интенсивно работающих мышц, повышению уровня трофических процессов в последних.
 Установлено участие мозжечка в регуляции
таких вегетативных функций, как зрачковый
рефлекс, трофика кожи (скорость заживления
ран), сокращение мышц, поднимающих
волосы.
Установлено участие мозжечка в регуляции
таких вегетативных функций, как зрачковый
рефлекс, трофика кожи (скорость заживления
ран), сокращение мышц, поднимающих
волосы.
- Гипоталамус — главный подкорковый центр интеграции вегетативных функций, имеет существенное значение в поддержании оптимального уровня обмена веществ (белкового, углеводного, жирового, минерального, водного) и терморегуляции. За счет связей с таламусом он получает разностороннюю информацию о состоянии органов и систем организма, а вместе с гипофизом образует функциональный комплекс — гипоталамо-гипофизарную систему. Гипоталамус в ней выполняет роль своеобразного реле, включающего гипофизарную гормональную цепь в регуляцию различных висцеральных и соматических функций.
Особое место занимает лимбическая система обеспечивающая интеграцию вегетативных, соматических и эмоциональных реакций.
Полосатое тело имеет ближайшее отношение к безусловнорефлекторной регуляции вегетативных функций.

Высшим центром регуляции вегетативных и соматических функций, а также их координации является кора полушарий большого мозга. Непрерывный поток импульсов от органов чувств, сомы и внутренних органов по афферентным путям поступает в кору головного мозга и через эфферентную часть вегетативной нервной системы, главным образом через гипоталамус, кора оказывает соответствующее влияние на функцию внутренних органов, обеспечивая адаптацию организма к меняющимся условиям окружающей и внутренней среды. Примером кортиковисцеральной связи может служить изменение вегетативных реакций под влиянием словесных сигналов (через вторую сигнальную систему).
Таким
образом, вегетативная нервная система,
так же как и вся нервная система, построена
по принципу иерархии, подчиненности.
Схему организации вегетативной иннервации
иллюстрирует рис.
Рис. 1 Принцип организации вегетативной нервной системы.
Строение вегетативной нервной системы
Вегетативная нервная система выступает, наряду с соматической, подразделением большой и сложной нервной системы организма. С ее помощью идет постоянная регуляция работы органов, желез и сосудов (как кровеносных, так и лимфатических). Произвольно руководить вегетативной нервной системой невозможно — человек не может ни поднять температуру усилием воли, ни приказать желудку остановиться и не просить пищи.
По устройству и выполняемым задачам вегетативная нервная система разделена на две. Симпатическая, или же «система стресса», работает тогда, когда организм возбужден. Например, когда вы волнуетесь перед экзаменом или убегаете от злой овчарки. Правда, эта система тормозит работу органов пищеварения и мочеобразования.
Вторая, парасимпатическая, «система покоя», включается тогда, когда организм расслаблен и отдыхает.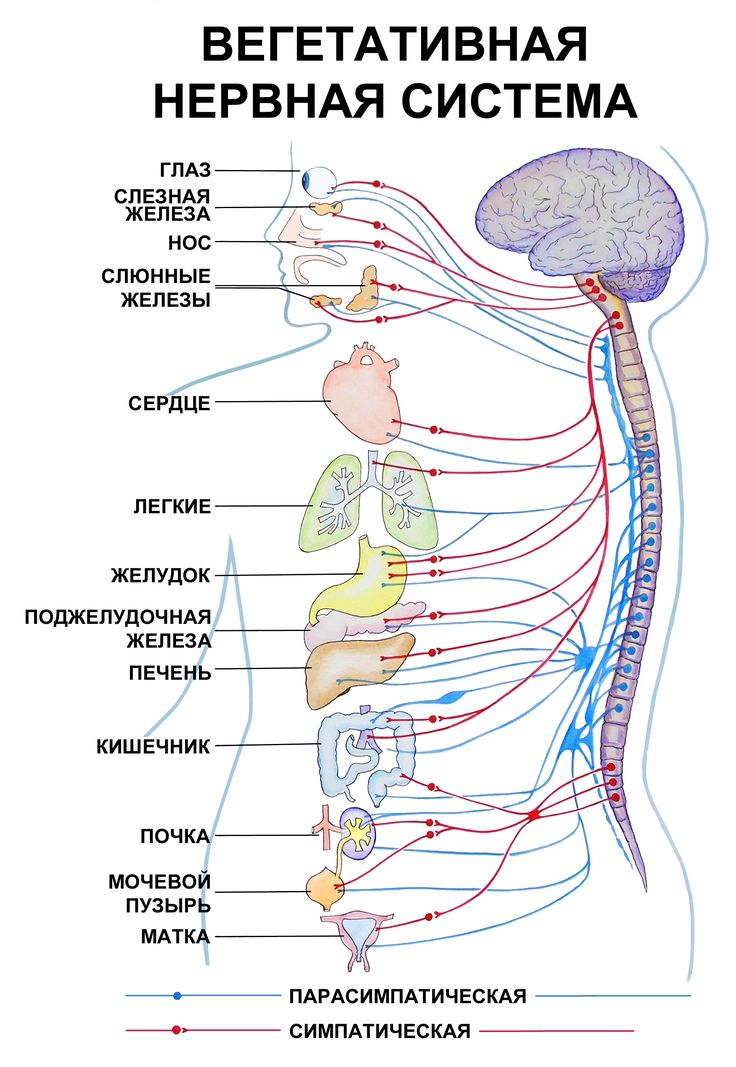 Но при этом она активирует пищеварение (замечали ли вы, что после чересчур плотного обеда наступает сонливость?) и мочеобразование, вот такие вот «перекрестья». Эти две системы действуют, словно качели из досочки: когда один край взлетает высоко, второй опускается на землю. И все-таки вместе они замечательно поддерживают внутренние настройки организма.
Но при этом она активирует пищеварение (замечали ли вы, что после чересчур плотного обеда наступает сонливость?) и мочеобразование, вот такие вот «перекрестья». Эти две системы действуют, словно качели из досочки: когда один край взлетает высоко, второй опускается на землю. И все-таки вместе они замечательно поддерживают внутренние настройки организма.
Высший центр вегетативной нервной системы — гипоталамус (часть промежуточного мозга). Кроме гипоталамуса в управлении участвует и продолговатый мозг.
Строение симпатической нервной системы. Симпатические ядра, их положение
1) Симпатические ядра представляют собой сгущения тел нейронов, лежащие в боковых рогах спинного мозга, причем только в грудном и поясничном его отделах.
2) От тел нейронов отходят длинные отростки-аксоны, формирующие нервные волокна.
3) Для симпатической системы характерны двигательные нейроны
Преганглионарные волокна и симпатические узлы. Постганглионарные волокна
1. Как симпатическая, так и парасимпатическая системы имеют характерное двухнейронное строение, при котором один нейрон лежит в центральной нервной системе, второй — на периферии, в узле-ганглии или непосредственно в органе.
2. Сгущения отростков первых нейронов формируют преганглионарные волокна, скопления отростков вторых нейронов — волокна постганглионарные.
3. Преганглионарные волокна отходят от симпатических ядер боковых рогов серого вещества спинного мозга (то есть они расположены «перед» ганглиями).
4. Аксоны преганглионарных нейронов, имеющие миелиновую оболочку, отходят от спинного мозга и переключаются на тела вторых нейронов — постганглионарных.
5. Скопления тел постганглионарных нейронов называются симпатическими узлами (ганглиями). Они находятся, во-первых, в симпатических стволах рядом с позвоночником, во-вторых, «разбросаны» в полостях тела и стенках органов. Симпатические ганглии также образуют сплетения: солнечное, легочное, сердечное, брыжеечный узел.
6. Постганглионарные волокна идут от симпатических узлов к органам, тканям, мускулам, миелиновой оболочки у них нет. Например, от чревного ганглия волокна «разбегаются» к печени, желудку, селезенке.
7. Важно, что преганглионарные волокна симпатической системы более короткие и толстые, а постганглионарные более длинные и тонкие. Из-за отсутствия миелиновой оболочки нервное возбуждение по ним передается медленнее.
Строение парасимпатической нервной системы
1) Парасимпатические ядра рассыпаны в стволе головного мозга и в спинном мозге, но только в крестцовом отделе (отсюда они уходят к кишечнику и органам выделения).
2) Парасимпатические ганглии (узлы) в большинстве своем мелкие, разбросанные, находятся довольно далеко от ядер, непосредственно рядом с органами или прямо в их толще. В связи с такой спецификой расположения узлов преганглионарные волокна длинные, а постганлионарные, наоборот, очень короткие — они уже, так скажем, работают на местах.
3) Основной, крупный смешанный нерв парасимпатической системы — блуждающий. Его можно представить в виде полноводной мощной реки, которая тянется на много километров, делает широкие изгибы, имеет множественные рукава, — потому что он подходит почти ко всем внутренним органам.
Сравнительная характеристика отделов периферической нервной системы
1.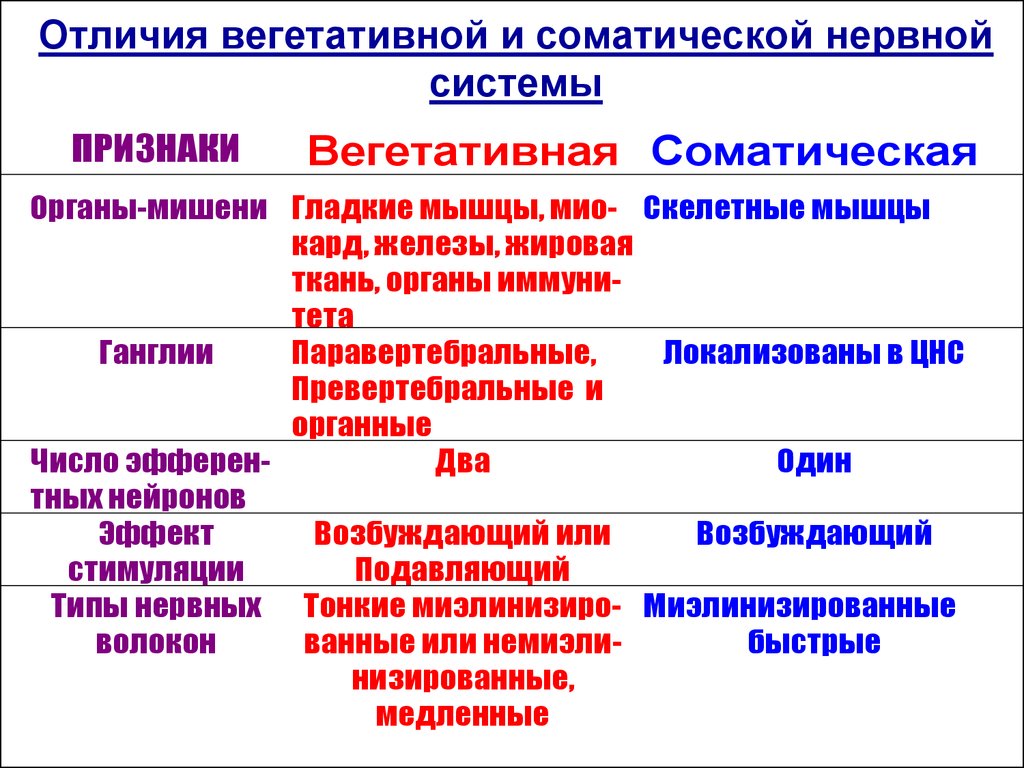 Соматическая нервная система:
Соматическая нервная система:
1) Нервы подходят к скелетной мускулатуре, сухожилиям и суставам.
2) Поддается сознательному контролю: мы можем по своему желанию идти быстрее или медленнее, взять чашку, принять определенную позу.
3) Управляющие центры в ЦНС расположены в коре больших полушарий.
4) Двигательные нервные узлы-ганглии скопились в передних рогах спинного мозга. Вторые, дополнительные, узлы вне ЦНС отсутствуют.
5) Отростки клеток покрыты миелиновой оболочкой.
2. Вегетативная нервная система:
1) Нервы «подключены» к гладкой мускулатуре органов, к железам, сердцу.
2) Сознанию неподконтрольна.
3) Управляющие центры в ЦНС представляют собой вегетативные ядра в спинном мозге и стволе головного мозга.
4) Двигательные нервные узлы (ганглии) скапливаются в боковых рогах спинного мозга. Вторые узлы вне ЦНС имеются, это симпатические узлы, лежащие неподалеку от спинного мозга или парасимпатические внутри иннервируемого органа.
Вторые узлы вне ЦНС имеются, это симпатические узлы, лежащие неподалеку от спинного мозга или парасимпатические внутри иннервируемого органа.
5) Миелиновая оболочка есть лишь до второго узла (до симпатического или парасимпатического), после второго узла отсутствует.
Выводы о строении отделов вегетативной нервной системы
Выше мы уже рассмотрели строение двух систем в составе вегетативной, а сейчас будет полезно повторить основные положения и наглядно сравнить их.
1. Симпатическая система:
1) Вегетативные ядра — центральная часть отдела, первые узлы — концентрируются в боковых рогах спинного мозга, а именно в его грудном и поясничном отделах.
2) Вторые узлы — вторые ганглии, вегетативные узлы расположены парами вдоль спинного мозга, по обе его стороны, или в нервных сплетениях.
3) Предузловое (предганглионарное) волокно короткое. Послеузловое (постганглионарное) намного длиннее.
Послеузловое (постганглионарное) намного длиннее.
4) Основные узлы: солнечное, легочное и сердечное сплетения, брыжеечный узел.
2. Парасимпатическая система:
1) Вегетативные ядра расположились в головном мозге (ствол) и спинном (крестец).
2) Вегетативные узлы находятся прямо в иннервируемом органе или же рядом с ним.
3) Предузловое (предганглионарное) волокно длинное. Послеузловое (постганглионарное) короткое.
4) Основной нерв — блуждающий.
Хочешь сдать экзамен на отлично? Жми сюда — видео уроки для подготовки к ОГЭ по биологии
Вегетативная нервная система | Кинезиолог
Краткое описание:
Ссыдка для цитирования: Сазонов В.Ф., Ендолов В.В., Муравьёва М.С. Вегетативная нервная система [Электронный ресурс] // Кинезиолог, 2009-2017: [сайт]. Дата обновления: 30.09.2019. URL: hhttp://kineziolog.su/content/vegetativnaya-nervnaya-sistema (дата обращения: __.__.2019).
_ __Вегетативная нервная система (ВНС) (синонимы: автономная, чревная, висцеральная, ганглионарная) — это часть нервной системы, которая регулирует уровень функциональной активности внутренних органов, кровеносных и лимфатических сосудов, секреторную активность желез внешней и внутренней секреции организма. Рассматриваются её особенности. Для биологов, медиков, психологов.
URL: hhttp://kineziolog.su/content/vegetativnaya-nervnaya-sistema (дата обращения: __.__.2019).
_ __Вегетативная нервная система (ВНС) (синонимы: автономная, чревная, висцеральная, ганглионарная) — это часть нервной системы, которая регулирует уровень функциональной активности внутренних органов, кровеносных и лимфатических сосудов, секреторную активность желез внешней и внутренней секреции организма. Рассматриваются её особенности. Для биологов, медиков, психологов.
Строение и функции вегетативной (автономной) нервной системы
Сазонов В.Ф., Ендолов В.В., Муравьёва М.С.
Кафедра биологии и методики её преподавания РГУ имени С.А. Есенина, г. Рязань
Вегетативная нервная система (ВНС) (синонимы: автономная, чревная, висцеральная, ганглионарная) — это часть нервной системы, которая регулирует уровень функциональной активности внутренних органов, кровеносных и лимфатических сосудов, секреторную активность желез внешней и внутренней секреции организма.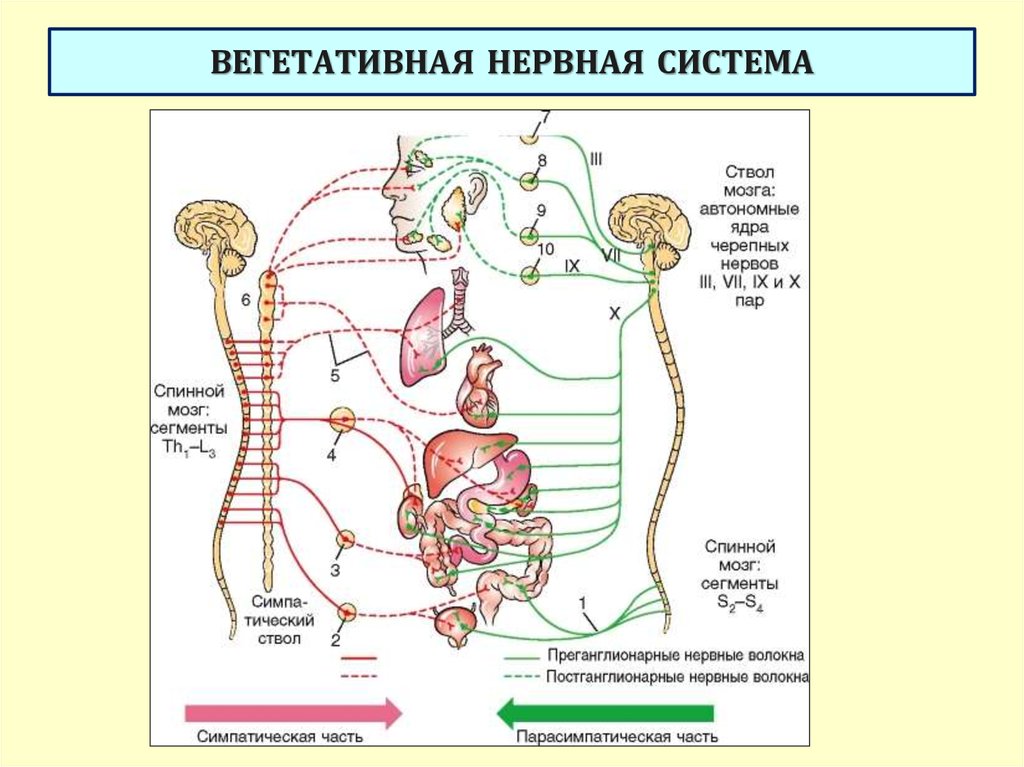
Вегетативная (автономная) нервная система выполняет адаптационно-трофические функции, активно участвуя в поддержании гомеостазиса (т.е. постоянства среды) в организме. Она приспосабливает функции внутренних органов и всего организма человека к конкретным изменениям окружающей среды, влияя и на физическую, и на психическую активность человека.
Её нервные волокна (обычно не все полностью покрытые миелином) иннервируют гладкую мускулатуру стенок внутренних органов, кровеносных сосудов и кожи, железы и сердечную мышцу. Оканчиваясь в скелетных мышцах и в коже, они регулируют уровень обмена веществ в них, обеспечивая их питание (трофику). Влияние ВНС распространяется также и на степень чувствительности рецепторов. Таким образом, вегетативная нервная система охватывает более обширные области иннервации, чем соматическая, т. к. соматическая нервная система иннервирует только кожу и скелетные мышцы, а ВНС — регулирует и все внутренние органы, и все ткани, осуществляя адаптационно-трофические функции в отношении всего организма, в том числе и кожи, и мышц.
По своему строению ВНС отличается от соматической. Волокна соматической нервной системы всегда выходят из ЦНС (спинного и головного мозга) и идут, не прерываясь, до иннервируемого органа. И они полностью покрыты миелиновой оболочной. Соматический нерв образован, таким образом, только отростками нейронов, тела которых лежат в ЦНС. Что касается нервов ВНС, то они всегда образованы двумя нейронами. Один — центральный, лежит в спинном или головном мозге, второй (эффекторный) — в вегетативном ганглии, и нерв состоит из двух отделов — преганглионарного, как правило, покрытого миелиновой оболочкой и оттого белого цвета, и постганглионарного — не покрытого миелиновой оболочкой и оттого серого цвета. Их вегетативные ганглии, (всегда вынесенные на периферию из ЦНС), располагаются в трёх местах. Первые (паравертебральные ганглии)— в симпатической нервной цепочке, расположенной по бокам позвоночника; вторая группа — более отдалённо от спинного мозга — превертебральные, и, наконец, третья группа — в стенках иннервируемых органов (интрамурально).
Некоторые авторы выделяют также экстрамуральные ганглии, лежащие не в стенке, а поблизости от иннервируемого органа. Чем дальше расположены ганглии от ЦНС, тем большая часть вегетативного нерва покрыта миелиновой оболочкой. И, следовательно, скорость передачи нервного импульса в этой части вегетативного нерва выше.
Следующее отличие состоит в том, что работа соматической нервной системы, как правило, может контролироваться сознанием, а ВНС — нет. Работой скелетных мышц мы, в основном, можем управлять, а сокращением гладкой мускулатуры (например, кишечника) никак не можем. В отличие от соматической в ней нет такой выреженной сегментарности в иннервации. Нервные волокна ВНС выходят из центральной нервной системы из трёх её отделов — головного мозга, грудопоясничных и крестцовых отделов спинного мозга.
Рефлекторные дуги ВНС по своей структуре отличаются от рефлекторных дуг соматических рефлексов. Дуга рефлекса соматической нервной системы всегда проходит через ЦНС. Что касается ВНС, то у неё рефлексы могут осуществляться как через длинные дуги (через ЦНС), так и через короткие — через вегетативные ганглии. Короткие рефлекторные дуги, проходящие через вегетативные ганглии, имеют большое значение, т.к. обеспечивают срочные адаптационные реакции иннервируемых органов, не требующих участия ЦНС.
Дуга рефлекса соматической нервной системы всегда проходит через ЦНС. Что касается ВНС, то у неё рефлексы могут осуществляться как через длинные дуги (через ЦНС), так и через короткие — через вегетативные ганглии. Короткие рефлекторные дуги, проходящие через вегетативные ганглии, имеют большое значение, т.к. обеспечивают срочные адаптационные реакции иннервируемых органов, не требующих участия ЦНС.
Метасимпатическая нервная система ВНС
Способность формировать местные рефлекторные дуги возможна благодаря тому, что в вегетативных ганглиях находятся как афферентные, так и эфферентные и ассоциативные нейроны, т.е. все типы нейронов, необходимые для формироования полноценной рефлекторной дуги. Такие рефлекторные дуги имеются, в частности, в стенке кишечника. Они образуют интрамуральные (от лат. intra — внутри, muralis — стенной) сплетения нейронов, позволяющие осуществлять местную регуляцию функций органа без участия структур ЦНС.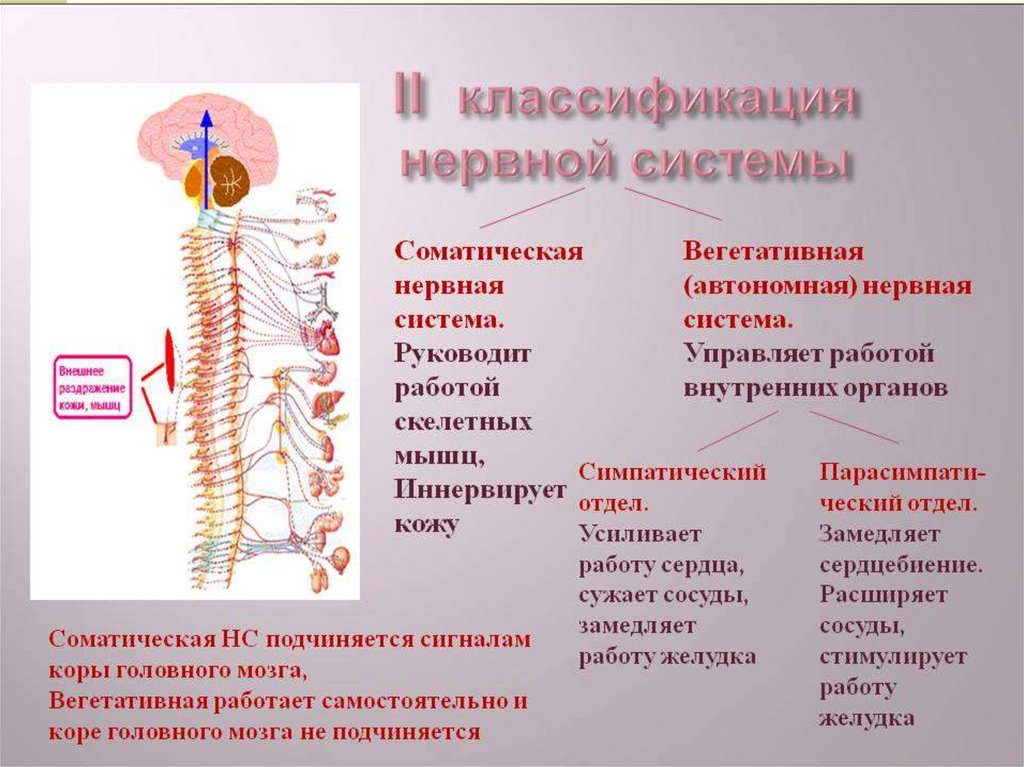 Некоторые из физиологов (Ноздрачев А.Д.) в связи с этим выделили их в третий отдел ВНС – метасимпатическую нервную систему. Её отделы располагаются в стенках внутренних органов. Эта особенность дает возможность наиболее точно изменять функцию органа (в частности, кишечника) в соответствии с конкретной ситуацией, которая складывается в зависимости от состава пищевой кашицы, степени её переваренности и других характеристик, которые могут быть оценены только на местном уровне регуляции.
Некоторые из физиологов (Ноздрачев А.Д.) в связи с этим выделили их в третий отдел ВНС – метасимпатическую нервную систему. Её отделы располагаются в стенках внутренних органов. Эта особенность дает возможность наиболее точно изменять функцию органа (в частности, кишечника) в соответствии с конкретной ситуацией, которая складывается в зависимости от состава пищевой кашицы, степени её переваренности и других характеристик, которые могут быть оценены только на местном уровне регуляции.
Энтеральная нервная система (ЭНС) — совокупность собственных нервных клеток (интрамуральные нейроны общим числом около 100 млн) пищеварительного тракта, а также отростков вегетативных нейронов, расположенных за пределами пищеварительной трубки (экстрамуральные нейроны). ЭНС находится в непосредственной близости от эффекторных систем ЖКТ (гладкомышечных, секреторных клеток и сосудов). Регуляция двигательной и секреторной активности ЖКТ — главная функция ЭНС. Стенка ЖКТ содержит мощные сети нервных сплетений. Структура, функция и нейрохимия ганглиев ЭНС отличается от других ганглиев вегетативной нервной системы, основная функция которых заключается в перераспределении сигналов от ЦНС. Ганглии ЭНС так взаимосвязаны между собой, что образуют нервную систему с механизмами для интеграции и обработки информации, подобно ЦНС, что дало основание называть энтеральную систему малым мозгом кишечника. Собственный нервный аппарат пищеварительного тракта представлен подслизистым и межмышечным сплетением.
Стенка ЖКТ содержит мощные сети нервных сплетений. Структура, функция и нейрохимия ганглиев ЭНС отличается от других ганглиев вегетативной нервной системы, основная функция которых заключается в перераспределении сигналов от ЦНС. Ганглии ЭНС так взаимосвязаны между собой, что образуют нервную систему с механизмами для интеграции и обработки информации, подобно ЦНС, что дало основание называть энтеральную систему малым мозгом кишечника. Собственный нервный аппарат пищеварительного тракта представлен подслизистым и межмышечным сплетением.
Межмышечное нервное сплетение (Ауэрбаха) расположено в мышечной оболочке пищеварительного тракта, состоит из сети нервных волокон, содержащей ганглии. Количество нейронов в ганглии варьирует от единиц до сотен. Мотонейроны ЭНС подразделяются на возбуждающие (мотонейроны) и тормозные. Медиаторами возбуждающих нейронов служат ацетилхолин и субстанция P, медиаторами тормозных нейронов — оксид азота и вазоинтестинальный пептид. Межмышечное нервное сплетение необходимо в первую очередь для управления моторикой пищеварительной трубки.
Межмышечное нервное сплетение необходимо в первую очередь для управления моторикой пищеварительной трубки.
Подслизистое нервное сплетение (Майсснера) расположено в подслизистой оболочке. Это сплетение управляет сокращениями ГМК мышечного слоя слизистой оболочки, а также секрецией желёз слизистой и подслизистой оболочек. Мотонейроны к секреторным клеткам слизистой оболочки выделяют ацетилхолин и VIP.
Иннервация ЖКТ
1. Парасимпатическая иннервация. Возбуждение парасимпатических нервов стимулирует ЭНС, увеличивая активность пищеварительного тракта. Парасимпатический двигательный путь состоит из двух нейронов.
2. Симпатическая иннервация. Возбуждение симпатической нервной системы тормозит активность пищеварительного тракта. Нейронная цепочка содержит два либо три нейрона.
Афференты. Чувствительные хемо- и механорецепторы в оболочках ЖКТ образуют терминальные разветвления собственных нейронов ЭНС (клетки Догеля 2-го типа), а также афферентные волокна первичных чувствительных нейронов спинномозговых узлов. . Источник: http://vmede.org/sait/?page=24&id=Fiziologija_orlov_2010&menu=Fiziologij…
. Источник: http://vmede.org/sait/?page=24&id=Fiziologija_orlov_2010&menu=Fiziologij…
Видеолекция: Вегетативная нервная система кишечника
ВНС делится на центральный и периферический отделы.
Нервные центры ВНС находятся в спинном мозге (в боковых рогах серого вещества), и в отделах головного мозга — продолговатом мозге, мосте, гипоталамусе, базальных ядрах. Лимбическая система также содержит регуляторные центры ВНС. Адаптационно-трофические функции выполняет также мозжечок, – он влияет на функциональный уровень работы пищеварительной системы, органов дыхания, работу сердечно-сосудистой системы, влияет на региональный кровоток.Наконец, в коре больших полушарий имеются представительства вегетативных функций.
В состав периферического отдела входят нервы, ветви и нервные волокна, выходящие из центров ВНС в головном и спинном мозге, нервные сплетения этих нервов и нервных волокон, вегетативные узлы (ганглии), симпатические стволы, состоящие из ганглиев с их соединительными ветвями и нервами, а так же ганглии парасимпатического отдела ВНС. Следует отметить, что количество выходящих (постганглионарных) волокон ВНС гораздо больше количества входящих в ганглий, т. е. преганглионарных. Выйдя из ганглиев, эти волокна способны образовывать многочисленные и сложные сплетения, играющие чрезвычайно важную роль в иннервации внутренних органов, в частности, органов брюшной полости. Это одна из особенностей строения ВНС.
Симпатическая и парасимпатическая ВНС
ВНС делится на два отдела – симпатический и парасимпатический. По строению они различаются расположением своих центральных и эффекторных нейронов, своими рефлекторными дугами.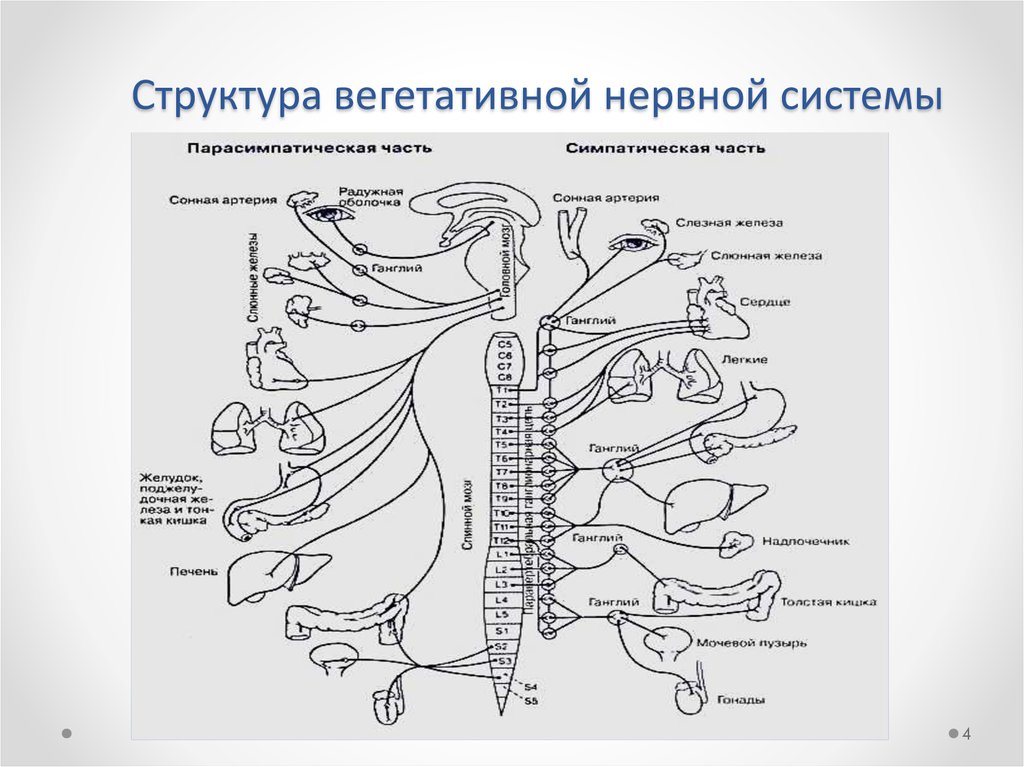 Они различаются так же и по своему влиянию на функции иннервируемых структур.
Они различаются так же и по своему влиянию на функции иннервируемых структур.
В чем состоят различия этих отделов? Центральные нейроны симпатической нервной системы расположены, как правило, в сером веществе боковых рогах спинного мозга от 8 шейного до 2-3 поясничных сегментов. Таким образом, симпатические нервы всегда отходят только от спинного мозга в составе спинномозговых нервов по передним (вентральным) корешкам.
Центральные нейроны парасимпатической же нервной системы находятся в крестцовых сегментах спинного мозга (2-4 сегменты), но большая часть центральных нейронов находятся в стволе мозга. Большая же часть нервов парасимпатической системы отходят от головного мозга в составе смешанных черепно — мозговых нервов. А именно : из среднего мозга в составе III пары (глазодвигательный нерв) — иннервируя мышцы ресничного тела и кольцевые мышцы зрачка глаза, из Варолиевого моста выходит лицевой нерв — VII пара (секреторный нерв) иннервирует железы слизистой оболочки носа, слёзные железы, подчелюстную и подъязычную железы. Из продолговатого мозга отходит IX пара — секреторный, языкоглоточный нерв, иннервирует околоушные слюнные железы и железы слизистой щек и губ, X пара (блуждающий нерв) — самая значительная часть парасимпатического отдела ВНС, проходя в грудную и брюшную полости, иннервирует весь комплекс внутренних органов. Нервы, отходящие от крестцовых сегментов (2-4 сегменты), иннервируют органы малого таза и входят в состав подчревного сплетения.
Из продолговатого мозга отходит IX пара — секреторный, языкоглоточный нерв, иннервирует околоушные слюнные железы и железы слизистой щек и губ, X пара (блуждающий нерв) — самая значительная часть парасимпатического отдела ВНС, проходя в грудную и брюшную полости, иннервирует весь комплекс внутренних органов. Нервы, отходящие от крестцовых сегментов (2-4 сегменты), иннервируют органы малого таза и входят в состав подчревного сплетения.
Эффекторные нейроны симпатической нервной системы вынесены на периферию и находятся или в паравертебральных ганглиях (в симпатической нервной цепочке), или превертебрально. Постганглионарные волокна образуют различные сплетения. Среди них наиболее важное значение имеет чревное (солнечное) сплетение, но в его состав входят не только симпатические, но и парасимпатичесике волокна. Оно обеспечивает иннервацию всех органов расположенных в брюшной полости. Вот почему так опасны удары и травмы верхней части брюшной полости (примерно под диафрагму). Они способны вызвать шоковое состояние.
Они способны вызвать шоковое состояние.
Эффекторные нейроны парасимпатической нервной системы всегда находятся в стенках внутренних органов (интрамурально). Таким образом, у парасимпатических нервов большая часть волокон покрыты миелиновой оболочкой, и импульсы достигают эффекторных органов быстрее, чем у симпатической. Это обеспечивает парасимпатические нервные влияния, обеспечивающие сбережение ресурсов органа и организма в целом. Внутренние органы, расположенные в грудной и брюшной полости иннервируются главным образом блуждающим нервом (n. vagus), поэтому эти влияния часто называют вагусными (вагальными).
Имеются существенные различия и в их функциональных характеристиках.
Симпатический отдел, как правило, мобилизует ресурсы организма для осуществления энергичной деятельности (усиливается работа сердца, сужается просвет кровеносных сосудов и повышается артериальное давление, учащается дыхание, расширяются зрачки и т. п.), но происходит торможение работы пищеварительной системы, за исключением работы слюнных желез. У животных это происходит всегда (слюна нужна им для зализывание возможных ран), но и у некоторых людей при возбуждении слюноотделение усиливается.
п.), но происходит торможение работы пищеварительной системы, за исключением работы слюнных желез. У животных это происходит всегда (слюна нужна им для зализывание возможных ран), но и у некоторых людей при возбуждении слюноотделение усиливается.
Парасимпатическая, напротив, стимулирует работу пищеварительной системы. Неслучайно после сытного обеда отмечается вялость, нам так хочется поспать. При возбуждении парасимпатической нервная система обеспечивает восстановление равновесия внутренней среды организма. Она обеспечивает работу внутренних органов в состоянии покоя.
В функциональном смысле симпатическая и парасимпатическая системы являются антагонистами, дополняя друг друга в процессе поддержания гомеостазиса, поэтому многие органы получают двойную иннервацию — и со стороны симпатического, и со стороны парасимпатического отделов. Но, как правило, у разных людей преобладает или тот или другой отдел ВНС. Неслучайно известный отечественный физиолог Л.А. Орбели попытался классифицировать людей по этому признаку. Он выделил три типа людей: симпатикотоники (с преобладанием тонуса симпатической нервной системы) — их отличает сухость кожи, повышенная возбудимость; второй тип — ваготоники с преобладанием парасимпатических влияний — для них характерна жирная кожа, замедленные реакции. Третий тип — промежуточный. Л.А. Орбели считал знание этих типов важным для врачей, особенно при назначении доз лекарственных препаратов, т. к. одни и те же лекарственные препараты в одинаковой дозе по-разному влияют на пациентов с разным типом ВНС. Даже из повседневной практики каждый из нас может заметить, что чай и кофе вызывают различную реакцию у людей с разным типом функциональной активности ВНС. Из экспериментов на животных известно, что у животных с разным типом ВНС введение брома и кофеина так же оказывает различные реакции. Но на протяжении жизни человека его тип ВНС может изменяться в зависимости от возраста, периода полового созревания, беременности и других влияний.
Неслучайно известный отечественный физиолог Л.А. Орбели попытался классифицировать людей по этому признаку. Он выделил три типа людей: симпатикотоники (с преобладанием тонуса симпатической нервной системы) — их отличает сухость кожи, повышенная возбудимость; второй тип — ваготоники с преобладанием парасимпатических влияний — для них характерна жирная кожа, замедленные реакции. Третий тип — промежуточный. Л.А. Орбели считал знание этих типов важным для врачей, особенно при назначении доз лекарственных препаратов, т. к. одни и те же лекарственные препараты в одинаковой дозе по-разному влияют на пациентов с разным типом ВНС. Даже из повседневной практики каждый из нас может заметить, что чай и кофе вызывают различную реакцию у людей с разным типом функциональной активности ВНС. Из экспериментов на животных известно, что у животных с разным типом ВНС введение брома и кофеина так же оказывает различные реакции. Но на протяжении жизни человека его тип ВНС может изменяться в зависимости от возраста, периода полового созревания, беременности и других влияний. Несмотря на перечисленные различия, обе эти системы, однако, составляют единое функциональное целое, т. к. интеграция их функций осуществляется на уровне ЦНС. Вы уже знаете, что в сером веществе спинного мозга центры вегетативных и соматических рефлексов успешно соседствуют, также как они располагаются близко друг с другом в стволе мозга, и в высших подкорковых центрах. Так же как, в конечном счете, в единстве функционирует вся нервная система.
Несмотря на перечисленные различия, обе эти системы, однако, составляют единое функциональное целое, т. к. интеграция их функций осуществляется на уровне ЦНС. Вы уже знаете, что в сером веществе спинного мозга центры вегетативных и соматических рефлексов успешно соседствуют, также как они располагаются близко друг с другом в стволе мозга, и в высших подкорковых центрах. Так же как, в конечном счете, в единстве функционирует вся нервная система.
Подкорковые высшие центры ВНС находятся в гипоталамусе, который связан обширными нервными связями с другими отделами ЦНС. Гипоталамус является в то же время частью лимбической системы мозга. Функции вегетативной нервной системы, как известно, не контролируются сознанием человека. Но именно через гипоталамус и (связанный с ним гипофиз) высшие отделы ЦНС способны влиять на функциональную активность вегетативной нервной системы и через неё на функции внутренних органов. Функции дыхательной, сердечно-сосудистой, пищеварительной и других систем органов непосредственно регулируются вегетативными центрами, расположенными в среднем, продолговатом отделах головного и отделах спинного мозга, которые подчинены в своих функциях центрам гипоталамуса. В то же время туда же продолжаются ядра черной субстанции, черные ядра, располдоженные и в среднем мозге, ретикулярная формация.
В то же время туда же продолжаются ядра черной субстанции, черные ядра, располдоженные и в среднем мозге, ретикулярная формация.
Действительно, реализация влияния психических реакций человека на соматические – повышение артериального давления при гневе, повышенное потоотделение при страхе, пересыхание во рту при волнении и многие другие проявления психических состояний, – происходит при участии гипоталамуса и ВНС под влиянием коры больших полушарий.
Гипоталамус является частью промежуточного мозга. В нем можно выделить передний отдел (передний гипоталамус) и задний отдел (задний гипоталамус).В гипоталамусе расположены многочисленные скопления серого вещества — ядра. Их более 32 пар. По своему расположению они делятся на области — преоптическую, переднюю, среднюю и заднюю. В каждой из этих областей лежат группы ядер, отвечающих за вегетативную регуляцию функций, а также ядра, выделяющие нейрогормоны. Эти ядра различают также по их функциям.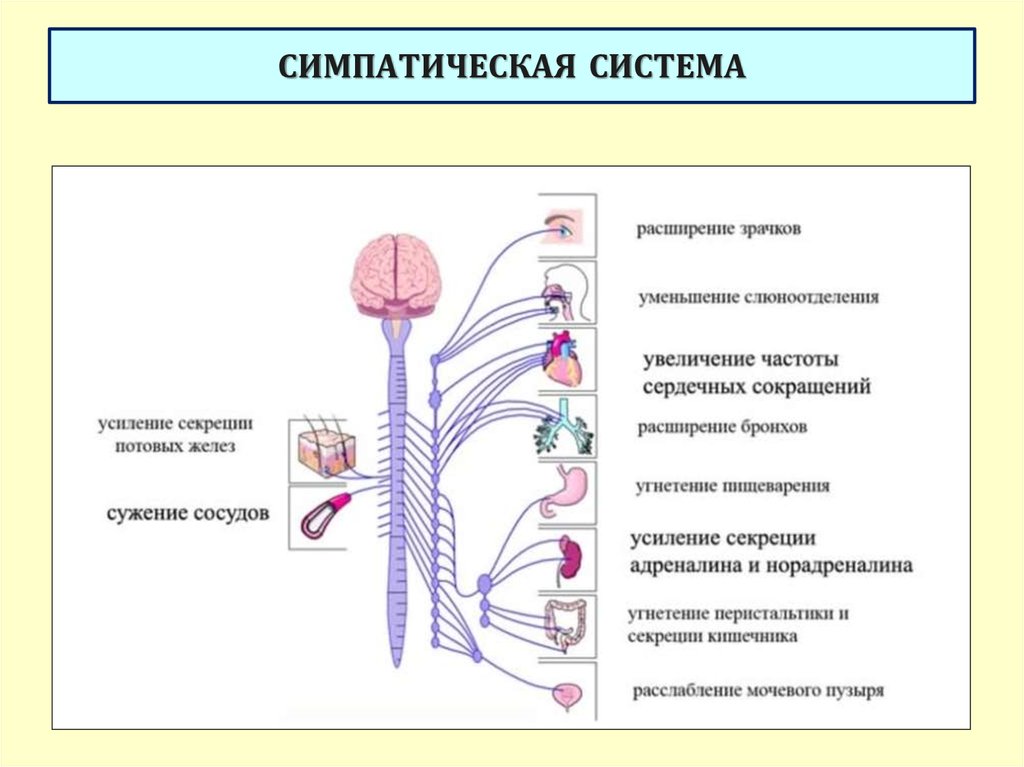 Так, в передней области находятся ядра, выполняющие функции регуляции теплоотдачи за счёт расширения кровеносных сосудов и увеличения отделения пота. А ядра, регулирующие теплопродукцию (за счёт повышения катаболических реакций и непроизвольных мышечных сокращений), располагаются в задней области гипоталамуса. В гипоталамусе расположены центры регуляции всех видов обмена веществ — белкового, жирового, углеводного, центры голода и насыщения. Среди групп ядер гипоталамуса находятся центры регуляции водно-солевого обмена, связанные с центром жажды, формирующего мотивацию поиска и потребления воды.
Так, в передней области находятся ядра, выполняющие функции регуляции теплоотдачи за счёт расширения кровеносных сосудов и увеличения отделения пота. А ядра, регулирующие теплопродукцию (за счёт повышения катаболических реакций и непроизвольных мышечных сокращений), располагаются в задней области гипоталамуса. В гипоталамусе расположены центры регуляции всех видов обмена веществ — белкового, жирового, углеводного, центры голода и насыщения. Среди групп ядер гипоталамуса находятся центры регуляции водно-солевого обмена, связанные с центром жажды, формирующего мотивацию поиска и потребления воды.
В передней области гипоталамуса лежат ядра, участвующие в процессах регуляции чередования сна и бодрствования (циркадных ритмов), а так же в регуляции полового поведения.
Проекции вегетативных центров представлены и в коре больших полушарий — в основном в лимбической и ростральной части коры. Парасимпатические и симпатические проекции одних и тех же органов проецируются в одни и те же или близко расположенные участки коры, это понятно, т.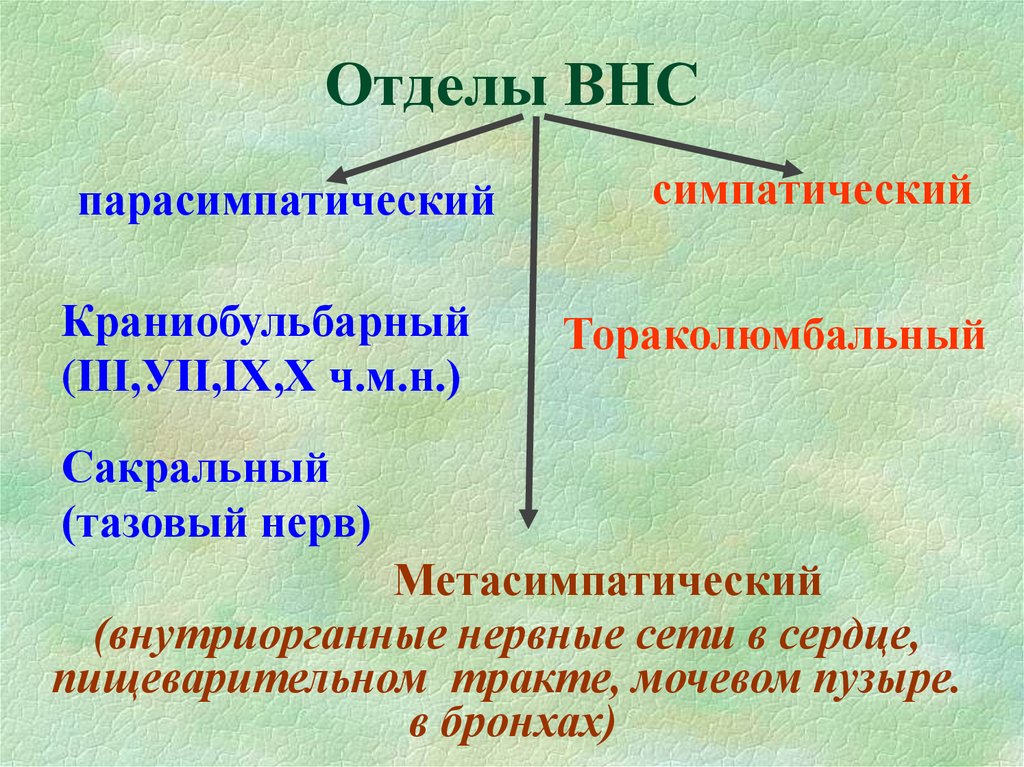 к. они совместно обеспечивают функции этих органов. Установлено, что парасмпатические проекции в коре представлены гораздо шире, чем симпатические, однако, функционально симпатические влияния более продолжительны, чем парасимпатические. Это связано с различиями медиаторов, которые выделяются окончаниями симатических (адреналин и норадреналин) и парасимпатических (ацетилхолин) волокон. Ацетилхолин — медиатор парасимпатической системы — быстро инактивируется ферментом ацетилхолинэстеразой (холинэстеразой) и её влияния быстро сходят на нет, в то время как адреналин и норадреналин инактивируются значительно медленнее (ферментом моноаминоксидазой), их влияние усиливается норадреналином и адреналином, выделяемыми надпочечниками. Таким образом, симпатические влияния длятся дольше и оказываются более выраженными, чем парасимпатические. Однако, во время сна парасимпатические влияния на все наши функции превалируют, что способствует восстановлению ресурсов организма.
к. они совместно обеспечивают функции этих органов. Установлено, что парасмпатические проекции в коре представлены гораздо шире, чем симпатические, однако, функционально симпатические влияния более продолжительны, чем парасимпатические. Это связано с различиями медиаторов, которые выделяются окончаниями симатических (адреналин и норадреналин) и парасимпатических (ацетилхолин) волокон. Ацетилхолин — медиатор парасимпатической системы — быстро инактивируется ферментом ацетилхолинэстеразой (холинэстеразой) и её влияния быстро сходят на нет, в то время как адреналин и норадреналин инактивируются значительно медленнее (ферментом моноаминоксидазой), их влияние усиливается норадреналином и адреналином, выделяемыми надпочечниками. Таким образом, симпатические влияния длятся дольше и оказываются более выраженными, чем парасимпатические. Однако, во время сна парасимпатические влияния на все наши функции превалируют, что способствует восстановлению ресурсов организма.
Но, несмотря на различия в строении и функциях различных отделов ВНС, различия соматической и вегетативной систем, — в конечном итоге, вся нервнаяя система работает как единое целое и интеграция происходит на всех уровнях как спинного, так и головного мозга.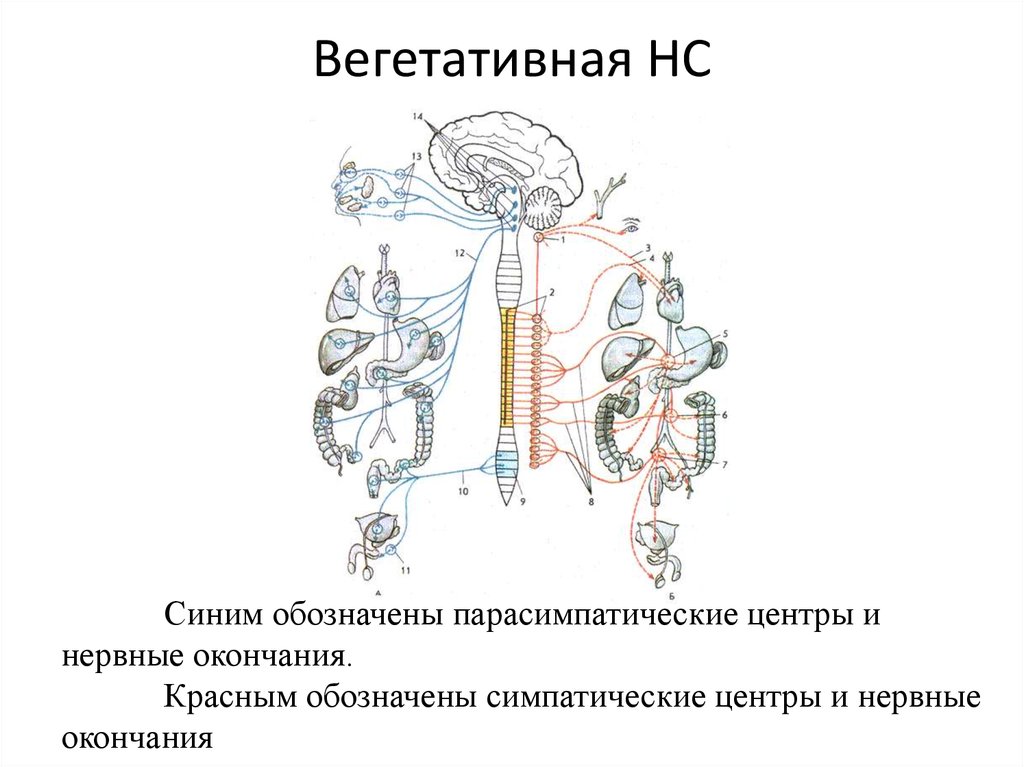 И высшим уровнем интеграции, безусловно, является кора больших полушарий головного мозга, объединяющая как нашу двигательную активность, работу наших внутренних органов так и, в конечном итоге, всю психическую деятельность человека.
И высшим уровнем интеграции, безусловно, является кора больших полушарий головного мозга, объединяющая как нашу двигательную активность, работу наших внутренних органов так и, в конечном итоге, всю психическую деятельность человека.
© 2011-2019 Сазонов В.Ф., Ендолов В.В., Муравьёва М.С.
© 2011-2016 kineziolog.bodhy.ru. © 2016-2019 kineziolog.su.
Вегетативная нервная система
Центробежные нервные волокна делятся на соматические и вегетативные.
Соматические нервная система проводят импульсы к скелетным поперечнополосатым мышцам, вызывая их сокращение. Соматическая нервная система осуществляет связь организма с внешней средой: воспринимает раздражение, регулирует работу скелетных мышц и органов чувств, обеспечивает разнообразные движения в ответ на раздражения, воспринимаемые органами чувств.
Вегетативные нервные волокна являются центробежными и идут к внутренним органам и системам, ко всем тканям организма, образуя вегетативную нервную систему.
Функция вегетативной нервной системы заключается в регулировании физиологических процессов в организме, в обеспечении приспособления организма к меняющимся условиям среды. Центры вегетативной нервной системы расположены в среднем, продолговатом и спинном мозге, а периферическая часть состоит из нервных узлов и нервных волокон, иннервирующих рабочий орган.
Вегетативная нервная система состоит из двух частей: симпатической и парасимпатической.
Симпатическая часть вегетативной нервной системы связана со спинным мозгом, от 1-го грудного до 3-го поясничного позвонка.
Парасимпатическая часть залегает в среднем продолговатом отделе головного и крестцовом отделе спинного мозга.
Большинство внутренних органов получают двойную вегетативную иннервацию, так как к ним подходят как симпатические, так и парасимпатические нервные волокна, которые функционируют в тесном взаимодействии, оказывая на органы противоположный эффект. Если первые, например, усиливают какую-либо активность, то вторые ослабляют ее, что показано в таблице.
| Орган | Действие симпатических нервов | Действие парасимпатических органов |
| 1 | 2 | 3 |
| Сердце | Усиление и учащение сердечных сокращений | Ослабление и замедление сердечных сокращений |
| Артерии | Сужение артерий и повышение кровяного давления | Расширение артерий и понижение кровяного давления |
| Пищеварительный тракт | Замедление перистальтики, уменьшение активности | Ускорение перистальтики, повышение активности |
| Мочевой пузырь | Расслабление пузыря | Сокращение пузыря |
| Мускулатура бронхов | Расширение бронхов, облегчение дыхания | Сокращение бронхов |
| Мышечные волокна радужной оболочки | Расширение зрачка | Сужение зрачка |
| Мышцы, поднимающие волосы | Поднятие волос | Прилегание волос |
| Потовые железы | Усиление секреции | Ослабление секреции |
Симпатическая нервная система усиливает обмен веществ, повышает возбудимость большинства тканей, мобилизует силы организма на активную деятельность.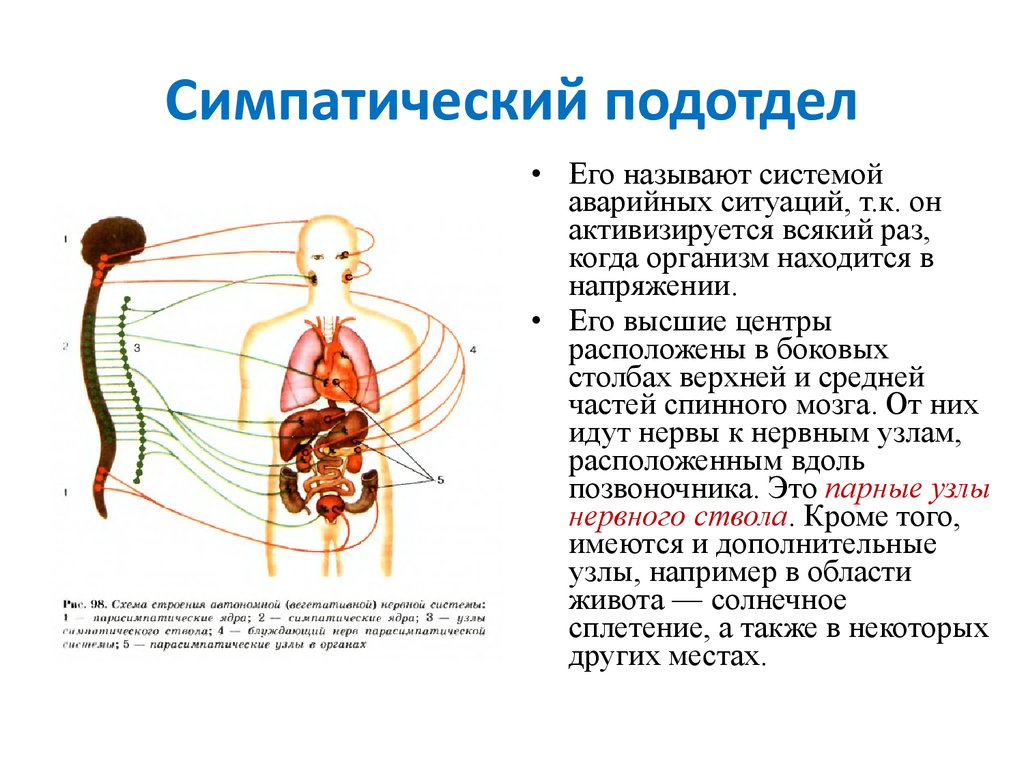 Парасимпатическая нервная система способствует восстановлению израсходованных запасов энергии, регулирует жизнедеятельность организма во время сна.
Парасимпатическая нервная система способствует восстановлению израсходованных запасов энергии, регулирует жизнедеятельность организма во время сна.
Вся деятельность вегетативной (автономной) нервной системы регулируется подбугровой областью — гипоталамусом промежуточного мозга, связанного со всеми отделами центральной нервной системы и с железами внутренней секреции.
Гуморальная регуляция функций организма — древнейшая форма химического взаимодействия клеток организма, осуществляемая продуктами обмена веществ, которые разносятся кровью по всему телу и оказывают влияние на деятельность других клеток, тканей, органов.
Основными факторами гуморальной регуляции являются биологически активные вещества — гормоны, которые выделяются эндокринными железами (железами внутренней секреции), образующими в организме эндокринную систему. Эндокринная и нервная системы тесно взаимодействуют в регуляторной деятельности, отличаясь лишь тем, что эндокринная система контролирует процессы, протекающие сравнительно медленно и длительно. Нервная система управляет быстрыми реакциями, чья длительность может измеряться миллисекундами.
Нервная система управляет быстрыми реакциями, чья длительность может измеряться миллисекундами.
Гормоны вырабатываются особыми железами, богато снабженными кровеносными сосудами. Эти железы не имеют выводных протоков, и их гормоны поступают непосредственно в кровь, а затем разносятся по всему телу, осуществляя гуморальную регуляцию всех функций: они возбуждают или угнетают деятельность организма, влияют на его рост и развитие, изменяют интенсивность обмена веществ. В связи с отсутствием выводных протоков эти железы называются железами внутренней секреции, или эндокринными, в отличие от пищеварительных, потовых, сальных желез внешней секреции, имеющих выводные протоки.
К железам внутренней секреции относятся: гипофиз, щитовидная железа, околощитовидные железы, над почечники, эпифиз, островковая часть поджелудочной железы, внутрисекреторная часть половых желез.
Железы внутренней секреции
Гипофиз — нижний мозговой придаток, одна из центральных желез внутренней секреции. Гипофиз состоит из трех долей: передней, средней и задней, окруженных общей капсулой из соединительной ткани.
Гипофиз состоит из трех долей: передней, средней и задней, окруженных общей капсулой из соединительной ткани.
Один из гормонов передней доли оказывает влияние па рост. Избыток этого гормона в молодом возрасте сопровождается резким усилением роста — гигантизм, а при повышенной функции гипофиза у взрослого, когда рост тела прекращается, наступает усиленный рост коротких костей: предплюсны, плюсны, фаланг пальцев, а также мягких тканей (языка, носа). Такая болезнь называется акромегалией. Повышенная функция передней доли гипофиза приводит к карликовому росту. Гипофизарные карлики пропорционально сложены и нормально умственно развиты. В передней доле гипофиза образуются также гормоны, влияющие на обмен жиров, белков, углеводов. В задней доле гипофиза вырабатывается гормон, снижающий скорость образования мочи и изменяющий водный обмен в организме.
Щитовидная железа лежит поверх щитовидного хряща гортани, выделяет в кровь гормоны, в состав которых входит йод. Недостаточная функция щитовидной железы в детском возрасте задерживает рост, умственное и половое развитие, развивается болезнь кретинизм.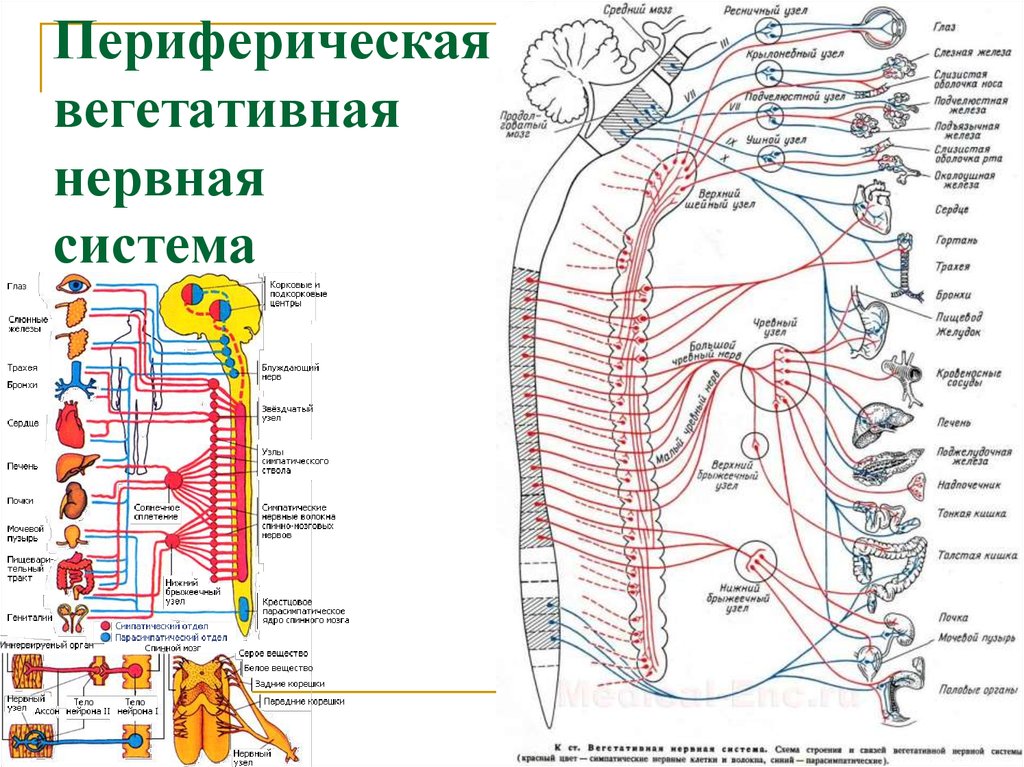 В другие периоды это приводит к снижению обмена веществ, при этом нервная деятельность замедляется, развиваются отеки, проявляются признаки тяжелого заболевания, называемого микседемой. Избыточная деятельность щитовидной железы приводит к базедовой болезни. Щитовидная железа при этом увеличивается в объеме и выступает на шее в виде зоба.
В другие периоды это приводит к снижению обмена веществ, при этом нервная деятельность замедляется, развиваются отеки, проявляются признаки тяжелого заболевания, называемого микседемой. Избыточная деятельность щитовидной железы приводит к базедовой болезни. Щитовидная железа при этом увеличивается в объеме и выступает на шее в виде зоба.
Эпифиз (шишковидная железа) — мелких размеров, расположен в промежуточном мозге. Изучен еще недостаточно. Предполагается, что гормоны эпифиза тормозят выделение гормонов роста гипофизом. Ее гормон — мелатонин влияет на пигменты кожи.
Надпочечники — парные железы, расположенные у верхнего края почек. Их масса около 12 г каждая, вместе с почками они покрыты жировой капсулой. В них различают корковое, более светлое вещество, и мозговое, темное. Они вырабатывают несколько гормонов. В наружном (корковом) слое образуются гормоны — кортикостероиды, оказывающие влияние на солевой и углеводный обмен, способствующие отложению гликогена в клетках печени и поддерживающие постоянную концентрацию глюкозы в крови. При недостаточной функции коркового слоя развивается Аддисонова болезнь, сопровождающаяся мышечной слабостью, одышкой, потерей аппетита, уменьшением концентрации в крови сахара, понижением температуры тела. Характерный признак такого заболевания — бронзовый оттенок кожи.
При недостаточной функции коркового слоя развивается Аддисонова болезнь, сопровождающаяся мышечной слабостью, одышкой, потерей аппетита, уменьшением концентрации в крови сахара, понижением температуры тела. Характерный признак такого заболевания — бронзовый оттенок кожи.
В мозговом слое надпочечников вырабатывается гормон — адреналин. Его действие многообразно: он увеличивает частоту и силу сердечных сокращений, повышает кровяное давление, усиливает обмен веществ, особенно углеводов, ускоряет превращение гликогена печени и работающих мышц в глюкозу, в результате чего работоспособность мыши восстанавливается.
Поджелудочная железа функционирует как смешанная железа. Вырабатываемый ею поджелудочный сок по выводным протокам попадает в двенадцатиперстную кишку и принимает участие в процессе расщепления питательных веществ. Это внешнесекреторная функция. Внутрисекреторную функцию выполняют особые клетки (островки Лангерганса), не имеющие выводных протоков и выделяющие гормоны прямо в кровь.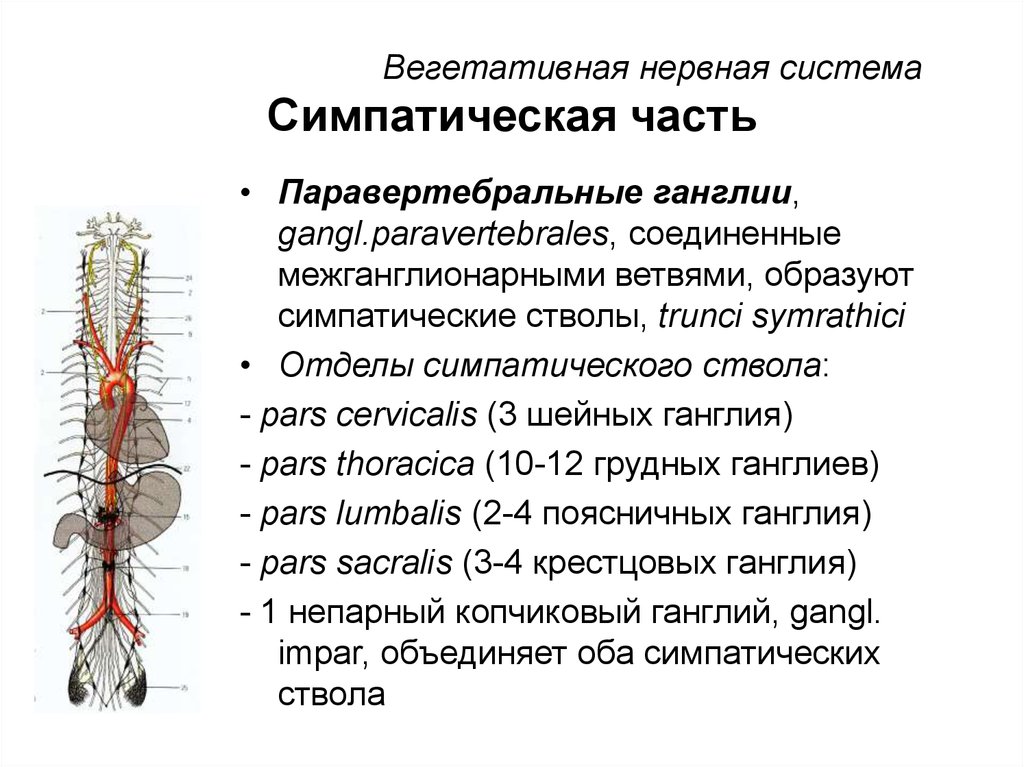 Один из них — инсулин — превращает избыток глюкозы в крови в животный крахмал гликоген и понижает уровень сахара в крови. Другой гормон — глюкоген — действует на углеводный обмен противоположно инсулину. При его действии происходит процесс превращения гликогена в глюкозу. Нарушение процесса образования инсулина в поджелудочной железе вызывает болезнь — сахарный диабет.
Один из них — инсулин — превращает избыток глюкозы в крови в животный крахмал гликоген и понижает уровень сахара в крови. Другой гормон — глюкоген — действует на углеводный обмен противоположно инсулину. При его действии происходит процесс превращения гликогена в глюкозу. Нарушение процесса образования инсулина в поджелудочной железе вызывает болезнь — сахарный диабет.
Половые железы являются также смешанными железами, образующими половые гормоны.
В мужских половых железах — семенниках — развиваются мужские половые клетки — сперматозоиды и вырабатываются мужские половые гормоны (андрогены, тестостерон). В женских половых железах — яичниках — содержатся яйцеклетки, вырабатывающие гормоны (эстрогены).
Под действием гормонов, выделяемых в кровь семенниками, происходит развитие вторичных половых признаков, характерных для мужского организма (волосяной покров на лице — борода, усы, развитый скелет и мускулатура, низкий голос).
Гормоны, образующиеся в яичниках, влияют на формирование вторичных половых признаков, характерных для женского организма (отсутствие волосяного покрова на лице, более тонкие, чем у мужчины, кости, отложение жира под кожей, развитые молочные железы, высокий голос).
Деятельность всех желез внутренней секреции взаимосвязана: гормоны передней доли гипофиза способствуют развитию коркового вещества надпочечников, усиливают секрецию инсулина, влияют на поступление в кровь тироксина и на функцию половых желез.
Работу всех желез внутренней секреции регулирует центральная нервная система, в которой находится ряд центров, связанных с функцией желез. В свою очередь гормоны влияют на деятельность нервной системы. Нарушение взаимодействия этих двух систем сопровождается серьезными расстройствами функций органов и организма в целом.
Следовательно, взаимодействие нервной и гуморальной системы следует рассматривать как единый механизм нейрогуморальной регуляции функций, обеспечивающей целостность человеческого организма.
Запись опубликована в рубрике Биология человека с метками нервная система, система органов, человек. Добавьте в закладки постоянную ссылку.
58. КЛАССИФИКАЦИЯ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ. ЦЕНТРАЛЬНЫЕ И ПЕРИФЕРИЧЕСКИЕ ОТДЕЛЫ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ.
 ОТЛИЧИЯ ВНС ОТ СОМАТИЧЕСКОЙ, СИМПАТИЧЕСКОЙ НС ОТ ПАРАСИМПАТИЧЕСКОЙ.
ОТЛИЧИЯ ВНС ОТ СОМАТИЧЕСКОЙ, СИМПАТИЧЕСКОЙ НС ОТ ПАРАСИМПАТИЧЕСКОЙ.КВ Оригинал Согласование
(координация) моторных функций организма и вегетативных (обмен веществ,
кровообращение, дыхание, пищеварение, выделение и др.) осуществляется
лимбической системой и лобными долями больших полушарий. Раздражение коры
лобных долей изменяет сердечную деятельность и дыхание, пульс, артериальное
давление, вызывает отделение слюны, движение желудочно-кишечного тракта, т. |
Расстройства вегетативной нервной системы в Нейровегетологии — клиника интимной медицины «Мужское здоровье»
Вы здесь
Главная » Расстройства вегетативной нервной системы
Расстройства вегетативной
нервной системы
Вегетативная нервная система и ее нарушения в урологии сексопатологии
Вегетативная нервная система — совокупность центров и путей, обеспечивающих регулирование внутренней среды организма и адаптацию организма к воздействиям внешней среды.
Вегетативная нервная система тесно связана с соматической нервной системой, так как все двигательные реакции получают вегето-трофическое обеспечение, а сами двигательные реакции, в свою очередь, влияют на регуляцию вегетативных функций. Особенности вегетативной нервной системы
Особенности вегетативной нервной системы
В основе лежит рефлекторный принцип регуляции Вегетативные сегментарные эфферентные пути всегда двухнейронны.
Центры вегетативной нервной системы располагаются в головном мозге и боковых рогах спинного мозга.
Вегетативная нервная система:
- Симпатическая. Обеспечивает адаптацию внутренней среды организма к меняющимся условиям внешней среды (обеспечивает реакцию организма на неожиданный раздражитель).
- Парасимпатическая. Обеспечивает стабилизацию внутренней среды организма.
При нарушении функции соматической нервной системы вегето-трофическое обеспечение органа нарушается и становится либо повышенной, сниженной либо парадоксальной (т.е. при поступлении команды от центральных структур или периферических о снижении или увеличении функции, функция выполняется противоположная).
Лечение. В основе принципа лечения лежит разрушение патологического рефлекса. Подходы и подбор методик зависят от индивидуальных особенностей организма пациента и заболеваний, приведших к данной патологии: индивидуальная чувствительность и переносимость ганглиоблокаторов, чувствительность к гомеопатическим средствам, реакция на физиопроцедуры, необходимость использования имунносупресивной терапии при аутоиммунных ганглиолитах.
Подходы и подбор методик зависят от индивидуальных особенностей организма пациента и заболеваний, приведших к данной патологии: индивидуальная чувствительность и переносимость ганглиоблокаторов, чувствительность к гомеопатическим средствам, реакция на физиопроцедуры, необходимость использования имунносупресивной терапии при аутоиммунных ганглиолитах.
Читать далее
преимущества
Симпатическая нервная система (периферическая часть)
Пограничный симпатический ствол обычно включает в себя 20-25 симпатических узлов, соединенных между собой продольными волокнами. В шейном и грудном отделе узлы симпатической системы располагаются по бокам позвоночного столба, а в поясничном и крестцовом отделах — по передней поверхности позвоночника.
Шейный отдел спинного мозга (содержит три симпатических нервных узла) Верхний шейный узел. Отдает постганглионарные нервные волокна к четырем верхним шейным корешковым нервам, к сплетениям наружной и внутренней сонных артерий, подъязычному и диафрагмальному нервам.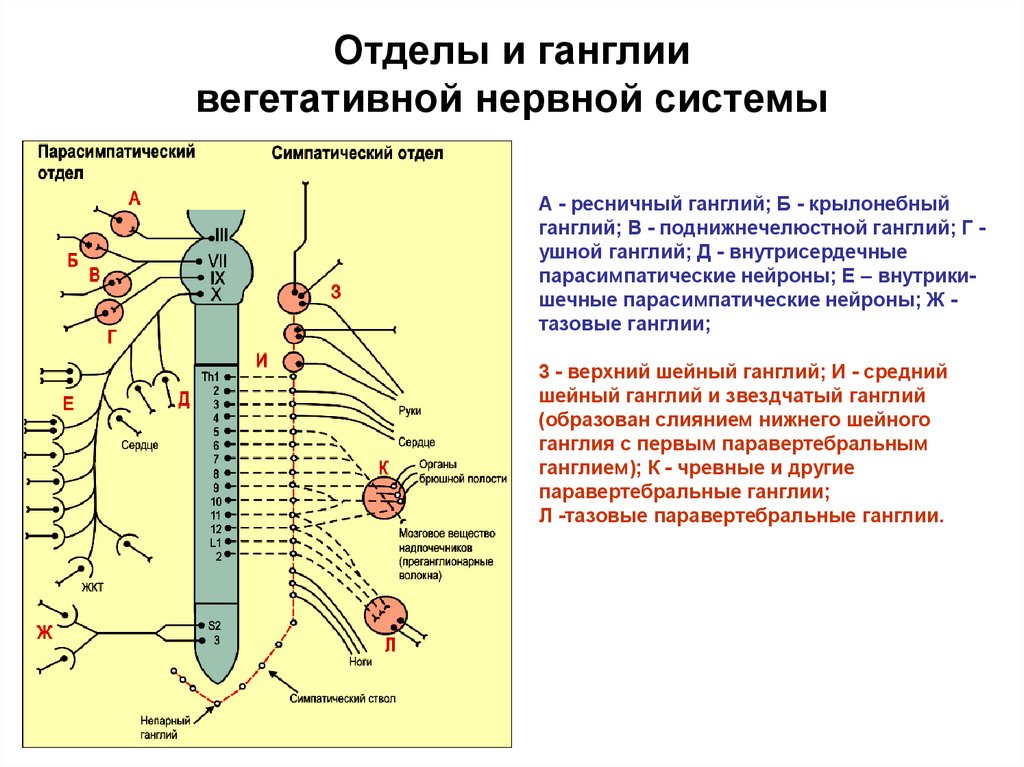 Средний шейный узел и нижний шейный узел. Отдают постганглионарные нервные волокна к 5-8 шейным и 1 грудному корешковым нервам, щитовидной железе, общей сонной артерии и подключичным артериям.
Средний шейный узел и нижний шейный узел. Отдают постганглионарные нервные волокна к 5-8 шейным и 1 грудному корешковым нервам, щитовидной железе, общей сонной артерии и подключичным артериям.
Часто второй и третий шейные симпатические узлы, сливаясь с первым грудным симпатическим узлом, образуют «звездчатый узел», отдающий волокна к 6-8 шейным корешковым нервам, позвоночным артериям и сердцу. Грудной отдел спинного мозга (содержит 10-12 симпатических нервных узлов). Постганглионарные волокна симпатических узлов грудного отдела спинного мозга следуют к межреберным нервам, сосудам и органам грудной и брюшной полостей.
- От Th5-Th5 — волокна к сердечному сплетению
- От Th5-Th20 — волокна к солнечному сплетению
- Поясничный отдел спинного мозга (содержит три-четыре симпатических нервных узла).
- Постганглионарные нервные волокна следуют к корешковым нервам, солнечному сплетению и брюшному отделу аорты.
- Крестцовый отдел спинного мозга (содержит три-четыре симпатических нервных узла)
- Постганглионарные нервные волокна следуют к крестцовым корешковым нервам и иннервируют органы малого таза.

Однако между соматической и симпатической нервными системами нет полного соответствия в сегментарной иннервации органов и систем. Так C8-Th4 сегменты осуществляют иннервацию головы и шеи, Th5-Th7 — рук, а Th8-Th9 — ног.
Лечение. При различных поражениях этих узлов появляется сегментарное нарушение функции органов иннервируемых данным нервным волокном. Восстановление проводимости волокна и его нормальное функционирование – принцип лечения таких больных. В основном это обеспечение анатомически правильным положением нервного корешка в костном канале, онконастороженность, лечение и санация тех воспалительных процессов, которые находятся вблизи нервных структур. Слежение за состоянием иммунной системы (системные заболевания, аутоиммунные агрессии, псевдоаллергические реакции).
Парасимпатическая нервная система
Основные центры:
- Средний мозг (мезэнцефальный отдел парасимпатической нервной системы.
 Включает в себя ядро Якубовича и центральное хвостовое ядро Перлиа, волокна, которых следуют в составе глазодвигательных нервов.
Включает в себя ядро Якубовича и центральное хвостовое ядро Перлиа, волокна, которых следуют в составе глазодвигательных нервов. - Продолговатый мозг (бульбарный отдел парасимпатической нервной системы). Включает в себя секреторные и слюноотделительные ядра (верхние и нижние), иннервирующие слезные и слюнные железы, а так же заднее ядро блуждающего нерва (иннервирующее внутренние органы, гладкую мускулатуру и железы).
- Крестцовые сегменты спинного мозга (сакральный, крестцовый отдел спинного мозга). Тазовый нерв, образованный волокнами крестцового отдела парасимпатической системы, обеспечивает иннервацию органов малого таза (мочевого пузыря, прямой кишки и половых органов).
Нарушения в каждом из подразделений вызывают четкий, патологический симтомокомплекс.
Лечение. Осуществляется по тем же принципам, с учетом этиопатогенетических факторов, посиндромно.
Заседа Юрий Игоревич
Андролог, сексолог, уролог, репродуктолог, психотерапевт.
Опыт врачебной практики более 31 года.
Врач высшей категории. Доктор медицинских наук. Основатель и главный врач клиники.
Соломенный Руслан Иванович
Врач уролог, специалист УЗИ
Опыт врачебной практики более 5 лет.
Вегетативная нервная система: функции и отделы
Определение
Вегетативная нервная система представляет собой сложный набор нейронов, которые опосредуют внутренний гомеостаз без сознательного вмешательства или произвольного контроля. Эта система иннервирует большинство частей тела и влияет на их активность, а также опосредует изменения в общем обмене веществ. Ее можно разделить на симпатических и парасимпатических нервных систем.
Обзор
Вегетативная нервная система (ВНС) поддерживает артериальное давление, регулирует частоту дыхания, влияет на пищеварение, мочеиспускание и модулирует сексуальное возбуждение. Симпатическая часть ВНС контролирует такие реакции, как реакция на стресс и реакция «бей или беги». Парасимпатическая часть ВНС контролирует реакции, связанные с приемом пищи, ростом и размножением.
Парасимпатическая часть ВНС контролирует реакции, связанные с приемом пищи, ростом и размножением.
Вегетативную нервную систему можно противопоставить соматической нервной системе , которая контролируется произвольно. В то время как вегетативная нервная система контролирует такие вещи, как частота сердечных сокращений и пищеварение, соматическая нервная система контролирует такие вещи, как движения мышц. Дыхание — это функция, которая может переключаться между вегетативной и соматической нервными системами; вот почему вы можете задерживать дыхание, но также и поэтому вам никогда не приходится думать о дыхании.
Функция вегетативной нервной системы
Вегетативная нервная система контролирует многие системы, включая сердечно-сосудистую систему. Он может изменять силу и скорость сокращения сердца, а также сужение и расширение кровеносных сосудов. Следовательно, он также влияет на кровяное давление. Скорость дыхания также может изменяться вегетативной нервной системой. Он влияет как на скелетные, так и на гладкомышечные волокна по всему телу, независимо от того, изменяет ли он метаболизм глюкозы в скелетных мышцах или вызывает расширение зрачка глаза.
Скорость дыхания также может изменяться вегетативной нервной системой. Он влияет как на скелетные, так и на гладкомышечные волокна по всему телу, независимо от того, изменяет ли он метаболизм глюкозы в скелетных мышцах или вызывает расширение зрачка глаза.
Вегетативная нервная система может влиять на эффективность пищеварения, изменяя секрецию ферментов железами и скорость перистальтики. Например, активация симпатической нервной системы замедляет пищеварение и направляет кровоток в сторону скелетных мышц. Это может ослабить сексуальное возбуждение и отключить большинство второстепенных функций организма. С другой стороны, вегетативная нервная система может также усиливать пищеварительную секрецию, перистальтические движения, поддерживать нормальные циклы циркадной активности, способствовать глубокому сну и активировать механизмы восстановления организма.
Непроизвольные действия, такие как чихание, глотание или рвота, также контролируются ВНС. Имеются данные о том, что вегетативная нервная система не только влияет на сексуальное возбуждение, но также играет решающую роль в поддержании беременности и индукции родов. Наконец, вегетативная нервная система также изменяет диурез и частоту мочеиспускания.
Наконец, вегетативная нервная система также изменяет диурез и частоту мочеиспускания.
Отделы вегетативной нервной системы
Существуют два основных отдела вегетативной нервной системы. Во-первых, это симпатическая нервная система. Симпатическая нервная система обычно контролирует ответ «беги или сражайся» . Это включает высвобождение гормонов стресса, регулирование метаболизма клеток и общее поддержание гомеостаза в организме.
Вторым отделом вегетативной нервной системы является парасимпатическая нервная система. Этот отдел обычно контролирует реакции «корми или размножайся» , включая поведение по сбору пищи, ритуалы спаривания и сексуальную активность. В большинстве случаев физиологический ответ парасимпатической нервной системы прямо противоположен результатам, опосредованным симпатической нервной системой.
Вегетативная нервная система содержит два типа нейронов, которые взаимодействуют друг с другом в ганглиях около спинного мозга. Начальные преганглионарные нейроны начинаются в центральной нервной системе в разных отделах спинного мозга. Эти преганглионарные нейроны образуют синапсы с постганглионарными нейронами в ганглиях, украшающих обе стороны спинного мозга. Постганглионарный нейрон образует синапс с эффекторными клетками.
Начальные преганглионарные нейроны начинаются в центральной нервной системе в разных отделах спинного мозга. Эти преганглионарные нейроны образуют синапсы с постганглионарными нейронами в ганглиях, украшающих обе стороны спинного мозга. Постганглионарный нейрон образует синапс с эффекторными клетками.
Нейроны симпатической нервной системы выходят из грудного и поясничного отделов спинного мозга, а парасимпатические нейроны связаны с краниальным и крестцовым отделами. Симпатическая нервная система обычно активируется в ответ на чрезвычайные ситуации, особенно те, которые угрожают выживанию. С другой стороны, парасимпатическая реакция связана с усилением роста и размножения.
Диаграмма вегетативной нервной системыПримеры реакции вегетативной нервной системы
Реакции борьбы или бегства
Вегетативная нервная система часто описывается с использованием реакции на неминуемую физическую опасность и восстановления организма после того, как угроза отступила. Например, столкнувшись с хищником, тело увеличивает частоту сердечных сокращений и дыхания, снижает пищеварительную секрецию и активность и преимущественно направляет кровь к скелетным мышцам, чтобы тело могло физически бороться с вызовом. Это обычно сопровождается пилоэрекцией для сохранения тепла тела.
Например, столкнувшись с хищником, тело увеличивает частоту сердечных сокращений и дыхания, снижает пищеварительную секрецию и активность и преимущественно направляет кровь к скелетным мышцам, чтобы тело могло физически бороться с вызовом. Это обычно сопровождается пилоэрекцией для сохранения тепла тела.
Вот почему считается, что симпатическая нервная система опосредует реакцию «бей или беги». Как только ситуация становится более спокойной, парасимпатическая нервная система восстанавливает нормальную работу организма, возобновляя пищеварение и выделение, снижая кровяное давление и восстанавливая нормальные циркадные ритмы.
Общая активность
Однако даже при отсутствии внешней угрозы две ветви вегетативной нервной системы претерпевают изменения и тесно взаимодействуют с эндокринной системой для ежеминутного мониторинга внутренней и внешней среды. Например, симпатическая активация может привести к увеличению уровней циркулирующего в плазме адреналина и норадреналина, секретируемых надпочечниками.
Обычно частота сердечных сокращений увеличивается во время вдоха и уменьшается во время выдоха. Это изменение является нормальным и зависит от блуждающего нерва и, следовательно, от вегетативной нервной системы. Когда вариабельность сердечного ритма снижается, это указывает на снижение парасимпатической активности.
Гормоны и вегетативная нервная система
Гормоны также могут изменять реакцию вегетативной нервной системы. У фертильных репродуктивных самок млекопитающих это взаимодействие между ВНС и эндокринной системой представляет особый интерес. Эстроген участвует в повышении активности важнейшей части парасимпатической нервной системы — блуждающего нерва. Эстроген одновременно подавляет активность симпатической нервной системы. Гормон прогестерон оказывает противоположное действие.
В фолликулярную фазу менструального цикла в кровотоке повышается концентрация эстрогенов. Под влиянием повышенных концентраций эстрогенов в плазме происходит усиление активности парасимпатической нервной системы, что вызывает повышение вариабельности сердечного ритма. С другой стороны, во время лютеиновой фазы менструального цикла вариабельность сердечного ритма указывает на снижение активности блуждающего нерва. Это свидетельствует о другом сдвиге в симпатовагальном балансе. Важность этих изменений сердечно-сосудистой микросреды до конца не изучена, но предполагается, что это может объяснить различия в риске сердечно-сосудистых заболеваний у мужчин и женщин.
С другой стороны, во время лютеиновой фазы менструального цикла вариабельность сердечного ритма указывает на снижение активности блуждающего нерва. Это свидетельствует о другом сдвиге в симпатовагальном балансе. Важность этих изменений сердечно-сосудистой микросреды до конца не изучена, но предполагается, что это может объяснить различия в риске сердечно-сосудистых заболеваний у мужчин и женщин.
Однако важно отметить, что основные параметры сердечно-сосудистой системы, такие как артериальное давление или частота сердечных сокращений, практически не зависят от фазы менструального цикла благодаря другим компенсаторным механизмам.
Вегетативная нервная система и сердечно-сосудистая система
Взаимодействие между вегетативной нервной системой и сердечно-сосудистой системой становится еще более важным во время беременности, поскольку происходят широкомасштабные изменения гемодинамики. Объем крови, базальное потребление кислорода, масса эритроцитов, сердечный выброс и увеличение частоты сердечных сокращений у беременных женщин. Падает как систолическое, так и диастолическое кровяное давление, и происходит обширное ремоделирование всех кровеносных сосудов. Хотя изменение гормональной среды в первую очередь опосредует эти изменения, вегетативная нервная система также играет важную роль.
Падает как систолическое, так и диастолическое кровяное давление, и происходит обширное ремоделирование всех кровеносных сосудов. Хотя изменение гормональной среды в первую очередь опосредует эти изменения, вегетативная нервная система также играет важную роль.
Опять же, вариабельность сердечного ритма становится относительно чувствительным и неинвазивным показателем активности вегетативной нервной системы. Изучение вариабельности частоты сердечных сокращений у беременных в разные сроки гестации выявило усиление активности блуждающего нерва в I триместре на фоне снижения активации симпатической нервной системы. Это меняется по мере увеличения гестационного возраста с резкими всплесками нейронной активности симпатической нервной системы и высвобождением гормонов надпочечников, когда женщина приближается к сроку.
Заболевания вегетативной нервной системы
У людей существует широкий спектр заболеваний вегетативной нервной системы. Каждый год более 1 миллиона американцев испытывают дисфункцию вегетативной системы, известную как дизавтономия. Поскольку ВНС в основном отвечает за реакцию «бей или беги» и реакцию «размножайся и корми», любое расстройство, скорее всего, повлияет на одну из этих двух систем.
Поскольку ВНС в основном отвечает за реакцию «бей или беги» и реакцию «размножайся и корми», любое расстройство, скорее всего, повлияет на одну из этих двух систем.
Например, распространенным расстройством ВНС является эректильная дисфункция или неспособность мужчины достичь эрекции. Другие дизавтономии включают нарушение пищеварения, проблемы с контролем сердца или легких и другие нарушения, связанные с системами, которые обычно находятся под контролем подсознания. Поскольку ВНС контролирует так много аспектов тела, дизавтономии включают в себя огромный спектр расстройств.
Тест
1. Какое из этих утверждений о вегетативной нервной системе верно?
A. Не подлежит добровольному контролю
B. Влияет на сердечно-сосудистую систему
C. Взаимодействует с эндокринной системой.
D. Все вышеперечисленное
2. Какое из этих утверждений о блуждающем нерве верно?
А. Важная часть симпатической нервной системы
B. Увеличивает вариабельность сердечного ритма
Увеличивает вариабельность сердечного ритма
C. Повышенная активность в третьем триместре беременности.
D. Все вышеперечисленное
3. Группа хирургов усердно работает над пересадкой печени. Процедура длится более 12 часов, в течение которых они в основном стояли, глубоко сосредотачивались и пристально смотрели на операционные поверхности. Если бы можно было измерить их физиологические параметры, какие из этих изменений были бы видны в их телах?
A. Повышение превращения глюкозы в гликоген в скелетных мышцах
B. Сужение зрачков
C. Изменения уровня мелатонина
D. Все вышеперечисленное
D.
4. Что из перечисленного НЕ является функцией вегетативной нервной системы?
A. Ваши зрачки расширяются в зависимости от уровня освещения в комнате.
B. Вы хотите достать банку с фасолью на верхней полке, поэтому поднимаете руку над головой.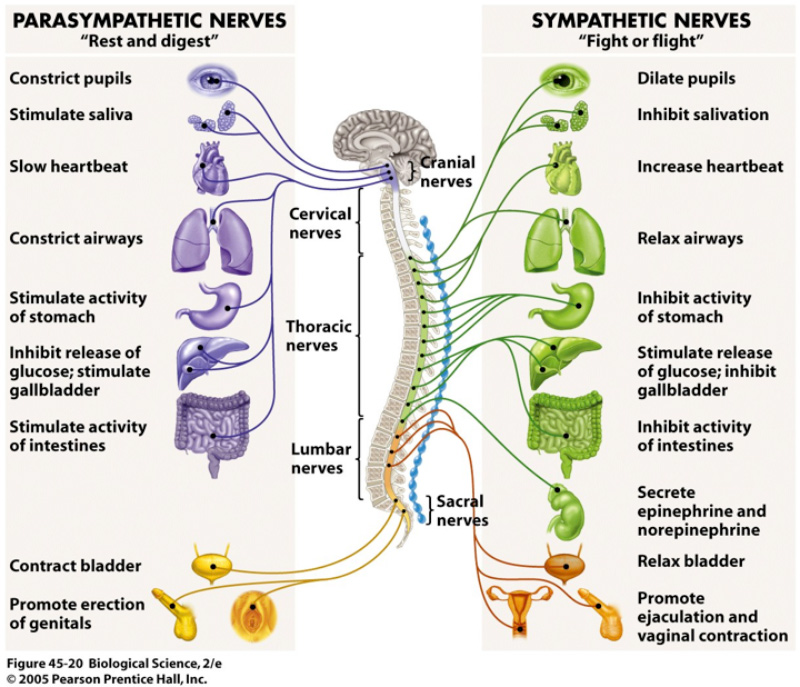
C. Частота вашего дыхания увеличивается по мере того, как гормон стресса кортизол воздействует на вашу систему.
Д. Ничего из вышеперечисленного.
5. В чем основное различие между вегетативной нервной системой и соматической нервной системой?
А. Разницы нет.
B. Соматика в основном произвольна и рефлексивна, тогда как вегетативная нервная система контролирует действия подсознания.
C. Соматическая система контролирует действия подсознания, тогда как вегетативная система контролирует произвольные действия.
Дизавтономия | Заболевания вегетативной нервной системы
Также называется: дисавтономия
На этой странице
Основы
- Резюме
- Начните здесь
- Диагностика и тесты
Узнать больше
- Особенности
- Генетика
Смотрите, играйте и учитесь
- Ссылки недоступны
Исследования
- Клинические испытания
- Журнальная статья
Ресурсы
- Найти эксперта
Для вас
- Дети
- Раздаточные материалы для пациентов
Ваша вегетативная нервная система — это часть вашей нервной системы, которая контролирует непроизвольные действия, такие как биение сердца и расширение или сужение кровеносных сосудов. Когда что-то пойдет не так в этой системе, это может вызвать серьезные проблемы, в том числе:
Когда что-то пойдет не так в этой системе, это может вызвать серьезные проблемы, в том числе:
- Проблемы с артериальным давлением
- Проблемы с сердцем
- Проблемы с дыханием и глотанием
- Эректильная дисфункция у мужчин
Нарушения вегетативной нервной системы могут возникать самостоятельно или в результате другого заболевания, такого как болезнь Паркинсона, алкоголизм и диабет. Проблемы могут затрагивать либо часть системы, как при комплексных регионарных болевых синдромах, либо всю систему. Некоторые типы являются временными, но многие со временем ухудшаются. Когда они влияют на ваше дыхание или работу сердца, эти расстройства могут быть опасными для жизни.
Некоторые расстройства вегетативной нервной системы улучшаются при лечении основного заболевания. Однако часто нет никакого лечения. В этом случае целью лечения является улучшение симптомов.
NIH: Национальный институт неврологических расстройств и инсульта
- Автономная невропатия (Фонд Мэйо для медицинского образования и исследований) Также на Испанский
- дизавтономия (Национальный институт неврологических расстройств и инсульта)
- Обзор вегетативной нервной системы
(Мерк и Ко.
 , Инк.)
Также на Испанский
, Инк.)
Также на Испанский
- Барорефлексная недостаточность (Информационный центр генетических и редких заболеваний)
- Врожденный синдром центральной гиповентиляции (Информационный центр генетических и редких заболеваний)
- Синдром Холмса-Ади (Национальный институт неврологических расстройств и инсульта)
- Синдром Хорнера (Фонд Мэйо для медицинского образования и исследований)
- Множественная системная атрофия (Национальный институт неврологических расстройств и инсульта) — Краткое содержание Также на Испанский
- Множественная системная атрофия (Национальный институт неврологических расстройств и инсульта)
- Ортостатическая гипотензия (Национальный институт неврологических расстройств и инсульта)
- Синдром постуральной тахикардии (Национальный институт неврологических расстройств и инсульта)
- Чистая вегетативная недостаточность (Информационный центр генетических и редких заболеваний)
- ClinicalTrials.
 gov: Заболевания вегетативной нервной системы
(Национальные институты здоровья)
gov: Заболевания вегетативной нервной системы
(Национальные институты здоровья) - ClinicalTrials.gov: гипотензия, ортостатическая (Национальные институты здоровья)
- ClinicalTrials.
 gov: Множественная системная атрофия
(Национальные институты здоровья)
gov: Множественная системная атрофия
(Национальные институты здоровья)
- Статья: Связь маскированной артериальной гипертензии с вегетативной дисфункцией и кардиометаболическими параметрами:.
 ..
.. - Статья: Вариабельность сердечного ритма при наклоне головы вверх показывает индивидуальные различия у здоровых…
- Статья: Вегетативная дисфункция и метаболические нарушения как возможные последствия COVID-19.
 ..
.. - Заболевания вегетативной нервной системы — см. другие статьи
- Национальный институт неврологических расстройств и инсульта Также на Испанский
- Анизокория и синдром Горнера (Американская ассоциация детской офтальмологии и косоглазия)
5.
 Вегетативная нервная система • Функции клеток и организма человека
Вегетативная нервная система • Функции клеток и организма человекаСодержание:
1. Введение в вегетативную нервную систему
2. Устройство симпатической и парасимпатической нервной системы
3. Функции вегетативной нервной системы
14_
Введение в вегетативную нервную систему
Вегетативная нервная система ( ANS ) является частью центральной нервной системы, которая контролирует висцеральные функции человеческого тела , напр. кровяное давление, перистальтика кишечника, опорожнение мочевого пузыря, регуляция температуры тела и т.д.
Эти регуляции происходят быстро . Например, изменение активности ВНС приведет к удвоению частоты сердечных сокращений или артериального давления в течение нескольких секунд.
Функциональная анатомия ВНС
Центры, контролирующие висцеральные нервы, расположены в спинном мозге, стволе головного мозга и гипоталамусе . Лимбическая система превосходит большую часть этих центров и запускает некоторые висцеральные проявления эмоциональных реакций.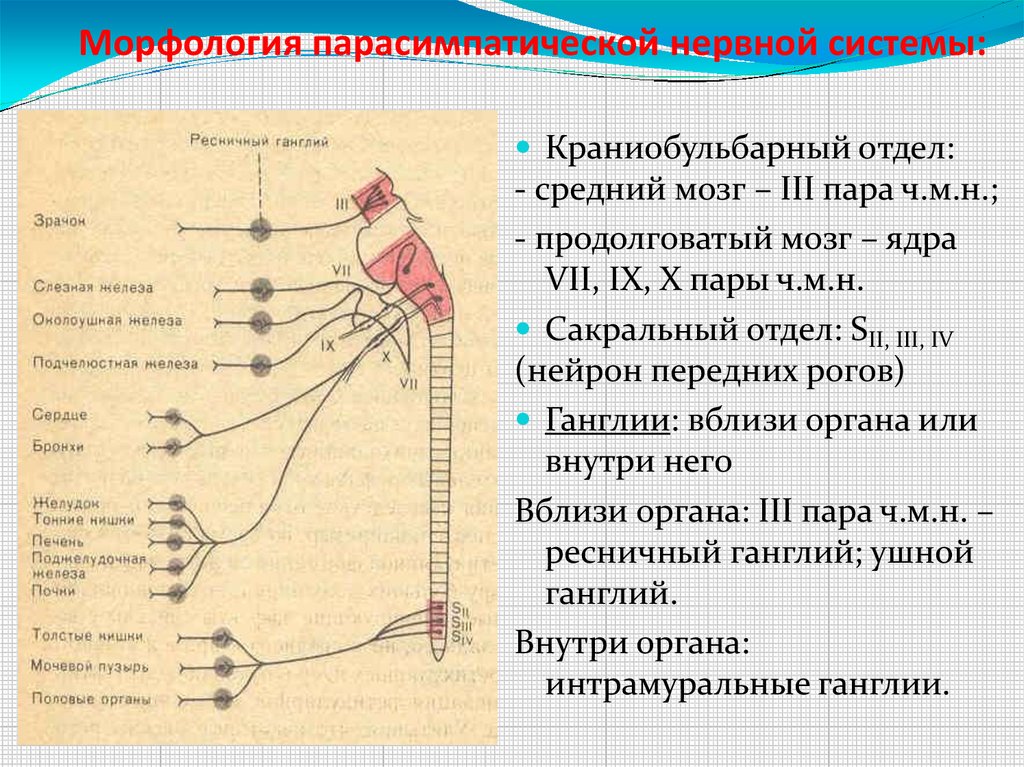 Поэтому у нас может быть «ком в горле» или потные руки при стрессе.
Поэтому у нас может быть «ком в горле» или потные руки при стрессе.
Основная функциональная единица ВНС называется висцеральным рефлексом . Имеет (как двигательный рефлекс) рецептор , центростремительный (афферентный) путь , центр рефлекса , центробежный (эфферентный) путь и эффектор .
Подсознательный сенсорный сигнал, воспринимаемый рецептором в иннервируемом органе, поступает по афферентным волокнам в соответствующий рефлекторный центр в вегетативных ганглиях , стволе головного мозга или гипоталамусе . Здесь информация обрабатывается, и центр посылает ответ через эфферентные нервы эффектору, обычно обратно в иннервируемый орган, где происходит адекватный ответ.
Эфферентные волокна передают сигналы, кодирующие соответствующий ответ, через два основных отдела ВНС: симпатическую и парасимпатическую нервную систему .
Уже в начале следует помнить, что висцеральный рефлекс скорее регулирует относительную активность этих двух отделов. Увеличение симпатической активности чаще всего означает снижение парасимпатической активности и наоборот. Эти системы зависят друг от друга и взаимосвязаны.
Увеличение симпатической активности чаще всего означает снижение парасимпатической активности и наоборот. Эти системы зависят друг от друга и взаимосвязаны.
_
Расположение симпатической и парасимпатической нервной системы
Симпатическая нервная система
Симпатические волокна имеют свои рефлекторные центры в СПИНАЛЬНЫЕ БУДОВ , в SEGMENTS T1 . SYSTERSINTIST SYSTERS SYSTERSTINTINTS SYSTERSTINTINTIST SISTERSTINTINTIST SISTERSTINTICTS
. иногда называют грудопоясничным отделом .Эти первые нейроны берут начало в спинном мозге и через несколько сантиметров перестраиваются в паравертебральные симпатическая цепь ганглиев, от которых отходят эфферентные волокна к тканям и органам. Это также означает, что каждое эфферентное симпатическое волокно состоит из двух нейронов — первого преганглионарного и второго постганглионарного.
Тела преганглионарных нейронов расположены в промежуточно-латеральном столбе спинного мозга и соединяются с соответствующим спинномозговым нервом в переднем столбе. Сразу после выхода из позвоночного канала симпатические волокна проходят через белые соединительные ветви и проникают в симпатические ганглии.
Сразу после выхода из позвоночного канала симпатические волокна проходят через белые соединительные ветви и проникают в симпатические ганглии.
Далее идет один из трех следующих путей:
1) Преганглионарный нейрон здесь соединяется с постганглионарным
2) Аксон преганглионарного нейрона продолжается вверх или вниз к отдаленным ганглиям, в которых он связан
3) Выходит из симпатической цепочки, не соединяясь, и продолжается в периферические симпатические ганглии, , где он окончательно соединяется (редкий вариант)
Как правило, длинных постганглионарных симпатических волокон идут от симпатической цепи к органу-мишени, где они заканчиваются луковичными расширениями, называемыми варикозными расширениями . Это модифицированное окончание аксона высвобождает нейротрансмиттер (в случае симпатической нервной системы норэпинефрин ) в его окружение .
Варикозное расширение вен можно рассматривать как ряд маленьких шариков, нанизанных на нить, каждый аксон имеет относительно большое количество этих окончаний. В отличие от обычных окончаний аксонов, варикозы имеют постсинаптический терминал не назначен . Однако они похожи на обычные синапсы в отношении своего молекулярного оборудования или молекулярно-биологического механизма экзоцитоза. Здесь есть как активная зона с везикулами и митохондриями, так и белки SNARE.
В отличие от обычных окончаний аксонов, варикозы имеют постсинаптический терминал не назначен . Однако они похожи на обычные синапсы в отношении своего молекулярного оборудования или молекулярно-биологического механизма экзоцитоза. Здесь есть как активная зона с везикулами и митохондриями, так и белки SNARE.
Часть постсинаптических нервных волокон выходит из симпатических ганглиев через серые соединительные ветви и присоединяются к иннервации скелетных мышц, с помощью которых волокна выводятся на периферию. Там эти симпатические волокна иннервируют кровеносные сосуды, потовые железы и пилоэректорные мышцы.
Парасимпатическая нервная система
Парасимпатические рефлекторные центры связаны с ядрами черепных нервов III, VII, IX и X и с спинными сегментами S2 и S3 (вариабельно также S1 и S4). Поэтому парасимпатический отдел ВНС иногда называют краниосакральным отделом. Около 75 % парасимпатических волокон приносит блуждающий нерв .
Эфферентные волокна парасимпатических висцеральных рефлексов состоят из двух нейронов. Как и в случае с симпатической нервной системой, мы различаем преганглионарных и постганглионарных нейронов. Однако существенное отличие состоит в том, что преганглионарный нейрон непрерывно продолжается от своего ядра до стенки органа , который иннервирует. Здесь вверху — в интрамуральном ганглии — находится длинный преганглионарный нейрон, соединенный синапсом с коротким постганглионарным нейроном. Постганглионарные волокна, действительно очень короткие, часто имеют длину всего доли миллиметра.
Интересно также само понятие «интрамуральный ганглий». Термин «ганглий» в данном случае вводит в заблуждение, поскольку постганглионарные нейроны часто располагаются довольно далеко друг от друга.0326 диффузно в стенке органа , чем в дискретных ганглиях.
Холинергические и адренергические волокна
Двумя основными нейротрансмиттерами в ВНС являются ацетилхолин и норадреналин . Волокна, высвобождающие ацетилхолин, называются холинергическими, , а волокна, высвобождающие норадреналин, называются адренергическими .
Волокна, высвобождающие ацетилхолин, называются холинергическими, , а волокна, высвобождающие норадреналин, называются адренергическими .
Все преганглионарные волокна являются холинергическими , как в симпатической, так и в парасимпатической части ВНС. Почти все постганглионарные парасимпатические волокна также являются холинергическими. Напротив, большинство постганглионарных симпатических волокон являются адренергическими. Исключение среди симпатических волокон составляют те волокна, которые иннервируют потовые железы и пилоэректорные мышцы – это холинергические.
Подробнее о синтезе и химических свойствах обоих нейротрансмиттеров см. в подразделе 12/4.
_
Функции вегетативной нервной системы
Эффекты ацетилхолина
Возбуждающие эффекты ацетилхолина в ANS опосредованы Рецептором :
1) MUSCARINICARSEPTOR :
1) MUSCARINICARSEPTOR :
1) MUSCARINICARSEPTOR :
1) MUSCARINICAROLS :
6 1).
1) Мускариновые рецепторы
Эти рецепторы связан с G-белком и контролирует ионные каналы . Мускариновые рецепторы можно найти во всех эффекторных клетках, иннервируемых постганглионарными холинергическими волокнами . К настоящему времени было обнаружено пяти типов мускариновых рецепторов – от M 1 до M 5 . Рецепторы M 4 и M 5 еще недостаточно хорошо описаны, поэтому мы опускаем их в последующем тексте.
a) M 1 рецепторы , называемые « нейронными» , находятся в основном в центральной нервной системе . Это тип рецептора, который через белок G q снижает проницаемость мембраны для ионов калия . Это приводит к деполяризации мембраны. Считается, что их дисфункция или уменьшение их плотности является одной из причин деменции.
б) М 2 рецепторы , называемые «сердечный» можно обнаружить на мембранах клеток сердечной мышцы.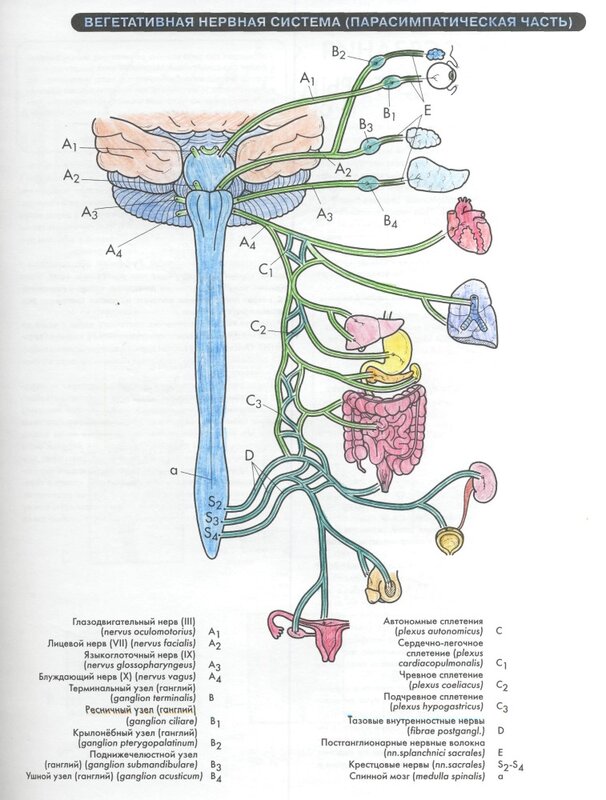 Через G и – белок (что приводит к снижению внутриклеточной концентрации цАМФ) открывают каналы для ионов калия и вызывают гиперполяризацию мембраны. Это механизм, по которому блуждающий нерв снижает частоту сердечных сокращений (уменьшает частоту разрядов кардиостимулятора в СА-узле) и снижает скорость проведения (замедляет проведение от предсердий к желудочкам через АВ-узел).
Через G и – белок (что приводит к снижению внутриклеточной концентрации цАМФ) открывают каналы для ионов калия и вызывают гиперполяризацию мембраны. Это механизм, по которому блуждающий нерв снижает частоту сердечных сокращений (уменьшает частоту разрядов кардиостимулятора в СА-узле) и снижает скорость проведения (замедляет проведение от предсердий к желудочкам через АВ-узел).
c) M 3 рецепторы расположены, в частности, в железах и гладкомышечных клетках и опосредуют парасимпатическую стимуляцию железистой секреции и сокращение гладкой мускулатуры в пищеварительном тракте (и других органах). Эти рецепторы связаны с G q- белком и через фосфолипазу С (катализирующую образование IP 3 и DAG) увеличивают внутриклеточную концентрацию кальция.
2) Никотиновые рецепторы
Никотиновые рецепторы в основном представляют собой лиганд-контролируемые катионные каналы , особенно проницаемые для ионов натрия и калия . Их основная классификация различает мышечный тип ( N M рецептор ), присутствующий в нервно-мышечном соединении, и нейрональный тип ( N N рецептор ), расположенный во всех вегетативных ганглиях . Таким образом, последние рецепторы могут быть обнаружены на мембранах тел и дендритов постганглионарных нейронов, иннервируемых преганглионарных нейронов .
Их основная классификация различает мышечный тип ( N M рецептор ), присутствующий в нервно-мышечном соединении, и нейрональный тип ( N N рецептор ), расположенный во всех вегетативных ганглиях . Таким образом, последние рецепторы могут быть обнаружены на мембранах тел и дендритов постганглионарных нейронов, иннервируемых преганглионарных нейронов .
Эффекты норадреналина
Норадреналин является нейротрансмиттером ВНС, присутствующим только в постсинаптических симпатических волокнах .
Действие норадреналина на конкретную ткань определяется наличием определенного типа рецептора на мембране эффекторных клеток. В настоящее время описано пять основных подтипов адренорецепторов: α 1 , α 2 , β 1 , β 2 , β 3 . Отдельные типы отличаются сродством к своим физиологическим лигандам, адреналину и норадреналину.
Норадреналин связывается с более высоким сродством к α-рецепторам . Его связывание с β-рецепторами не такое сильное, поэтому β-рецепторы менее активируются норэпинефрином. Эпинефрин связывается с обоими типами рецепторов примерно с равной аффинностью . Поэтому реакция ткани определяется наличием определенного типа рецепторов на клеточных мембранах. Если преобладают β-рецепторы в определенной ткани, «гормон» адреналина будет здесь гораздо более мощным, чем симпатическая стимуляция.
Его связывание с β-рецепторами не такое сильное, поэтому β-рецепторы менее активируются норэпинефрином. Эпинефрин связывается с обоими типами рецепторов примерно с равной аффинностью . Поэтому реакция ткани определяется наличием определенного типа рецепторов на клеточных мембранах. Если преобладают β-рецепторы в определенной ткани, «гормон» адреналина будет здесь гораздо более мощным, чем симпатическая стимуляция.
1) α-рецепторы
Опосредованное сужение сосудов, мидриаз и сокращение сфинктеров . Кроме того, α 2 -рецепторы ингибируют дальнейшее высвобождение нейротрансмиттера из варикозных узлов и, таким образом, действуют как ауторецепторы . Эти рецепторы связаны с Gq-белком.
2) β
1 -рецепторы β 1 рецепторы расположены на клетках сердечной мышцы и увеличивают частоту сердечных сокращений . Кроме того, на адипоцитах эти рецепторы способны усиливать липолиз .
3) β
2 -рецепторыЭтот подтип рецепторов проявляет разнообразные эффекты, среди которых преобладают мощные сосудорасширяющие и бронхорасширяющие эффекты. Кроме того, он усиливает калоригенез , т.е. повышает метаболическую активность клеток (тем самым увеличивая потребление кислорода и теплопродукцию).
Обратите внимание, что стимуляция адренергических нервных волокон вызывает вазоконстрикцию ( α 1 -рецептор s), но эндокринная стимуляция адреналином оказывает скорее сосудорасширяющее действие ( β 7 2 Например, в сосудах мышц преобладают β-рецепторы , так при симпатической активации с синхронной активацией мозгового вещества надпочечников происходит вазодилатация . Наоборот, в сосудах желудочно-кишечного тракта преобладают α-рецепторы . Изменения активности отдельных отделов ВНС по-разному действуют на различные системы органов. Иногда можно оценить эти эффекты на основе простого правила: Симпатическая нервная система подготавливает тело к « Бой или бегство ». Парасимпатическая нервная система регулирует функции организма в значении « Отдых и пищеварение ». Повышенный симпатический тонус активирует поперечные волокна радужки и вызывает расширение зрачка – мидриаз . Этот ответ согласуется с предыдущим, потому что во время боя или бегства нам нужно иметь как можно более широкий угол обзора. Наоборот, повышенный парасимпатический тонус сужает круговые волокна радужки, вследствие чего уменьшается диаметр зрачка и возникает миоз . Это происходит при активации парасимпатического рефлекса, реагирующего на воздействие избыточного количества света на сетчатку. Слезные и слюнные железы, а также железы желудочно-кишечного тракта стимулируются парасимпатической нервной системой . Повышение парасимпатического тонуса обычно приводит к повышенному выделению воды или увеличению объема секрета . Ситуация в желудочно-кишечном тракте достаточно сложная, так как парасимпатическая нервная система непосредственно регулирует секрецию желез верхних отделов пищеварительного тракта. С другой стороны, кишечные железы относительно независимы и управляются собственной энтеральной нервной системой . Однако парасимпатическая нервная система, по крайней мере, повышает свою активность. 9. Таким образом, выделяемая жидкость становится более концентрированной. Потовые железы в основном не подвержены прямому влиянию парасимпатической нервной системы. И наоборот, повышенный симпатический тон значительно увеличивает количество выделяемого пота . Таким образом, это единственная железа, которая увеличивает объем своей секреции при симпатических раздражениях. Апокринные железы, вырабатывающие смазочный секрет и уменьшающие трение в подмышечных впадинах, также контролируются симпатической нервной системой, но с обычными адренергическими волокнами . Как правило, симпатическая стимуляция увеличивает сердечный выброс , что сопровождается увеличением сократительной способности миокарда и частоты сердечных сокращений (опосредовано более высокой активностью кардиостимулятора, возбудимостью и скоростью проводимости). Парасимпатическая нервная система позволяет сердцу «отдыхать» в то время, когда не требуется высокий сердечный выброс. Он уменьшает как силу сокращений , так и их частоту . Однако это явление не связано с прямым влиянием парасимпатической нервной системы на клетки сердечной мышцы. Как упоминалось выше, повышение тонуса одного отдела вегетативной нервной системы снижает тонус другого отдела. Симпатическая стимуляция увеличивает как сердечный выброс , так и периферическое сопротивление , поскольку вызывает сужение сосудов в брюшной полости. Вследствие этих факторов происходит острое повышение артериального давления . В долгосрочной перспективе давление не меняется. Парасимпатическая нервная система снижает сердечный выброс, но практически не влияет на кровеносные сосуды. Следовательно, его активация приводит к незначительное падение артериального давления . Физиологически как симпатическая, так и парасимпатическая нервная система остаются постоянно активными . Обе системы непрерывно производят импульсы определенной поддерживающей частоты к исполнительным органам. Отличие заключается в том, что тон АНС основан на низких частотах . Базальная активность симпатической и парасимпатической нервной системы поддерживается одним разрядом в течение нескольких секунд. Полная активация происходит при частоте около десяти разрядов в секунду. В мотонейронах для подобной активности необходимы сотни разрядов в течение одной секунды. Физиологическая полезность этого тона заключается в том, что он позволяет регулируемой функции (или органу) увеличение или уменьшение активности в зависимости от изменения частоты разрядов . Например, симпатическая нервная система в норме поддерживает сужение большинства артериол до половины их максимального диаметра. При повышенном симпатическом тонусе происходит еще более мощное сокращение, например до одной трети максимального диаметра. Наоборот, снижение симпатического тонуса приведет к расширению сосудов. Авторы подглавы: Патрик Маджа и Йозеф Фонтана Вегетативная нервная система (ВНС) регулирует
функции наших внутренних органов (внутренностей), таких как сердце,
желудок и кишечник. ВНС является частью периферической нервной системы.
и он также контролирует некоторые мышцы тела. Мы часто
не знает о ВНС, потому что она функционирует непроизвольно и рефлекторно. За
например, мы не замечаем, когда кровеносные сосуды меняют размер или когда наше сердце
бьется быстрее. Однако некоторых людей можно научить контролировать некоторые
функции ВНС, такие как частота сердечных сокращений или артериальное давление. ВНС наиболее важна в двух ситуациях: ВНС регулирует: — в коже (вокруг волосяных фолликулов; гладкие мышцы ВНС делится на три части: Хороший солнечный день… вы прогуливаетесь в парке.
Внезапно сердитый
появляется медведь
на вашем пути. Вы остаетесь и сражаетесь ИЛИ вы поворачиваетесь и убегаете? Эти
являются ответами «бей или беги». В подобных ситуациях ваш
симпатическая нервная система приводится в действие – она использует энергию – ваше
артериальное давление повышается, сердце бьется быстрее, а пищеварение замедляется
вниз. Обратите внимание на рисунок слева, что симпатическая нервная система
берет начало в спинном мозге. В частности, клеточные тела первых
нейроны (преганглионарные нейроны) располагаются в грудном и поясничном отделах
спинной мозг. Аксоны этих нейронов проецируются в цепочку ганглиев.
расположен рядом со спинным мозгом. В большинстве случаев этот нейрон образует синапс с другим нейроном (постганглионарным
нейрон) в ганглии. Несколько преганглионарных нейронов идут к другим ганглиям
вне симпатической цепи и синапсов нет. постганглионарные
затем нейрон проецируется на «мишень» — мышцу или железу. Еще два факта о симпатической нервной системе: синапс в
симпатический ганглий использует ацетилхолин в качестве нейротрансмиттера; синапс постганглионарного
нейрон с органом-мишенью использует нейротрансмиттер, называемый норадреналин . (Конечно, есть одно исключение:
симпатический постганглионарный нейрон, оканчивающийся на потовых железах
использует ацетилхолин. Хороший солнечный день… вы прогуливаетесь в парке.
Однако на этот раз вы решаете расслабиться в удобном кресле, которое у вас есть.
принес с собой. Это требует ответов «Отдых и переваривание». Сейчас
время для парасимпатической нервной системы для экономии энергии. Это когда
кровяное давление может снизиться, частота пульса может замедлиться, а пищеварение может
Начало. Обратите внимание на изображение слева, что тела клеток
парасимпатическая нервная система расположена в спинном мозге (крестцовый
области) и в мозговое вещество . В продолговатом мозгу черепные нервы III, VII, IX и X образуют
преганглионарные парасимпатические волокна. Преганглионарное волокно из
продолговатый или спинной мозг проецируется на ганглии очень близко к органу-мишени
и образует синапс. Этот синапс использует нейротрансмиттер, называемый ацетилхолин . Вот краткое изложение некоторых эффектов симпатического и
парасимпатическая стимуляция. Обратите внимание, что эффекты обычно находятся в
противостояние друг другу. Вегетативная нервная система Следует отметить, что вегетативная нервная система работает всегда. Кишечная нервная
система является третьим отделом вегетативной нервной системы,
ты многого не слышишь. Энтеральная нервная система представляет собой сеть
нервные волокна, иннервирующие внутренние органы (желудочно-кишечный тракт, поджелудочную железу,
и желчный пузырь). Copyright © 1996-2020, Эрик Х. Чудлер, Университет
Washington Рисунок 3. 3.1 Определение центральной вегетативной сети Поскольку многие студенты были убеждены, что вегетативная нервная система относительно примитивна, большинство из них пришли к выводу, что нормальная регуляция этой системы происходит на ганглиозном или, в лучшем случае, на спинальном уровне. Таким образом, они часто очень удивляются, обнаружив, что дисфункция мозга обычно сопровождается вегетативной дисфункцией, которая может быть опасной для жизни. Например, у больных с перерезкой позвоночника могут возникать тяжелые гипертонические кризы, спровоцированные полным мочевым пузырем, ущемлением толстой кишки или даже поглаживанием кожи. Это не означает, что спинной мозг и вегетативные ганглии не играют важной роли в вегетативной регуляции. Но что организация вегетативной деятельности происходит на супраспинальном уровне. Обширные взаимосвязи возникают между участками, получающими висцеральные входы и контролирующими вегетативные эфферентные выходы, между участками контроля симпатической и парасимпатической нервной системы, а также между участками вегетативного контроля и соматическими, эндокринными и лимбическими цепями. 3.2 Структура центральной вегетативной сети Центральная вегетативная сеть состоит из гипоталамических и экстрагипоталамических ядер. Некоторые из этих участков регулируют симпатический отток, тогда как другие регулируют парасимпатический отток. Эта структура была впервые обнаружена в исследованиях повреждений, которые выявили мультисинаптические связи, нисходящие от гипоталамуса и среднего мозга к преганглионарным нейронам в стволе головного и спинном мозге. Точно так же были продемонстрированы связи от различных лимбических структур мозга, особенно миндалевидного тела, через гипоталамус. Конечным результатом работы этой сети в полном объеме является индукция вегетативных реакций на висцеральные и соматические стрессовые стимулы, такие как повышение частоты сердечных сокращений и артериального давления с началом боли. В качестве альтернативы, хроническая гипертензия у людей типа «А» или у стрессированных лиц представляет собой повышенный центральный автономный отток в ответ на усиление входных сигналов лимбической системы. Существует три типа предавтономных парвоцеллюлярных нейронов (типы A, B и C), которые можно разделить на основе анатомических и физиологических критериев, а также на основе субнуклеарного расположения в PVN. Преавтономные нейроны PVN проецируются непосредственно на преганглионарные вегетативные нейроны в дорсальном моторном ядре блуждающего нерва, вегетативных релейных ядрах ствола головного мозга (A5, ростральные вентральные латеральные продолговатые мозги) и даже непосредственно на промежуточно-латеральные спинные столбы. Эти проекции спускаются ипсилатерально через ствол головного и спинной мозг с четырьмя точками перекреста (надсосковая, мостовая покрышка, комиссуральная часть ядра солитарного тракта (большая), X пластинка спинного мозга), так что в конечном итоге иннервация является двусторонней, но с ипсилатеральным доминированием. Другие ядра гипоталамуса в центральной вегетативной сети включают дорсомедиальное ядро, латеральную область гипоталамуса, заднее ядро гипоталамуса и сосцевидное ядро. Эти ядра посылают и получают проекции от PVN, дорсального двигательного ядра блуждающего нерва, центрального серого вещества, парабрахиального ядра, ядра солитарного тракта, латерального и вентрального продолговатого мозга и промежуточно-латеральных позвоночных столбов. Латеральный гипоталамус особенно вовлечен в сердечно-сосудистый контроль, а также в контроль питания, насыщения и высвобождения инсулина. Рисунок 3.2 3.3 Схема гипоталамического контроля вегетативной нервной системы Гипоталамус связан с остальной частью центральной вегетативной сети тремя основными проводящими путями: дорсальным продольным пучком, медиальным пучком переднего мозга и маммиллотегментальным трактом. Основным путем гипоталамуса в центральной вегетативной сети является дорсальный продольный пучок (DLF). DLF берет начало в области паравентрикулярного ядра и спускается по самой медиальной части третьего желудочка через периакведуктальную серую и мезэнцефальную ретикулярную формацию. DLF продолжается каудально по средней линии около дна четвертого желудочка до закрытия открытого мозгового вещества, где он становится интернализованным около остатка центрального канала. Это положение оставляет DLF в идеальном положении для иннервации периакведуктального серого, парабрахиального ядра, мезэнцефального ядра шва и голубого пятна рострально и дорсального двигательного ядра блуждающего нерва, ядра двойственного и медуллярного шва более каудально. Медиальный пучок переднего мозга (MFB) является основным путем входа в гипоталамус из ядер перегородок и базальных лимбических структур переднего мозга. Входы от миндалевидного тела и гиппокампа, хотя сначала достигают гипоталамуса через терминальную полоску, вентральный миндалевидный путь и свод, в конечном итоге соединяются с MFB и, таким образом, получают доступ к паравентрикулярному ядру. MFB также имеет волокна от паравентрикулярного ядра, которые опускаются, чтобы иннервировать практически те же ядра, что и DLF. Маммиллотегментальный путь менее выражен, чем DLF или MFB, тем не менее, этот путь, который берет начало в сосцевидном ядре, посылает проекции в мезэнцефальные и мостовые ретикулярные формации, которые, в свою очередь, влияют на активность вегетативных ядер ствола мозга, перечисленных выше. Соматические афференты восходят к гипоталамусу через спино-гипоталамический тракт. Рисунок 3.3 3.4 Нарушения центрального вегетативного контроля 3. Как отмечалось выше, центральная вегетативная сеть состоит из трех иерархически упорядоченных цепей или петель: кратковременной стволово-спинномозговой петли и лимбической мозг-гипоталамус-стволовой мозг-спинномозговой петли спинного мозга, опосредующие предвосхищающие и стрессовые реакции, и петли промежуточной длины гипоталамо-стволовой мозг-спинной мозг, опосредующие более длительные вегетативные рефлексы. Здесь мы сосредоточимся на этой более поздней петле в ее роли в терморегуляции. Следующая глава будет посвящена этой петле в регуляции питания. Гипоталамическая основа заданной температуры. Регулирование внутренней температуры имеет важное значение, поскольку большинство метаболических процессов, необходимых для жизни, сильно зависят от температуры. Нормальная заданная температура тела в первую очередь определяется активностью нейронов в медиальных преоптических и передних ядрах гипоталамуса, а также нейронами в прилегающих медиальных ядрах перегородки. 3.6 Нейроны, чувствительные к температуре Ранее упоминалось, что гипоталамус является одной из немногих областей мозга, где находятся нейроны ЦНС, непосредственно чувствительные к физическим или химическим переменным, таким как температура, осмоляльность плазмы, глюкоза плазмы и различные гормоны. . POAH имеет три типа нейронов, участвующих в определении заданного значения температуры: чувствительные к теплу нейроны, чувствительные к холоду нейроны и нечувствительные к температуре нейроны, которые определяются изменениями скорости разряда после локального нагревания или охлаждения POAH. Теплочувствительные нейроны составляют около 30% пула нейронов ПОАГ. Скорость возбуждения этих нейронов зависит от температуры, как показано на рис. 3.4. Изменение температуры ниже 37 градусов мало влияет на скорость разряда. Рис. 3.4 3.7 Нейронные механизмы установки температуры Основной схемой регулирования температуры тела является отвод тепла. Теплочувствительные нейроны ПОАГ имеют собственные мембранные рецепторы, чувствительные к изменениям температуры мозга и крови выше 37 градусов. Это неспецифические катионные каналы, которые, скорее всего, связаны с ваниллоидным (чувствительным к капсаицину) семейством терморецепторов. Рисунок 3.5 Лихорадка. «У человечества есть только три великих врага: лихорадка, голод и война,
и из них, безусловно, самая страшная и самая ужасная — лихорадка». Рисунок 3.6 Тепловой удар. Если тепловое истощение не лечить, оно может прогрессировать до теплового удара. Экстремальная гипотензия приводит к падению кожного кровотока и уменьшению потоотделения. Температура ядра впоследствии будет повышаться. Если это повышение слишком сильное, нормальное функционирование мозга может быть прервано, и контроль заданного значения температуры не удастся. Это приводит к дальнейшему ухудшению механизмов рассеивания тепла и дальнейшему повышению внутренней температуры, что приводит к повреждению тканей, что может привести к коме, а затем к смерти. Этот пациент с тепловым ударом находится в неотложной медицинской помощи и нуждается в срочном снижении внутренней температуры путем восполнения жидкости и электролитов. Повреждение печени часто встречается при этом состоянии, и желтуха может развиться через 1–2 дня после госпитализации. Злокачественная гипертермия представляет собой группу наследственных заболеваний, характеризующихся внезапным и экстремальным повышением внутренней температуры после воздействия газообразных анестетиков, включая галотан, метоксифлуран, циклопропан или этиловый эфир; или после воздействия миорелаксантов, особенно сукцинилхолина. Эти агенты провоцируют чрезмерное высвобождение кальция из мышечного саркоплазматического ретикулума, что приводит к активации миозиновой АТФазы и, таким образом, к избыточному выделению тепла. Одна форма заболевания наследуется по аутосомно-доминантному типу, вторая – по рецессивному у мальчиков и реже у девочек, имеющих также ряд других врожденных аномалий, составляющих синдром Кинга. Злокачественная гипертермия также иногда возникает при других миопатиях, таких как врожденная миотония и мышечная дистрофия Дюшенна. Рисунок 3. Гипотермия определяется как внутренняя температура 35 градусов или ниже и представляет потенциальную неотложную медицинскую помощь. Случайная гипотермия распространена зимой после длительного воздействия, не обязательно чрезмерно низких температур, и может сопровождать сепсис, гипотиреоз, гипофизарную или надпочечниковую недостаточность, гипогликемию, инфаркт миокарда и прием лекарств, особенно алкоголя. Однако гипотермия также может возникать при определенных медицинских состояниях без воздействия, включая застойную сердечную недостаточность, уремию, передозировку лекарств, острую дыхательную недостаточность и гипогликемию. Большинство этих пациентов пожилого возраста. Пациенты с центральной температурой менее 26,7 градусов обычно находятся в бессознательном состоянии, миотичны, имеют брадипноэ, брадикардию и гипотонию с генерализованными отеками. При температуре тела ниже 25°С больные впадают в кому, арефлексичны и могут появиться трупные окоченения. 3.9 Резюме Несколько структур переднего мозга, диэнцефалии и ствола головного мозга связаны между собой для организации выхода вегетативной нервной системы. В совокупности это называется центральной автономной сетью и далее организовано в иерархию функциональных петель. Гипоталамус является ключевым участком головного мозга для центрального контроля вегетативной нервной системы, а паравентрикулярное ядро является ключевым участком гипоталамуса для этого контроля. Основной путь от гипоталамуса для вегетативного контроля — дорсальный продольный пучок. Регуляция температуры тела является одним из примеров гипоталамического контроля вегетативных ядер ствола мозга и спинного мозга, связанного с долгосрочными вегетативными рефлексами. Лихорадка является наиболее распространенным нарушением терморегуляции. Лихорадка следует за высвобождением эндогенных пирогенов, которые повышают уровень простагландина Е2 в преоптическом переднем гипоталамусе, что вызывает снижение активности теплочувствительных нейронов и последующее растормаживание холодочувствительных нейронов. Проверьте свои знания Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: А. перивентрикулярное ядро B. паравентрикулярное ядро С. D. заднее ядро Е. вентромедиальное ядро Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: A. перивентрикулярное ядро Это НЕВЕРНЫЙ ответ. B. паравентрикулярное ядро C. переднее ядро D. заднее ядро Е. вентромедиальное ядро Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: А. перивентрикулярное ядро B. паравентрикулярное ядро Это ПРАВИЛЬНЫЙ ответ! С. переднее ядро D. заднее ядро Е. вентромедиальное ядро Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: А. B. паравентрикулярное ядро C. переднее ядро Это НЕВЕРНЫЙ ответ. D. заднее ядро E. вентромедиальное ядро Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: А. перивентрикулярное ядро B. паравентрикулярное ядро С. переднее ядро D. заднее ядро Это НЕВЕРНЫЙ ответ. Е. вентромедиальное ядро Наиболее важным ядром гипоталамуса для центральной регуляции вегетативной нервной системы является: А. перивентрикулярное ядро B. паравентрикулярное ядро С. переднее ядро D. Вентромедиальное ядро E. Этот ответ НЕВЕРЕН. В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? А. вентромедиальное ядро B. дорсомедиальное ядро С. дугообразное ядро D. паравентрикулярное ядро E. преоптическое переднее ядро В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? A. B. дорсомедиальное ядро С. дугообразное ядро D. паравентрикулярное ядро E. преоптическое переднее ядро В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? А. вентромедиальное ядро B. дорсомедиальное ядро Это НЕВЕРНЫЙ ответ. С. дугообразное ядро D. паравентрикулярное ядро E. преоптическое переднее ядро В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? А. вентромедиальное ядро B. дорсомедиальное ядро C. D. паравентрикулярное ядро E. преоптическое переднее ядро В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? А. вентромедиальное ядро B. дорсомедиальное ядро С. дугообразное ядро D. паравентрикулярное ядро Это НЕВЕРНЫЙ ответ. E. преоптическое переднее ядро В каком из следующих ядер гипоталамуса заданное значение температуры тела кодируется термочувствительными нейронами? А. вентромедиальное ядро B. дорсомедиальное ядро С. дугообразное ядро D. паравентрикулярное ядро E. Какое ядро гипоталамуса считается центром выработки/сохранения тепла? A. преоптическое переднее ядро B. паравентрикулярное ядро C. заднее ядро D. супраоптическое ядро Е. дугообразное ядро Какое ядро гипоталамуса считается центром выработки/сохранения тепла? A. преоптическое переднее ядро Этот ответ НЕВЕРЕН. B. паравентрикулярное ядро C. D. супраоптическое ядро Е. дугообразное ядро Какое ядро гипоталамуса считается центром выработки/сохранения тепла? А. преоптическое переднее ядро B. паравентрикулярное ядро Это НЕВЕРНЫЙ ответ. C. заднее ядро D. супраоптическое ядро Е. дугообразное ядро Какое ядро гипоталамуса считается центром выработки/сохранения тепла? А. преоптическое переднее ядро B. паравентрикулярное ядро C. заднее ядро Это ПРАВИЛЬНЫЙ ответ! D. супраоптическое ядро Е. дугообразное ядро Какое ядро гипоталамуса считается центром выработки/сохранения тепла? А. B. паравентрикулярное ядро C. заднее ядро D. супраоптическое ядро Это НЕВЕРНЫЙ ответ. Е. дугообразное ядро Какое ядро гипоталамуса считается центром выработки/сохранения тепла? А. преоптическое переднее ядро B. паравентрикулярное ядро C. заднее ядро D. супраоптическое ядро E. дугообразное ядро. Это НЕВЕРНЫЙ ответ. Основным путем центральной вегетативной сети является: А. B. терминальная полоска C. задний продольный пучок D. маммиллотегментальный тракт E. спино-гипоталамический тракт Основным путем центральной вегетативной сети является: A. медиальный пучок переднего мозга Это НЕВЕРНЫЙ ответ. B. терминальная полоска C. задний продольный пучок D. маммиллотегментальный тракт E. спино-гипоталамический тракт Основным путем центральной вегетативной сети является: А. медиальный пучок переднего мозга B. терминальная полоска Этот ответ НЕВЕРЕН. C. задний продольный пучок D. сосочно-тегментальный тракт E. Основным путем центральной вегетативной сети является: А. медиальный пучок переднего мозга B. терминальная полоска C. задний продольный пучок Это ПРАВИЛЬНЫЙ ответ! D. маммиллотегментальный тракт E. спино-гипоталамический тракт Основным путем центральной вегетативной сети является: А. медиальный пучок переднего мозга B. терминальная полоска C. задний продольный пучок D. сосочно-тегментальный тракт Этот ответ НЕВЕРЕН. E. спино-гипоталамический тракт Основным путем центральной вегетативной сети является: А. медиальный пучок переднего мозга B. C. задний продольный пучок D. маммиллотегментальный тракт E. спино-гипоталамический тракт Этот ответ НЕВЕРЕН. 0009 Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны organum vasculosum ингибируют теплочувствительные нейроны и стимулируют холодочувствительные нейроны E. Пирогены сужают кровеносные сосуды Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла. Этот ответ НЕВЕРНЫЙ. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны organum vasculosum ингибируют теплочувствительные нейроны и стимулируют холодочувствительные нейроны E. Пирогены сужают кровеносные сосуды Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. Этот ответ НЕВЕРНЫЙ. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны organum vasculosum ингибируют теплочувствительные нейроны и стимулируют холодочувствительные нейроны E. Пирогены сужают кровеносные сосуды Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны organum vasculosum ингибируют теплочувствительные нейроны и стимулируют холодочувствительные нейроны E. Пирогены сужают кровеносные сосуды Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны сосудистого органа подавляют теплочувствительные нейроны и стимулируют холодочувствительные нейроны. Этот ответ НЕВЕРЕН. E. Пирогены сужают кровеносные сосуды Какое из следующих явлений лучше всего объясняет возникновение лихорадки? A. B. Теплочувствительные нейроны возбуждаются простагландином Е2 и увеличивают приток тепла. C. Нечувствительные к температуре нейроны повышают активность расторможенных чувствительных к холоду нейронов. D. Нейроны organum vasculosum ингибируют теплочувствительные нейроны и стимулируют холодочувствительные нейроны E. Пирогены сужают кровеносные сосуды. Это НЕВЕРНЫЙ ответ. Сердечно-сосудистая диабетология том 20 , Номер статьи: 170 (2021)
Процитировать эту статью 8240 доступов 11 Цитаты Сведения о показателях Заболеваемость и распространенность артериальной гипертензии растет во всем мире, и в настоящее время этим заболеванием страдает около 1,13 миллиарда человек, часто в сочетании с другими заболеваниями, такими как сахарный диабет, хроническое заболевание почек, дислипидемия/гиперхолестеринемия и ожирение. Артериальная гипертензия является одной из основных причин преждевременной смерти во всем мире: гипертонией страдают 1,13 миллиарда человек. Это связано с повышенным риском сердечно-сосудистых заболеваний (ССЗ, например, инсульта, стенокардии, инфаркта миокарда, сердечной недостаточности, заболевания периферических артерий и аневризмы брюшной аорты), а также терминальной стадии почечной недостаточности [1, 2]. Вегетативная нервная система вовлечена в патофизиологию гипертензии [7, 8], и были разработаны методы лечения, нацеленные на симпатическую нервную систему (СНС) [9, 10], хотя в значительной степени забытые или исключенные в международных рекомендациях [1, 2 ]. Таким образом, целью данного обзора является изучение патофизиологии артериальной гипертензии, в частности роли вегетативной нервной системы (ВНС) и лекарственных средств, воздействующих на СНС для контроля артериальной гипертензии. Согласно рекомендациям ESC/ESH, артериальная гипертензия определяется как офисные значения системного артериального давления ≥ 140 мм рт.ст. и/или значения диастолического артериального давления ≥ 90 мм рт.ст. [2]. Этиология артериальной гипертензии в настоящее время до сих пор плохо изучена, хотя было выявлено несколько факторов риска ее развития, таких как избыточный вес, диета (например, потребление натрия), физическая активность и употребление алкоголя [11, 12]. Его патогенез многофакторный и очень сложный, с участием многих систем органов и многочисленных независимых и взаимозависимых путей [13]. Известные системы, участвующие в контроле артериального давления, включают сердечно-сосудистую, почечную, нервную и эндокринную системы, а также местные ткани, при этом почки играют центральную роль [13]. В то время как исследования на животных продемонстрировали обширные и взаимные взаимодействия между СНС и РААС, важные для сердечно-сосудистой регуляции и развития гипертонии, подтверждающие доказательства у людей в настоящее время отсутствуют [17, 18]. Поддержание сердечно-сосудистого гомеостаза требует постоянного перенаправления кровотока для обеспечения адекватного кровоснабжения активных тканей. Контроль артериального давления симпатической нервной системой (СНС) и ренин-ангиотензин-альдостероновой системой (РААС) Увеличенное изображение СНС играет важную роль в регуляции метаболических процессов в печени, при этом симпатическая и парасимпатическая системы, работающие в тандеме, чтобы соответственно стимулировать и подавлять глюконеогенез в печени, и инсулин, стимулирующий гликолиз и липогенез, и подавляющий глюконеогенез [21]. Последствия симпатической перегрузки, приводящие к гипертензии, многочисленны и включают сердечно-сосудистые, почечные и метаболические эффекты (рис. 2) [25,26,27]. Состояние симпатической активации связано с учащением сердечных сокращений и, по-видимому, способствует сердечным и сосудистым изменениям [25, 28], способствуя развитию серьезных осложнений гипертонии, таких как аритмия, гипертрофия левого желудочка и усиление жесткости артерий [25, 26]. Роль симпатической нервной системы (СНС) в энергетическом балансе и регуляции метаболизма, а также в контроле артериального давления у пациентов с избыточным весом. FFA Свободные жирные кислоты, OSA синдром обструктивного апноэ сна, RAAS ренин-ангиотензин-альдостерон. Красные кресты обозначают нарушение Увеличить Симпатическая активность повышена при гипертонии и сердечной недостаточности и ответственна за возникновение и развитие заболеваний [7, 8, 31]. В то время как конкретные причины этого увеличения в основном неизвестны, генетические влияния, поведенческие факторы и факторы образа жизни, по-видимому, связаны [7, 8]. Считается, что повышенная активность СНС способствует патофизиологии сердечной недостаточности посредством множества механизмов, включая десенсибилизацию кардиальных β-адренорецепторов, неблагоприятное воздействие на сопряжение возбуждения и сокращения и фиброз [16, 32]. Эффекты активации СНС опосредованы адренергическими нейротрансмиттерами (норэпинефрином, адреналином и дофамином), обладающими вазоконстрикторными свойствами [18]. Было показано, что выброс норадреналина увеличивается у пациентов с высоким кровяным давлением, и это увеличение в основном наблюдается в сердце и почках, которые активно участвуют в контроле артериального давления [18]. Высвобождение этих адренергических нейротрансмиттеров индуцирует действие на сердечно-сосудистую и метаболическую системы, воздействуя на органы, участвующие в контроле гомеостаза, такие как сердце, почки, вены и артериолы, что приводит к высвобождению ренина, задержке натрия, увеличению частоты сердечных сокращений, аритмии и левожелудочковой недостаточности. гипертрофия. Таким образом, эти мишени СНС способствуют повышению артериального давления. Что касается метаболических эффектов, то адренергические нейротрансмиттеры отвечают за действие на различные органы и ткани: на жировые клетки за усиление липолиза, что приводит к увеличению высвобождения жирных кислот, на печень за усиление глюконеогенеза, на β-клетки поджелудочной железы за снижение секреции инсулина. В отличие от повышенной симпатической активности, парасимпатическая активность снижена у пациентов с артериальной гипертензией, что свидетельствует о симпатическом/парасимпатическом дисбалансе [39,40,41]. Более высокая распространенность артериальной гипертензии обнаруживается у больных диабетом с нарушением парасимпатического контроля. Более того, существует связь между этим дефектом и профилем артериальной гипертензии и сосудистыми осложнениями [42]. Помимо гипертензии, аномальная активация СНС связана с метаболическим синдромом, известным фактором риска гипертонии [4, 43]. Гипертония часто встречается у лиц с ожирением. Подсчитано, что около 75% случаев артериальной гипертензии напрямую связаны с наличием ожирения (определяется индексом массы тела ≥ 30 кг/м 2 ). Нарушение активности СНС приводит к увеличению веса. Действительно, СНС играет решающую роль в контроле расхода энергии в ответ на определенные физиологические стимулы (например, изменение энергетического состояния, прием пищи, потребление углеводов, гиперинсулинемия и воздействие холода) посредством регуляции скорости метаболизма в состоянии покоя и инициирования термогенеза действием. на бурую жировую ткань [43, 44]. Однако ожирение связано с перегрузкой СНС, которая рассматривается как компенсаторный механизм увеличения расхода энергии, позволяющий восстановить энергетический баланс [45]. Однако некоторые данные свидетельствуют о том, что симпатическая реакция на различные стимулы может быть притуплена у пациентов с ожирением по сравнению с худыми людьми. Например, сообщалось, что симпатическая активность у пациентов с ожирением менее стимулируется после приема пищи, богатой углеводами, или перорального приема глюкозы, несмотря на более высокий инсулиновый ответ [49, 50, 51], и они демонстрируют более низкий гемодинамический ответ во время изометрических или гетерометрических упражнений [49, 50, 51]. Повышение уровня норадреналина и метаболитов в моче, а также повышенный выброс норадреналина в плазму были продемонстрированы у взрослых с ожирением по сравнению с худощавыми [56, 57]. Кроме того, у взрослых с ожирением наблюдается повышенная активность симпатического нерва в состоянии покоя в скелетных мышцах [58, 59, 60]. Ожирение также связано с повышенной активностью СНС в различных тканях, в частности в почках, что приводит к усилению вазоконстрикции и задержке жидкости, а также к активации ренин-ангиотензин-альдостероновой системы, способствуя повышению артериального давления [55]. ОГТ часто ассоциируется с сахарным диабетом, метаболическим синдромом и дислипидемией. В дополнение к симпатическим изменениям более чем у трети пациентов с метаболически здоровым ожирением может быть обнаружен дефект блуждающего нерва [66], что позволяет предположить, что ваго-симпатический дисбаланс является ранним нарушением при ожирении, которое может играть роль в последующей гипертензии. СНС также участвует в контроле частоты сердечных сокращений с помощью глюкагоноподобного пептида 1 (ГПП-1), инкретинового гормона, высвобождаемого кишечником в ответ на прием пищи, который имеет рецепторы в периферических тканях и центральной нервной системе [47, 68, 69]. Известно, что ГПП-1 оказывает благотворное влияние на метаболические параметры у пациентов с сахарным диабетом 2 типа, такие как увеличение высвобождения инсулина, пополнение запасов инсулина, пролиферация β-клеток поджелудочной железы, улучшение чувствительности к инсулину в скелетных мышцах, ингибирование секреции глюкагона, снижение глюконеогенеза в печени, снижение опорожнения желудка, усиление термогенеза, снижение аппетита и массы тела [70, 71]. Было высказано предположение, что активация вегетативной системы, вызванная барорефлекторной дисфункцией, предрасполагает к гипертонии у людей с апноэ во сне, при этом более выраженное нарушение чувствительности барорецепторного рефлекса в значительной степени связано с повышением артериального давления и артериальной гипертензией у в целом здоровых пожилых людей с апноэ во сне [78]. Повышенная симпатическая активность наблюдается у пациентов с апноэ во сне, даже когда они бодрствуют, а эпизоды апноэ связаны с дальнейшим повышением активности симпатических нервов и артериального давления во время сна [80]. Было показано, что увеличение активности СНС также ответственно за увеличение инсулинорезистентности и центрального ожирения, которые связаны с более высокими показателями апноэ во сне [81]. У пациентов с ожирением, резистентной артериальной гипертензией и апноэ во сне снижение симпатического перенапряжения приводит к значительной потере веса и снижению артериального давления [81]. Для измерения гиперактивности СНС доступно несколько методов, в том числе регистрация симпатического нерва, радиофармпрепараты для измерения регионарной активности симпатических нейронов или частоты сердечных сокращений и вариабельности артериального давления. Микронейрография заключается в измерении активности симпатического нерва в коже или скелетных мышцах (MSNA) [83]. Известно, что симпатические оттоки происходят вспышками, поэтому измерение симпатической активности основано на обнаружении этих вспышек. Микронейрография является инвазивным методом, для выполнения которого требуется опытный специалист [84]. Анализ можно проводить тремя способами: измерение частоты вспышек (количество вспышек в минуту), измерение частоты вспышек (количество вспышек на 100 сердечных сокращений) или измерение общей нервной активности ( сумма амплитуд вспышек за 1 мин) [31, 84, 85]. Поскольку сердце и почки недоступны для микронейрографии, были разработаны измерения, полученные с помощью радиоактивных индикаторов. Этот метод основан на измерении оттока норадреналина в кровоток. Тритиевый I-норэпинефрин вводят в кровоток пациента, что позволяет измерить органоспецифический выброс норадреналина в плазму путем изотопного разведения [86, 87]. 123I-метайодбензилгуанидин (123I-MIBG) является аналогом норадреналина, который можно использовать для неинвазивной оценки активности симпатических нейронов сердца [88, 89].]. Активность СНС можно также измерить косвенными методами, такими как вариабельность сердечного ритма, вариабельность артериального давления или чувствительность артериального барорефлекса. Вариабельность сердечного ритма (ВСР) представляет собой изменение во времени частоты сердечных сокращений вокруг среднего значения пациента между двумя сердечными сокращениями. Его можно измерить с помощью нескольких минут или 24-часовых записей ЭКГ, которые могут точно определять интервалы RR, и рассчитать с использованием нескольких индексов: индексов временной области, частотных индексов или нелинейных индексов [90]. ВСР также используется для оценки сердечного тонуса блуждающего нерва [89, 91]. Вариабельность артериального давления классифицируется как краткосрочная, среднесрочная и долгосрочная вариабельность и увеличивается в зависимости от состояния в зависимости от симпатической активности. Среднесрочную и долгосрочную вариабельность можно измерить с помощью амбулаторного мониторинга АД [9].2], а кратковременную вариабельность можно измерить с помощью спектрального анализа артериального давления, измеренного с помощью пальцевых плетизмографов [93]. Чувствительность барорефлекса определяет способность СНС реагировать на изменения артериального давления, воспринимаемые на уровне каротидного синуса и дуги аорты [94]. Его можно измерить с помощью шейной камеры (стимуляция каротидного барорефлекса), использования вазоактивных препаратов (определение изменений системного давления) и пробы Вальсальвы (для обнаружения брадикардических реакций). Чтобы определить чувствительность барорефлекса, врачи должны проанализировать связь между диастолическим артериальным давлением и MSNA [9].5, 96]. Камеры шеи измеряют чувствительность барорефлекса к растяжению и сжатию барорецепторов посредством отрицательного и положительного давления, приложенного к передней части шеи [97]. Инъекция вазоактивного препарата (ангиотензин или фенилэфрин) позволяет регистрировать ЭКГ и артериальное давление от удара к удару [98]. В многочисленных исследованиях проанализирована взаимная корреляция между вариабельностью ЧСС и АД, которая может объяснять изменения вегетативной нервной деятельности [99, 100]. Рекомендации по лечению артериальной гипертензии включают изменение образа жизни (например, диету, снижение массы тела, физические упражнения) либо отдельно, либо в сочетании с фармакотерапией [1]. Ожидается, что снижение симпатического перенапряжения вызовет ряд благоприятных сердечно-сосудистых и метаболических последствий [28], как показано в некоторых из этих стратегий лечения гипертензии. Изменение образа жизни является первой линией лечения гипертонии [1]. Хотя физические упражнения снижают артериальное давление и защищают от сердечно-сосудистых заболеваний, они, по-видимому, не влияют на артериальное давление, уровень липидов или риск развития диабета [39].]. Специализированный план питания с высоким содержанием белка, диетический подход к остановке гипертонии (DASH), с упором на фрукты и овощи, нежирные молочные продукты, цельнозерновые злаки, овощи и орехи, нежирное мясо, птицу и рыбу, снижает кровяное давление и уровень липидов, а также улучшают метаболические маркеры при использовании в рамках программы по снижению веса [38]. В исследовании CALERIE (Комплексная оценка долгосрочных эффектов снижения потребления энергии) [62] пациенты были разделены на три группы: ограничение калорий (снижение потребления энергии на 25 %), ограничение калорий и физические упражнения (снижение 12,5% связаны с увеличением расхода энергии на 12,5%) или низкокалорийной диетой до снижения веса на 15% с последующим поддержанием веса. Через 6 месяцев исследования во всех группах активность СНС снизилась, тогда как ПНС увеличилась, но изменения достигли значимости только во второй группе. Таким образом, результаты показывают, что потеря веса является важным фактором для улучшения баланса СНС/ПНС, особенно когда ограничение калорий сочетается с физическими упражнениями. Катетерная почечная денервация изучалась как метод лечения резистентной к лекарствам гипертензии [103, 104]. Почечная денервация снижала артериальное давление и снижала сердечно-сосудистые заболевания [105–106]. Помимо влияния на артериальное давление, почечная денервация продемонстрировала снижение активности мышечных симпатических нервов с уменьшением эффектов, опосредованных СНС, таких как улучшение гликемического контроля и резистентности к инсулину, а также снижение общего периферического сопротивления [103, 104, 107]. Наблюдаемые положительные эффекты почечной денервации на сердечно-сосудистую систему включают снижение жесткости артерий (снижение скорости пульсовой волны), уменьшение массы левого желудочка, улучшение симптомов сердечной недостаточности и диастолической функции, а также увеличение фракции выброса левого желудочка [103, 107]. Частота сердечных сокращений также значительно снижается за счет почечной денервации [108]. Можно использовать несколько фармакологических стратегий для снижения артериального давления, направленных на РААС (ингибиторы ангиотензинпревращающего фермента (АПФ)/блокаторы рецепторов ангиотензина (БРА)), сердечный выброс (β-блокаторы), периферическое сосудистое сопротивление ( блокаторы кальциевых каналов (БКК) или реабсорбцию натрия (диуретики) 9.0009 Фармакологическая терапия для лечения гипертензии путем ингибирования СНС включает бета-блокаторы и агонисты имидазолиновых рецепторов, нацеленные на бета-адренергические и имидазолиновые I 1 рецепторы соответственно [9, 10]. Бета-блокаторы, также показанные для лечения сердечной недостаточности [79, 112], уменьшают активацию СНС, противодействуя бета-адренергическим рецепторам [10], и потенциально оказывают благотворное влияние на сердечный фиброз. Хотя они снижают активацию СНС и сердечно-сосудистые исходы у пациентов с сердечной недостаточностью и сниженной фракцией выброса ЛЖ, они также оказывают нежелательные негативные метаболические эффекты, включая резистентность к инсулину, дислипидемию и снижение гликемического контроля [10, 31, 113]. Они также увеличивают прибавку в весе [2, 48]. Агонисты имидазолиновых рецепторов (например, клонидин, моксонидин, рилменидин) действуют на имидазолиновые I 1 рецепторы [9]. Имидазолиновые рецепторы I 1 , сконцентрированные в ростральном вентролатеральном мозговом веществе (RVLM), части ствола мозга, участвующей в симпатическом контроле артериального давления, важны для регуляции симпатического возбуждения [114, 115]. Mechanisms of action of imidazoline receptor agonists Full size image Metabolic and cardiovascular effects of selective imidazoline receptor agonists moxonidine and rilmenidine Full size image Hypertension is многофакторный патологический процесс, который является общепризнанным фактором сердечно-сосудистого риска. Гиперактивация СНС играет центральную роль в этиологии АГ, а также связана с несколькими сопутствующими заболеваниями, обычно связанными с АГ, такими как метаболический синдром, сахарный диабет, дислипидемия или синдром апноэ во сне. Некоторые методы лечения гипертонии, особенно селективные агонисты имидазолиновых рецепторов, нацелены на СНС и продемонстрировали благотворное влияние на сердечно-сосудистую систему, почки и метаболизм в дополнение к снижению артериального давления. Неприменимо. Симпатическая нервная система Сердечно-сосудистые заболевания Вегетативная нервная система Ренин-ангиотензин-альдостероновая система Парасимпатическая нервная система Глюкагоноподобный пептид 1 Активность симпатического нерва мышц Диетический подход к остановке гипертонии Комплексная оценка долгосрочных последствий снижения потребления энергии Ингибиторы ангиотензинпревращающего фермента Блокаторы ангиотензиновых рецепторов Блокаторы кальциевых каналов Ростральная вентролатеральная часть продолговатого мозга Селективные агонисты имидазолиновых рецепторов Whelton PK, Carey RM, Aronow WS, Casey DE, Collins KJ, Dennison Himmelfarb C, et al. Руководство ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA 2017 г. по профилактике, выявлению, оценке и лечению высокого кровяного давления у взрослых: краткое изложение: отчет Американского колледжа Кардиология/Специальная рабочая группа Американской кардиологической ассоциации по клиническим рекомендациям. Тираж. 2018; 138:e426–83. ПабМед
Google ученый Уильямс Б., Мансия Г., Спиринг В., Агабити Розеи Э., Азизи М., Бернье М. и др. Руководство ESC/ESH 2018 г. по лечению артериальной гипертензии. Европейское сердце J. 2018; 39: 3021–104. ПабМед
Статья
Google ученый Coats AJS, Cruickshank JM. Гипертоники с диабетом 2 типа, симпатическая нервная система и последствия лечения. Int J Кардиол. 2014; 174:702–9. ПабМед
Статья
Google ученый Демарко В.Г., Ароор А.Р., Сауэрс Младший. Патофизиология артериальной гипертензии у больных с ожирением. Нат Рев Эндокринол. 2014;10:364–76. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Миллс К.Т., Банди Дж.Д., Келли Т.Н., Рид Дж.Е., Кирни П.М., Рейнольдс К. и др. Глобальные различия в распространенности и контроле артериальной гипертензии: систематический анализ популяционных исследований в 90 странах. Тираж. 2016; 134:441–50. ПабМед
ПабМед Центральный
Статья
Google ученый Сотрудничество по факторам риска НИЗ (NCD-RisC). Мировые тенденции артериального давления с 1975 по 2015 год: объединенный анализ 1479 популяционных исследований с 19,1 млн участников. Ланцет Лонд англ. 2017; 389:37–55. Артикул
Google ученый Эслер М. Симпатическая система и гипертония. Ам Дж Гипертенс. 2000;13:99С-105С. КАС
пабмед
Статья
Google ученый Mancia G, Grassi G. Вегетативная нервная система и гипертония. Цирк рез. 2014; 114:1804–14. КАС
пабмед
Статья
Google ученый Sica DA. Антигипертензивные средства центрального действия: обновление. J Clin Hypertens Greenwich Conn. 2007; 9:399–405. КАС
Статья
Google ученый Фонсека В.А. Влияние бета-блокаторов на метаболизм глюкозы и липидов. Curr Med Res Opin. 2010;26:615–29. КАС
пабмед
Статья
Google ученый Савица В., Беллингьери Г., Коппле Д.Д. Влияние питания на артериальное давление. Анну Рев Нутр. КАС
пабмед
Статья
Google ученый Chan Q, Stamler J, Griep LMO, Daviglus ML, Horn LV, Elliott P. Последние новости о питательных веществах и артериальном давлении. J Атеросклеротический тромб. 2016; 23: 276–89. ПабМед
Статья
Google ученый Hall JE, Granger JP, do Carmo JM, da Silva AA, Dubinion J, George E, et al. Артериальная гипертензия: физиология и патофизиология. сост. физиол. 2012;2:2393–442. ПабМед
Статья
Google ученый Те Риет Л., ван Эш Дж.Х.М., Рокс А.Дж.М., ван ден Мейраккер А.Х., Дансер А.Х.Дж. Артериальная гипертензия: изменения ренин-ангиотензин-альдостероновой системы. Цирк рез. 2015;116:960–75. Артикул
КАС
Google ученый Патель С., Рауф А., Хан Х., Абу-Изнейд Т. Ренин-ангиотензин-альдостерон (РААС): вездесущая система гомеостаза и патологий. Биомед Фармаколог. 2017;94:317–25. КАС
пабмед
Статья
Google ученый Хартупи Дж., Манн Д.Л. Нейрогормональная активация при сердечной недостаточности со сниженной фракцией выброса. Нат Рев Кардиол. 2017;14:30–8. КАС
пабмед
Статья
Google ученый Миллер А.Дж., Арнольд А.С. Ренин-ангиотензиновая система в автономном контроле сердечно-сосудистой системы: последние разработки и клинические последствия. Клин Автон Рез. 2019;29:231–43. ПабМед
Статья
Google ученый Грасси Г., Рам В.С. Доказательства критической роли симпатической нервной системы при гипертонии. J Am Soc Hypertens JASH. 2016;10:457–66. КАС
пабмед
Статья
Google ученый Вервайн Э.А., Орер Х.С., Барман С.М. Обзор анатомии, физиологии и фармакологии вегетативной нервной системы. сост. физиол. 2016;6:1239–78. ПабМед
Статья
Google ученый 20.4 Гомеостатическая регуляция сосудистой системы — Анатомия и физиология человека Колледжа Дугласа I, 1-е издание. https://pressbooks.bccampus.ca/dcbiol11031109/глава/20-4-гомеостатическая-регуляция-сосудистой-системы/. По состоянию на 30 сентября 2019 г. Руи Л. Энергетический обмен в печени. сост. физиол. 2014;4:177–97. ПабМед
ПабМед Центральный
Статья
Google ученый Ahrén B. Вегетативная регуляция секреции гормонов островков — последствия для здоровья и болезней. Диабетология. ПабМед
Статья
Google ученый Pénicaud L. Вегетативная нервная система и кровоток островков поджелудочной железы. Биохимия. 2017; 143:29–32. ПабМед
Статья
КАС
Google ученый Яхаги Н. Печеночный контроль энергетического обмена через вегетативную нервную систему. J Атеросклеротический тромб. 2017; 24:14–8. ПабМед
ПабМед Центральный
Статья
Google ученый Grassi G. Оценка симпатического сердечно-сосудистого влечения при артериальной гипертензии человека: достижения и перспективы. Hypertens Dallas Tex. 1979; 2009 (54): 690–7. Google ученый Cosson E, Valensi P, Laude D, Mesangeau D, Dabire H. Жесткость артерий и вегетативная нервная система во время развития диабетических жирных крыс Zucker. КАС
пабмед
Статья
Google ученый Коссон Э., Херисс М., Лауд Д., Томас Ф., Валенси П., Аттали Дж.-Р. и др. Жесткость аорты и усиление пульсового давления у крыс Вистар-Киото и крыс со спонтанной гипертензией. Am J Physiol Heart Circ Physiol. 2007; 292:h3506-2512. КАС
пабмед
Статья
Google ученый Грасси Г., Марк А., Эслер М. Изменения симпатической нервной системы при гипертонии человека. Цирк рез. 2015; 116: 976–90. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Манолис А.Дж., Пулименос Л.Е., Каллистратос М.С., Гаврас И., Гаврас Х. Симпатическая гиперактивность при гипертонии и сердечно-сосудистых заболеваниях. Курр Васк Фармакол. 2014; 12:4–15. КАС
пабмед
Статья
Google ученый Preckel D, von Känel R. Регуляция гемостаза симпатической нервной системой: какой-либо вклад в ишемическую болезнь сердца? Слушайте испытания Excell Cardiovasc. 2004; 4: 123–30. Google ученый Парати Г., Эслер М. Симпатическая нервная система человека: ее значение при гипертонии и сердечной недостаточности. Европейское сердце J. 2012; 33: 1058–66. КАС
пабмед
Статья
Google ученый Triposkiadis F, Karayannis G, Giamouzis G, Skoularigis J, Louridas G, Butler J. Симпатическая нервная система в физиологии сердечной недостаточности, патофизиологии и клинических последствиях. J Am Coll Кардиол. 2009 г.;54:1747–62. КАС
пабмед
Статья
Google ученый Manzella D, Barbieri M, Rizzo MR, Ragno E, Passariello N, Gambardella A, et al. Артикул
Google ученый Карнагарин Р., Мэтьюз В.Б., Герат Л.И., Хо Дж.К., Шлайх М.П. Вегетативная регуляция гомеостаза глюкозы: особая роль активации симпатической нервной системы. Curr Diabetes Rep. 2018; 18:107. Артикул
КАС
Google ученый Брук Р.Д., Джулиус С. Автономный дисбаланс, гипертония и риск сердечно-сосудистых заболеваний. Ам Дж Гипертенс. 2000;13:112С-122С. КАС
пабмед
Статья
Google ученый Morton GJ, Muta K, Kaiyala KJ, Rojas JM, Scarlett JM, Matsen ME, et al. Доказательства того, что симпатическая нервная система вызывает быструю, скоординированную и взаимную регулировку секреции инсулина и чувствительности к инсулину во время воздействия холода. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Schumann U, Jenkinson CP, Alt A, Zügel M, Steinacker JM, Flechtner-Mors M. Активность симпатической нервной системы и антилиполитический ответ на внутривенную нагрузку глюкозой в подкожной жировой ткани у пациентов с ожирением и диабетом 2 типа с ожирением . ПЛОС ОДИН. 2017;12:e0173803. ПабМед
ПабМед Центральный
Статья
КАС
Google ученый Straznicky NE, Grima MT, Sari CI, Lambert EA, Phillips SE, Eikelis N, et al. Снижение периферического сосудистого сопротивления предсказывает улучшение клиренса инсулина после снижения веса. Сердечно-сосудистый Диабетол. 2015;14:113. ПабМед
ПабМед Центральный
Статья
КАС
Google ученый Эдвардс К. КАС
Статья
Google ученый Гойт РК, Ансари АХ. Снижение парасимпатического тонуса при впервые диагностированной эссенциальной гипертензии. Indian Heart J. 2016; 68: 153–7. ПабМед
ПабМед Центральный
Статья
Google ученый Диабет при сердечно-сосудистых заболеваниях: спутник болезни сердца Браунвальда. 1-е издание. https://www.elsevier.com/books/диабет-в-сердечно-сосудистых заболеваниях-a-companion-to-braunwalds-heart-disease/mcguire/978-1-4557-5418-2. По состоянию на 3 октября 2019 г. Аяд Ф., Белхадж М. КАС
Статья
Google ученый Thorp AA, Schlaich MP. Актуальность активации симпатической нервной системы при ожирении и метаболическом синдроме. J Диабет Res. 2015;2015:341583. ПабМед
ПабМед Центральный
Статья
Google ученый Шапело Д., Шарло К. Физиология энергетического гомеостаза: модели, участники, проблемы и глюкоадипостатическая петля. Метаболизм. 2019;92:11–25. КАС
пабмед
Статья
Google ученый Grassi G, Seravalle G, Dell’Oro R, Turri C, Bolla GB, Mancia G. Адренергические и рефлекторные нарушения при гипертонии, связанной с ожирением. КАС
пабмед
Статья
Google ученый Линдмарк С., Лённ Л., Виклунд У., Тафвессон М., Олссон Т., Эрикссон Дж.В. Дисрегуляция вегетативной нервной системы может быть связующим звеном между висцеральным ожирением и резистентностью к инсулину. Обес Рез. 2005; 13: 717–728. КАС
пабмед
Статья
Google ученый Гуарино Д., Наннипьери М., Иерваси Г., Таддей С., Бруно Р.М. Роль вегетативной нервной системы в патофизиологии ожирения. Фронт Физиол. 2017;8:665. ПабМед
ПабМед Центральный
Статья
Google ученый Карнагарин Р., Мэтьюз В., Грегори С., Шлайх М.П. Фармакотерапевтические стратегии лечения артериальной гипертензии у пациентов с ожирением. Эксперт Опин Фармаколог. 2018;19:643–51. КАС
пабмед
Статья
Google ученый Тентолурис Н., Цигос С., Переа Д., Кукоу Э., Кириаки Д., Китсоу Э. и др. Дифференциальное влияние изоэнергетической пищи с высоким содержанием жиров и углеводов на деятельность вегетативной нервной системы сердца у худых и тучных женщин. Метаболизм. 2003; 52:1426–32. КАС
пабмед
Статья
Google ученый Нагаи Н., Сакане Н., Хамада Т., Кимура Т., Моритани Т. Влияние высокоуглеводной пищи на постпрандиальный термогенез и активность симпатической нервной системы у мальчиков с недавним началом ожирения. Метаболизм. 2005; 54:430–8. КАС
пабмед
Статья
Google ученый Straznicky NE, Lambert GW, Masuo K, Dawood T, Eikelis N, Nestel PJ, et al. Притупленный симпатический нервный ответ на пероральный прием глюкозы у пациентов с ожирением и инсулинорезистентным метаболическим синдромом. Am J Clin Nutr. 2009 г. КАС
пабмед
Статья
Google ученый Валенси П., Нгок П.Б., Идрисс С., Париес Дж., Казес П., Лормо Б. и др. Гемодинамический ответ на изометрический тест с физической нагрузкой у пациентов с ожирением: влияние вегетативной дисфункции. Int J Obes Relat Metab Disord. 1999; 23: 543–9. КАС
пабмед
Статья
Google ученый Валенси П., Смаггью О., Парьес Дж., Велаюдон П., Лормо Б., Аттали Дж. Р. Нарушение кожного сосудосуживающего ответа на симпатическую активацию у пациентов с ожирением: влияние реологических нарушений. Метаболизм. 2000;49: 600–6. КАС
пабмед
Статья
Google ученый Ma D, Feitosa MF, Wilk JB, Laramie JM, Yu K, Leiendecker-Foster C, et al. Лептин связан с кровяным давлением и гипертонией у женщин из исследования семейного сердца Национального института сердца, легких и крови. Google ученый Белл Б.Б., Рахмуни К. Лептин как медиатор гипертонии, вызванной ожирением. Представитель Curr Obes, 2016; 5:397–404. ПабМед
ПабМед Центральный
Статья
Google ученый Ваз М., Дженнингс Г., Тернер А., Кокс Х., Ламберт Г., Эслер М. Регионарная симпатическая нервная активность и потребление кислорода у людей с нормальным давлением, страдающих ожирением. Тираж. 1997; 96:3423–9. КАС
пабмед
Статья
Google ученый Lee ZS, Critchley JA, Tomlinson B, Young RP, Thomas GN, Cockram CS, et al. Взаимосвязь адреналина и норадреналина в моче с ожирением, инсулином и метаболическим синдромом у гонконгских китайцев. Метаболизм. 2001; 50: 135–43. КАС
пабмед
Статья
Google ученый Грасси Г., Серавалле Г., Каттанео Б.М., Болла Г.Б., Ланфранчи А., Коломбо М. и др. Симпатическая активация у тучных нормотензивных субъектов. Hypertens Dallas Tex 1979. 1995; 25: 560–3. КАС
Google ученый Grassi G, Dell’Oro R, Facchini A, Quarti Trevano F, Bolla GB, Mancia G. Влияние центрального и периферического распределения жира в организме на симпатическую и барорефлекторную функцию у нормотензивов с ожирением. Дж Гипертензия. 2004; 22:2363–9. КАС
пабмед
Статья
Google ученый Стразницкий Н.Е., Ламберт Э.А., Ламберт Г.В., Масуо К., Эслер М.Д., Нестель П.Дж. Влияние диетической потери веса на симпатическую активность и сердечные факторы риска, связанные с метаболическим синдромом. J Clin Endocrinol Metab. 2005;90:5998–6005. КАС
пабмед
Статья
Google ученый Ламберт Э.А., Эслер М.Д., Шлайх М.П., Диксон Дж., Эйкелис Н., Ламберт Г.В. Связанное с ожирением органное поражение и активность симпатической нервной системы. Гипертенс Даллас Текс 1979. 1979; 73: 1150–9. Google ученый de Jonge L, Moreira EAM, Martin CK, Ravussin E, Pennington CALERIE Team. Влияние 6-месячного ограничения калорийности на активность вегетативной нервной системы у здоровых людей с избыточным весом. Obes Silver Spring Md. 2010; 18: 414–6. Артикул
Google ученый Ван Де Борн П., Хаусберг М., Хоффман Р.П., Марк А.Л., Андерсон Э.А. Гиперинсулинемия вызывает отключение блуждающего нерва и неравномерную симпатическую активацию у здоровых людей. Am J Physiol-Regul Integr Comp Physiol. 1999;276:R178–83. Артикул
Google ученый Vollenweider P, Tappy L, Randin D, Schneiter P, Jéquier E, Nicod P, et al. Дифференциальное влияние гиперинсулинемии и углеводного обмена на активность симпатических нервов и мышечный кровоток у человека. Джей Клин Инвест. 1993; 92: 147–54. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Холл Дж. Э., ду Карму Дж. М., да Силва А. А., Ван З., Холл М. Э. Гипертония, вызванная ожирением: взаимодействие нейрогуморальных и почечных механизмов. Цирк рез. 2015; 116:991–1006. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Чихеб С., Коссон Э., Бану И., Хамо-Чачуанг Э., Кюссак-Пиллеганд С., Нгуен М. и др. Действительно ли здоровы тучные люди без метаболического синдрома, но с увеличенной окружностью талии? Поперечное исследование. Exp Clin Endocrinol Diabetes. 2016; 124:410–6. КАС
пабмед
Статья
Google ученый Valensi P, Doaré L, Perret G, Germack R, Pariès J, Mesangeau D. Сердечно-сосудистая вагосимпатическая активность у крыс с вентромедиальным гипоталамическим ожирением. Обес Рез. 2003; 11:54–64. ПабМед
Статья
Google ученый Валенси П., Чихеб С., Фисекидис М. Инсулино- и глюкагоноподобные пептид-1-индуцированные изменения частоты сердечных сокращений и вагосимпатической активности: почему они имеют значение. Диабетология. 2013;56:1196–200. КАС
пабмед
Статья
Google ученый Baggio LL, Ussher JR, McLean BA, Cao X, Kabir MG, Mulvihill EE, et al. Вегетативная нервная система и сердечные рецепторы GLP-1 контролируют частоту сердечных сокращений у мышей. Мол метаб. 2017;6:1339–49. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Rowlands J, Heng J, Newsholme P, Carlessi R. Плейотропные эффекты GLP-1 и аналогов на клеточную передачу сигналов, метаболизм и функцию. Передний эндокринол. 2018;9:672. Артикул
Google ученый Гонсалес-Гарсия И., Милбанк Э., Диегес С., Лопес М., Контрерас С. Глюкагон, ГПП-1 и термогенез. Int J Mol Sci. 2019;20:3445. https://doi.org/10.3390/ijms20143445. КАС
Статья
ПабМед Центральный
Google ученый Barragán JM, Rodríguez RE, Blázquez E. Изменения артериального давления и частоты сердечных сокращений, вызванные амидом глюкагоноподобного пептида-1-(7–36) у крыс. Am J Physiol. 1994;266:Е459-466. ПабМед
Google ученый Barragán JM, Rodríguez RE, Eng J, Blázquez E. Взаимодействие экзендина-(9–39) с эффектами амида глюкагоноподобного пептида-1-(7–36) и экзендина-4 на артериальную кровь давление и частота сердечных сокращений у крыс. ПабМед
Статья
Google ученый Ямамото Х., Киши Т., Ли К.Э., Чой Б.Дж., Фанг Х., Холленберг А.Н. и др. Реагирующие на глюкагоноподобный пептид-1 катехоламиновые нейроны в пострематической области связывают периферический глюкагоноподобный пептид-1 с центральными вегетативными участками контроля. Дж. Нейроски. 2003;23:2939–46. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Yamamoto H, Lee CE, Marcus JN, Williams TD, Overton JM, Lopez ME, et al. Стимуляция рецептора глюкагоноподобного пептида-1 повышает кровяное давление и частоту сердечных сокращений и активирует вегетативные регуляторные нейроны. Джей Клин Инвест. 2002; 110:43–52. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Griffioen KJ, Wan R, Okun E, Wang X, Lovett-Barr MR, Li Y, et al. Стимуляция рецептора GLP-1 снижает вариабельность сердечного ритма и ингибирует нейротрансмиссию к нейронам блуждающего нерва сердца. Кардиовасц Рез. 2011;89:72–78. КАС
пабмед
Статья
Google ученый Нистрем Т., Гутняк М.К., Чжан К., Чжан Ф., Холст Дж.Дж., Арен Б. и др. Влияние глюкагоноподобного пептида-1 на функцию эндотелия у больных сахарным диабетом 2 типа со стабильной ишемической болезнью сердца. Am J Physiol-Endocrinol Metab. 2004;287:E1209–15. ПабМед
Статья
КАС
Google ученый Sforza E, Martin MS, Barthélémy JC, Roche F. Существует ли связь между измененной чувствительностью барорецепторов и обструктивным апноэ во сне у здоровых пожилых людей? ERJ Open Res. 2016. https://doi.org/10.1183/23120541.00072-2016. Артикул
пабмед
ПабМед Центральный
Google ученый Чжан Д.Ю., Андерсон А.С. Симпатическая нервная система и сердечная недостаточность. Кардиол клин. 2014;32:33–45, vii. ПабМед
ПабМед Центральный
Статья
Google ученый Somers VK, Dyken ME, Clary MP, Abboud FM. Симпатические нервные механизмы при обструктивном апноэ сна. Джей Клин Инвест. 1995; 96: 1897–904. КАС
пабмед
ПабМед Центральный
Статья
Google ученый Карнагарин Р., Ламберт Г.В., Киучи М.Г., Нольде Дж.М., Мэтьюз В.Б., Эйкелис Н. и др. Эффекты симпатической модуляции при метаболических заболеваниях. Энн Н.Ю. Академия наук. 2019;1454:80–9. ПабМед
Статья
Google ученый Борель А.-Л., Тамизиер Р., Бёме П., Приу П., Авиньон А., Бенхаму П.Ю. и др. Синдром обструктивного апноэ сна у больных сахарным диабетом: каких пациентов следует обследовать? Диабет метаб. ПабМед
Статья
Google ученый Уайт Д.В., Шумейкер Дж.К., Рэйвен П.Б. Методы и соображения для анализа и стандартизации оценки активности мышечных симпатических нервов у людей. Автон Нейроски. 2015;193:12–21. ПабМед
ПабМед Центральный
Статья
Google ученый Мейсфилд В. Симпатическая микронейрография. Handb Clin Neurol. 2013; 117: 353–64. ПабМед
Статья
Google ученый Greaney J, Kenney W. Измерение и количественная оценка активности симпатической нервной системы кожи у людей. J Нейрофизиол. 2017;118:2181–93. ПабМед
ПабМед Центральный
Статья
Google ученый Матиас СиДжей, Баннистер С.Р. Вегетативная недостаточность: учебник клинических расстройств вегетативной нервной системы. Книга
Google ученый Эслер М., Леонард П., О’Ди К., Джекман Г., Дженнингс Г., Корнер П. Биохимическая количественная оценка активности симпатической нервной системы у людей с использованием радиофармпрепарата: погрешность измерений норадреналина в плазме. J Cardiovasc Pharmacol. 1982;4(Приложение 1):S152-157. ПабМед
Статья
Google ученый Verberne HJ, Brewster LM, Somsen GA, van Eck-Smit BLF. Прогностическое значение параметров миокарда 123I-метайодбензилгуанидина (MIBG) у пациентов с сердечной недостаточностью: систематический обзор. Европейское сердце J. 2008; 29: 1147–59. ПабМед
Статья
Google ученый Бернарди Л., Спаллоне В., Стивенс М., Хилстед Дж., Фронтони С., Поп-Бусуи Р. и др. Методы исследования вегетативной дисфункции сердца в исследованиях на людях: методы исследования вегетативной функции сердца. ПабМед
Статья
Google ученый Буччеллетти Э., Джиларди Э., Скайни Э., Галиуто Л., Персиани Р., Бионди А. и др. Вариабельность сердечного ритма и инфаркт миокарда: систематический обзор литературы и метаанализ. Eur Rev Med Pharmacol Sci. 2009; 13: 299–307. КАС
пабмед
Google ученый Эрнст Г. Вариабельность сердечного ритма — больше, чем сердечные сокращения? Фронт общественного здравоохранения. 2017;5:240. ПабМед
ПабМед Центральный
Статья
Google ученый Парати Г. Вариабельность артериального давления: ее измерение и значение при гипертонии. Приложение J Hypertens. 2005;23:S19-25. КАС
пабмед
Статья
Google ученый Констант И., Лауд Д., Эльгози Ж.Л., Мурат И. Оценка краткосрочной вариабельности артериального давления у наркотизированных детей: сравнительное исследование внутриартериального и пальцевого артериального давления. J Clin Monit Comput. 1999;15:205–14. КАС
пабмед
Статья
Google ученый Rudas L, Crossman AA, Morillo CA, Halliwill JR, Tahvanainen KU, Kuusela TA, et al. Симпатические и вагусные барорефлексные реакции человека на последовательные нитропруссид и фенилэфрин. Am J Physiol. 1999;276:h2691-1698. КАС
пабмед
Google ученый Dutoit AP, Hart EC, Charkoudian N, Wallin BG, Curry TB, Joyner MJ. Чувствительность сердечного барорефлекса не коррелирует с чувствительностью симпатического барорефлекса у здоровых молодых людей. Гипертенс Даллас Текс 1979. 2010;56:1118–23. КАС
Google ученый Laude D, Elghozi J-L, Girard A, Bellard E, Bouhaddi M, Castiglioni P, et al. Сравнение различных методов, используемых для оценки чувствительности спонтанного барорефлекса (исследование EuroBaVar). Am J Physiol Regul Integr Comp Physiol. 2004; 286: R226-231. КАС
пабмед
Статья
Google ученый Экберг Д.Л. Нелинейности каротидного барорецепторно-сердечного рефлекса человека. Цирк рез. 1980;47:208–16. КАС
пабмед
Статья
Google ученый La Rovere MT, Pinna GD, Raczak G. Чувствительность барорефлекса: измерение и клинические последствия. Энн Неинвазивная электрокардиология. 2008; 13: 191–207. ПабМед
ПабМед Центральный
Статья
Google ученый Ядав Р.Л., Ядав П.К., Ядав Л.К., Агравал К., Сах С.К., Ислам М.Н. Артикул
Google ученый Сугита Н., Йошизава М., Абэ М., Танака А., Тиба С., Ямбе Т. и др. Сравнение максимального коэффициента кросс-корреляции между артериальным давлением и частотой сердечных сокращений с традиционным показателем, связанным с чувствительностью барорефлекса. В: 2008 г. 30-я ежегодная международная конференция инженерного сообщества IEEE в области медицины и биологии. Ванкувер, Британская Колумбия: IEEE; 2008. стр. 2574–7. Farquhar WB, Edwards DG, Jurkovitz CT, Weintraub WS. Диетический натрий и здоровье: больше, чем просто кровяное давление. J Am Coll Кардиол. 2015;65:1042–50. КАС
пабмед
ПабМед Центральный
Статья
Google ученый González SA, Forcada P, de Cavanagh EMV, Inserra F, Svane JC, Obregón S, et al. Потребление натрия связано с парасимпатическим тонусом и метаболическими параметрами при легкой гипертензии. Ам Дж Гипертенс. 2012;25:620–4. ПабМед
Статья
КАС
Google ученый Санчес-Альварес С., Гонсалес-Велес М., Стилп Э., Уорд С., Мена-Уртадо С. Симпатическая денервация почек при лечении резистентной гипертензии. Йель Дж Биол Мед. 2014; 87: 527–35. ПабМед
ПабМед Центральный
Google ученый Osborn JW, Banek CT. Катетерная абляция почечного нерва как новая терапия гипертонии: потеряна, а затем найдена в переводе. Hypertens Dallas Tex 1979. 2018; 71: 383–8. КАС
Google ученый Азизи М., Саповал М., Госсе П., Монж М., Бобри Г., Дельсарт П. Артикул
Google ученый Персу А., Маес Ф., Ренкин Дж., Патхак А. Денервация почек у пациентов с гипертонией: возвращение к анатомии? Гипертония. 2020; 76: 1084–1086. КАС
пабмед
Статья
Google ученый Хатипоглу Э., Ферро А. Катетерная почечная денервация для лечения резистентной гипертензии. JRSM Cardiovasc Dis. 2013;2:2048004013486634. ПабМед
ПабМед Центральный
Google ученый Бём М., Махфуд Ф., Таунсенд Р.Р., Кандзари Д.Е., Покок С., Укена С. и др. Амбулаторное снижение частоты сердечных сокращений после катетерной почечной денервации у пациентов с артериальной гипертензией, не получающих антигипертензивные препараты: данные SPYRAL HTN-OFF MED, рандомизированного, плацебо-контролируемого, подтверждающего исследования исследования. ПабМед
Статья
Google ученый Каннан А., Медина Р.И., Нагаджоти Н., Баламутусами С. Симпатическая нервная система почек и влияние денервации на почечные артерии. Мир J Кардиол. 2014; 6: 814–23. ПабМед
ПабМед Центральный
Статья
Google ученый Йоханссон М., Элам М., Рундквист Б., Эйзенхофер Г., Херлиц Х., Дженсен Г. и др. Дифференцированный ответ симпатической нервной системы на ингибирование ангиотензинпревращающего фермента при артериальной гипертензии. Гипертенс Даллас Текс 1979. 2000; 36: 543–8. КАС
Google ученый Krum H, Lambert E, Windebank E, Campbell DJ, Esler M. Влияние блокады рецепторов ангиотензина II на функцию вегетативной нервной системы у пациентов с гипертонической болезнью. КАС
пабмед
Статья
Google ученый Чаттерджи С., Бионди-Зоккай Г., Аббате А., Д’Асенцо Ф., Кастаньо Д., Ван Тассел Б. и др. Преимущества β-блокаторов у пациентов с сердечной недостаточностью и сниженной фракцией выброса: сетевой метаанализ. БМЖ. 2013;346:f55. ПабМед
ПабМед Центральный
Статья
КАС
Google ученый Дель Колле С., Морелло Ф., Раббиа Ф., Милан А., Насо Д., Пульизи Э. и др. Антигипертензивные препараты и симпатическая нервная система. J Cardiovasc Pharmacol. 2007; 50: 487–96. ПабМед
Статья
КАС
Google ученый Ernsberger P. I1-имидазолиновый рецептор и его клеточные сигнальные пути. Энн Н.Ю. Академия наук. 1999;881:35–53. КАС
пабмед
Статья
Google ученый Уоллер, Сэмпсон. Медицинская фармакология и терапия Дерека Г. Уоллера и Энтони П. Сэмпсона | электронная книга об Инклинге. 5-е издание. 2018. https://www.inkling.com/store/book/waller-medical-pharmacology-therapy-5e/. По состоянию на 30 сентября 2019 г. Эдвардс Л.П., Браун-Брайан Т.А., Маклин Л., Эрнсбергер П. Фармакологические свойства центрального антигипертензивного средства, моксонидина. Кардиоваск Ther. 2012;30:199–208. КАС
пабмед
Статья
Google ученый Ernsberger P, Graves ME, Graff LM, Zakieh N, Nguyen P, Collins LA, et al. I1-имидазолиновые рецепторы. Определение, характеристика, распределение и трансмембранная передача сигналов. Энн Н.Ю. Академия наук. 1995; 763: 22–42. КАС
пабмед
Статья
Google ученый Head GA, Burke SL. I1-имидазолиновые рецепторы в сердечно-сосудистой регуляции: место рилменидина. КАС
пабмед
Статья
Google ученый Haenni A, Lithell H. Моксонидин улучшает чувствительность к инсулину у инсулинорезистентных гипертоников. Приложение J Hypertens. 1999;17:С29-35. КАС
пабмед
Google ученый Фентон С., Китинг Г.М., Лисенг-Уильямсон К.А. Моксонидин: обзор его применения при гипертонической болезни. Наркотики. 2006; 66: 477–9.6. КАС
пабмед
Статья
Google ученый Чазова И., Шлайх М.П. Улучшение контроля артериального давления с помощью имидазолинового агониста моксонидина в многонациональной популяции с метаболическим синдромом: основные результаты исследования MERSY. Int J Hypertens. 2013;2013:541689. ПабМед
ПабМед Центральный
Статья
КАС
Google ученый Schlaich MP, Almahmeed W, Arnaout S, Prabhakaran D, Zhernakova J, Zvartau N, et al. Роль селективных агонистов имидазолиновых рецепторов в современном лечении артериальной гипертензии: международное исследование в реальных условиях (STRAIGHT). Curr Med Res Opin. 2020;36:1939–45. КАС
пабмед
Статья
Google ученый Ссылки на скачивание Помощь в написании этой рукописи была предоставлена Solenn Le Clanche и Hicham Lamrini (KPL Paris) при финансовой поддержке Abbott. Предоставлено компанией Abbott. Отделение эндокринологии, диабетологии и питания, Больница Жана Вердье, CINFO, CRNH-IdF, AP-HP, Университет Париж-Норд, Avenue du 14 Juillet, 93140, Бонди, Франция Поль Валенси Авторы Просмотр публикаций автора Вы также можете искать этого автора в
PubMed Google Scholar Автор прочитал и одобрил окончательный вариант рукописи. Пол Валенси. Неприменимо. Неприменимо. Пол Валенси сообщает о следующих потенциальных конфликтах интересов: лекции для Abbott, AstraZeneca, Bayer, Lilly, Hikma Pharmaceuticals, Merck Sharp & Dohme, Novo Nordisk, Novartis, Pfizer, Sanofi; исследовательские гранты от Abbott, Bristol-Myers-Squibb-AstraZeneca, Novo Nordisk; участие в экспертных комитетах компаний AstraZeneca, Boehringer Ingelheim, Daiichi Sankyo, Lilly, Novo Nordisk, Sanofi, Servier, Stendo. Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности. Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4. рецепторов). Тем не менее, это зависит от оснащенности данного кровеносного сосуда указанными адренорецепторами и преобладающего типа рецептора. 
Влияние симпатической и парасимпатической нервной системы на отдельные органы
Глаз

Железы
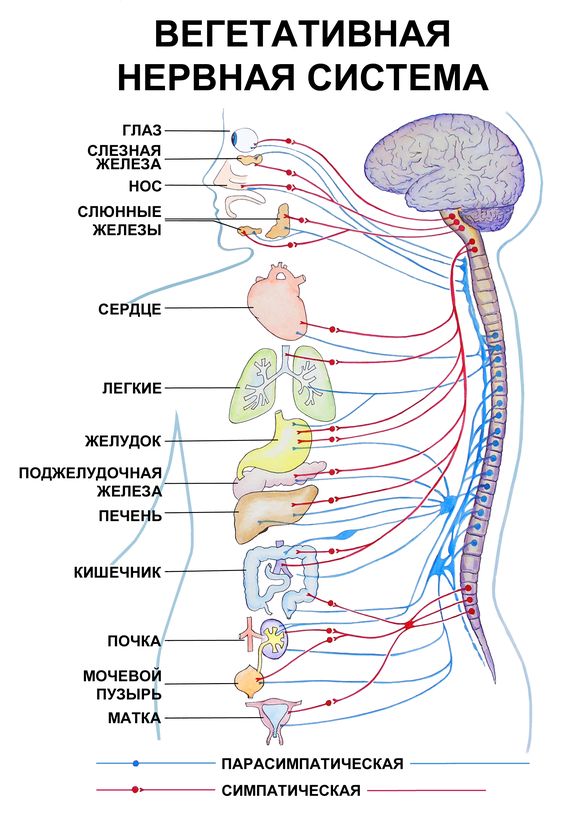 Интересно также, что активность потовых желез контролируется симпатические холинергические волокна .
Интересно также, что активность потовых желез контролируется симпатические холинергические волокна . Сердце
 Таким образом, повышенная парасимпатическая активность снижает стимулируемую симпатической нервной системой сократимость и частоту сердечных сокращений.
Таким образом, повышенная парасимпатическая активность снижает стимулируемую симпатической нервной системой сократимость и частоту сердечных сокращений. Артериальное давление
Симпатический и парасимпатический тонус
 Это явление называется симпатическим соответственно парасимпатическим тонусом и сходно с принципом тонуса в иннервируемых скелетных мышцах.
Это явление называется симпатическим соответственно парасимпатическим тонусом и сходно с принципом тонуса в иннервируемых скелетных мышцах. Если бы не было тонуса, во внимание принималась бы только вазоконстрикция, и симпатическая нервная система никогда не была бы способна производить относительную вазодилатацию.
Если бы не было тонуса, во внимание принималась бы только вазоконстрикция, и симпатическая нервная система никогда не была бы способна производить относительную вазодилатацию. Неврология для детей. Вегетативная нервная система
Вегетативная нервная система

— вокруг кровеносных сосудов (гладкие мышцы)
— в глазу (радужная оболочка; гладкие мышцы)
— в желудке, кишечнике и мочевом пузыре (гладкая мышца)
— сердца (сердечная мышца) Симпатическая нервная система 
 )
) Парасимпатическая нервная система  Из этого ганглия постганглионарная
нейрон проецируется на орган-мишень и использует ацетилхолин снова на своем
Терминал.
Из этого ганглия постганглионарная
нейрон проецируется на орган-мишень и использует ацетилхолин снова на своем
Терминал. Структура Симпатическая стимуляция Парасимпатическая
Стимуляция Радужка (мышца глаза) Расширение зрачка Зрачок
сужение Слюнные железы Выработка слюны
уменьшено Увеличение продукции слюны Слизистая оболочка полости рта/носа Продукция слизи
снижено Производство слизи увеличено Сердце Частота и сила сердечных сокращений
увеличен Частота и сила сердечных сокращений снижены Легкие Бронхиальные мышцы расслаблены Бронхиальные мышцы
сокращенный Желудок Перистальтика снижена Желудок
выделяется сок; подвижность повышена Тонкий кишечник Моторика
сниженный Пищеварение повышенный Толстый кишечник Моторика
снижение Повышение секреции и подвижности Печень Повышение конверсии
гликогена в глюкозу Почки Уменьшение количества мочи
секреция Повышенная секреция мочи Мозговое вещество надпочечников Норадреналин и
адреналин
секретный Мочевой пузырь Расслабленная стенка
Сфинктер
закрытый Стенка сокращена
Сфинктер расслаблен Он активен НЕ только во время «бей или беги» или «отдыхай и переваривай».
ситуации. Скорее вегетативная нервная система действует для поддержания нормального
внутренние функции и работает с соматической нервной системой.
Он активен НЕ только во время «бей или беги» или «отдыхай и переваривай».
ситуации. Скорее вегетативная нервная система действует для поддержания нормального
внутренние функции и работает с соматической нервной системой. ПОПРОБУЙ! —> Интерактивный поиск слов
Головоломка про вегетативную нервную систему. Центральный контроль вегетативной нервной системы и терморегуляции (раздел 4, глава 3) Neuroscience Online: Электронный учебник по нейронаукам | Кафедра нейробиологии и анатомии
 1
1
Обзор центральной автономной сети В совокупности этот набор взаимосвязей называется центральной автономной сетью.
В совокупности этот набор взаимосвязей называется центральной автономной сетью. Иерархия в вегетативной сети приводит к тому, что петли от ствола головного мозга к спинному мозгу отвечают за быструю кратковременную регуляцию вегетативной нервной системы, пути гипоталамо-стволового мозга-спинного мозга служат для долгосрочной регуляции метаболизма и репродуктивной функции и, наконец, лимбической системы. — гипоталамо-стволово-спинномозговые петли, обеспечивающие антиципационную вегетативную регуляцию.
Иерархия в вегетативной сети приводит к тому, что петли от ствола головного мозга к спинному мозгу отвечают за быструю кратковременную регуляцию вегетативной нервной системы, пути гипоталамо-стволового мозга-спинного мозга служат для долгосрочной регуляции метаболизма и репродуктивной функции и, наконец, лимбической системы. — гипоталамо-стволово-спинномозговые петли, обеспечивающие антиципационную вегетативную регуляцию. Подробнее об этих двух функциональных группах будет рассказано в следующей главе. Наконец, группа парвоцеллюлярных нейронов включает третью функциональную группу нейронов PVN, которые участвуют в центральном вегетативном контроле.
Подробнее об этих двух функциональных группах будет рассказано в следующей главе. Наконец, группа парвоцеллюлярных нейронов включает третью функциональную группу нейронов PVN, которые участвуют в центральном вегетативном контроле. Таким образом, PVN, в отличие от любого другого участка мозга, имеет прямое влияние как на симпатический, так и на парасимпатический отток. Кроме того, PVN получает прямые симпатические и парасимпатические афферентные импульсы от хвостовой части тройничного нерва (симпатическая) и ядра одиночного тракта (парасимпатическая). Таким образом, PVN является единственным мозговым участком в замкнутой эфферентно-афферентной рефлекторной петле как с симпатической, так и с парасимпатической нервной системой.
Таким образом, PVN, в отличие от любого другого участка мозга, имеет прямое влияние как на симпатический, так и на парасимпатический отток. Кроме того, PVN получает прямые симпатические и парасимпатические афферентные импульсы от хвостовой части тройничного нерва (симпатическая) и ядра одиночного тракта (парасимпатическая). Таким образом, PVN является единственным мозговым участком в замкнутой эфферентно-афферентной рефлекторной петле как с симпатической, так и с парасимпатической нервной системой.
Схема центральной автономной сети Наконец, лимбическая кора, включая поясную, орбитофронтальную, островковую и ринальную кору, а также гиппокамп влияет на оба набора автономного оттока.
Наконец, лимбическая кора, включая поясную, орбитофронтальную, островковую и ринальную кору, а также гиппокамп влияет на оба набора автономного оттока. 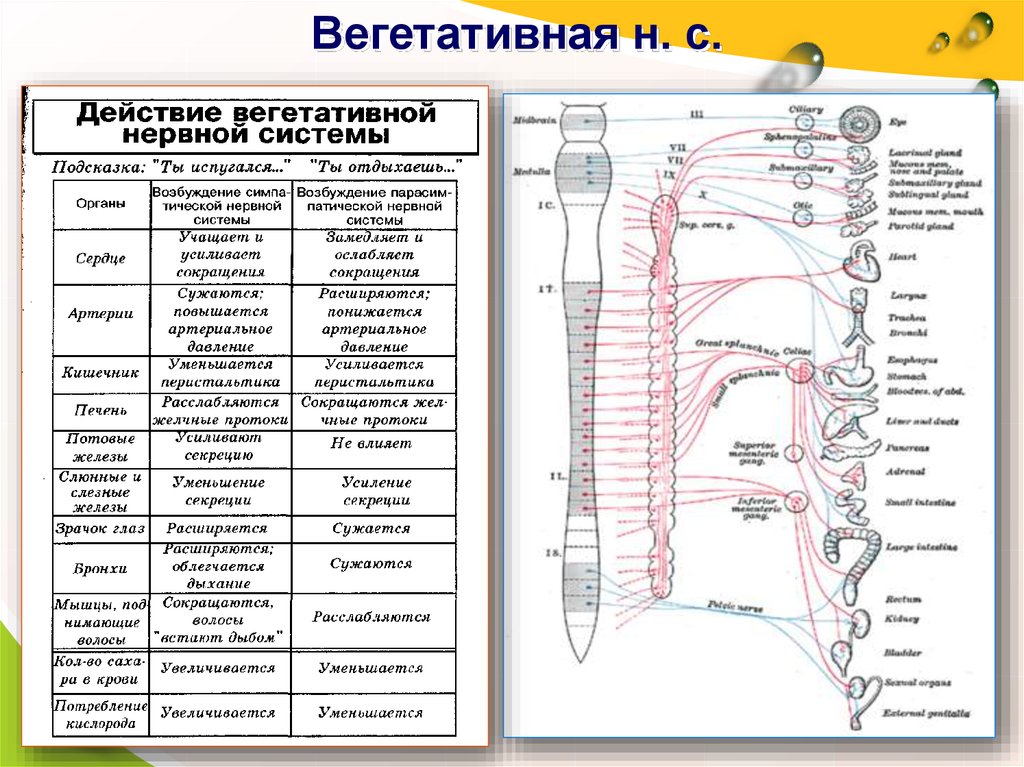 Централизованное расположение DLF, поскольку он продолжается в нижний отдел продолговатого мозга, а затем в спинной мозг, делает его идеальным местом для иннервации парасимпатических и симпатических нейронов промежуточно-латерального спинного мозга. Как подробно описано выше, проекции DLF являются двусторонними, хотя и с ипсилатеральным преобладанием из-за нескольких точек пересечения. Афферентные входы от периакведуктального серого, парабрахиального ядра и голубого пятна поднимаются через DLF к гипоталамусу.
Централизованное расположение DLF, поскольку он продолжается в нижний отдел продолговатого мозга, а затем в спинной мозг, делает его идеальным местом для иннервации парасимпатических и симпатических нейронов промежуточно-латерального спинного мозга. Как подробно описано выше, проекции DLF являются двусторонними, хотя и с ипсилатеральным преобладанием из-за нескольких точек пересечения. Афферентные входы от периакведуктального серого, парабрахиального ядра и голубого пятна поднимаются через DLF к гипоталамусу. Висцеральные афференты от ядра солитарного пути поднимаются от ствола мозга в гипоталамус через MFB. MFB, как и DLF, имеет несколько точек пересечения, так что есть входные данные для двусторонних структур, но с ипсилатеральным доминированием.
Висцеральные афференты от ядра солитарного пути поднимаются от ствола мозга в гипоталамус через MFB. MFB, как и DLF, имеет несколько точек пересечения, так что есть входные данные для двусторонних структур, но с ипсилатеральным доминированием.
Схема гипоталамического контроля вегетативной нервной системы Преувеличенные вегетативные рефлексы, особенно внезапное резкое повышение артериального давления, провоцируются неадекватными раздражителями, такими как давление на мочевой пузырь.
Преувеличенные вегетативные рефлексы, особенно внезапное резкое повышение артериального давления, провоцируются неадекватными раздражителями, такими как давление на мочевой пузырь.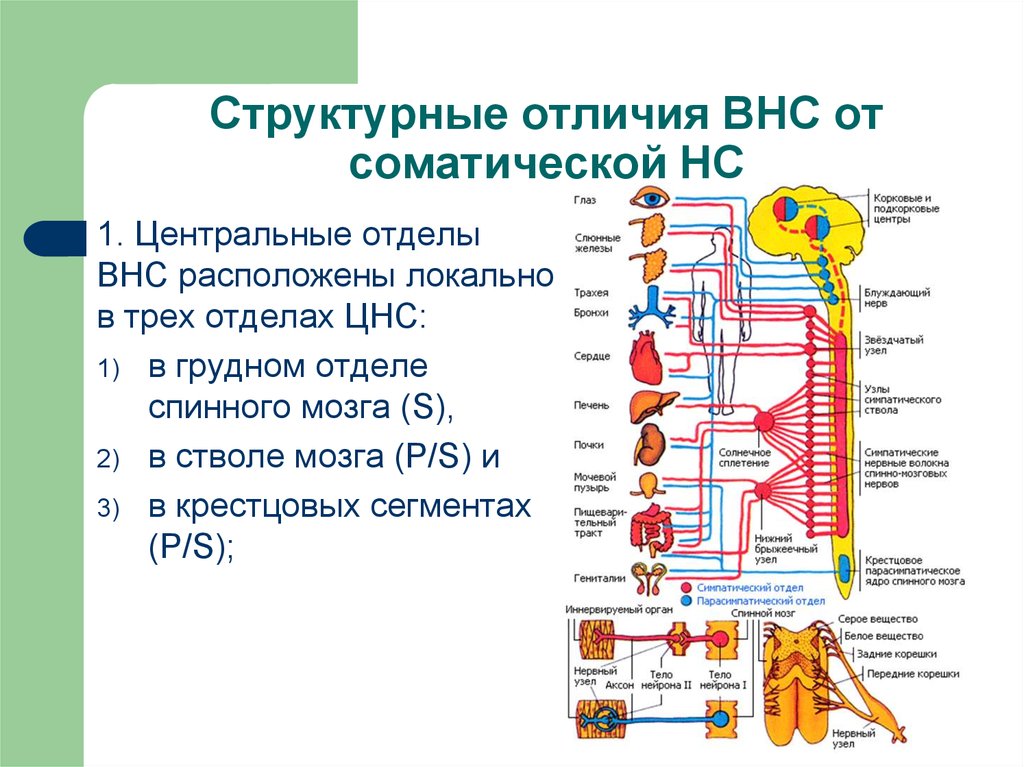 Отличительным признаком является глубокая ортостатическая гипотензия без компенсаторного увеличения частоты сердечных сокращений.
Отличительным признаком является глубокая ортостатическая гипотензия без компенсаторного увеличения частоты сердечных сокращений. 5 Центральная вегетативная сеть и контроль температуры тела
5 Центральная вегетативная сеть и контроль температуры тела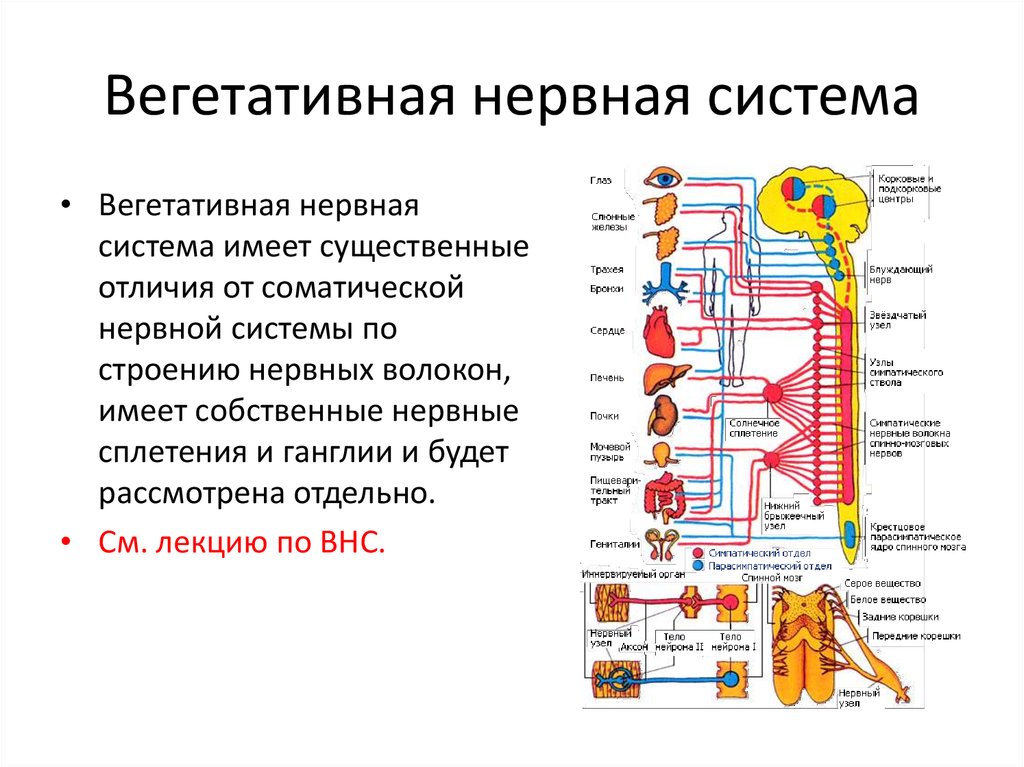 В совокупности эту область часто называют преоптическим передним гипоталамусом (POAH). Вторая область, которая также играет критическую, хотя и подчиненную роль ПОАГ, в регуляции температуры, — это задний гипоталамус.
В совокупности эту область часто называют преоптическим передним гипоталамусом (POAH). Вторая область, которая также играет критическую, хотя и подчиненную роль ПОАГ, в регуляции температуры, — это задний гипоталамус. Однако при повышении температуры выше 37 градусов скорость разряда этих нейронов резко возрастает. Активация теплочувствительных нейронов приводит к активации нейронов в паравентрикулярном ядре (PVN) и латеральном гипоталамусе, что приводит к усилению парасимпатического оттока, что способствует рассеиванию тепла. Холодочувствительные нейроны, которые составляют лишь около 5% клеточной популяции в POAH, но более распространены в заднем ядре гипоталамуса, обладают разрядными свойствами, противоположными теплочувствительным нейронам. Чувствительные к холоду нейроны демонстрируют низкую скорость разряда при температуре выше 37 градусов, но резко увеличивают скорость возбуждения при понижении температуры ниже 37 градусов. Увеличение разрядов в холодочувствительных нейронах приводит к активации нейронов в PVN и заднем гипоталамусе, что увеличивает симпатический отток, способствуя выработке и сохранению тепла. Относительная концентрация чувствительных к теплу нейронов в ПОАГ, которые способствуют потере тепла, и чувствительных к холоду нейронов в заднем гипоталамусе, которые способствуют выработке тепла, привела к тому, что ПОАГ часто называют центром рассеивания тепла, а задний гипоталамус обозначают как центр рассеяния тепла.
Однако при повышении температуры выше 37 градусов скорость разряда этих нейронов резко возрастает. Активация теплочувствительных нейронов приводит к активации нейронов в паравентрикулярном ядре (PVN) и латеральном гипоталамусе, что приводит к усилению парасимпатического оттока, что способствует рассеиванию тепла. Холодочувствительные нейроны, которые составляют лишь около 5% клеточной популяции в POAH, но более распространены в заднем ядре гипоталамуса, обладают разрядными свойствами, противоположными теплочувствительным нейронам. Чувствительные к холоду нейроны демонстрируют низкую скорость разряда при температуре выше 37 градусов, но резко увеличивают скорость возбуждения при понижении температуры ниже 37 градусов. Увеличение разрядов в холодочувствительных нейронах приводит к активации нейронов в PVN и заднем гипоталамусе, что увеличивает симпатический отток, способствуя выработке и сохранению тепла. Относительная концентрация чувствительных к теплу нейронов в ПОАГ, которые способствуют потере тепла, и чувствительных к холоду нейронов в заднем гипоталамусе, которые способствуют выработке тепла, привела к тому, что ПОАГ часто называют центром рассеивания тепла, а задний гипоталамус обозначают как центр рассеяния тепла. центр производства/сохранения тепла. Последняя группа нейронов, обнаруженных в POAH и заднем гипоталамусе, — это температурно-нечувствительные нейроны. Это, безусловно, самые многочисленные нейроны в этих ядрах, составляющие более 60 процентов нейронов в POAH. Хотя по определению они не чувствительны к изменениям температуры, эти нейроны играют решающую роль в выработке/сохранении тепла, как обсуждается ниже.
центр производства/сохранения тепла. Последняя группа нейронов, обнаруженных в POAH и заднем гипоталамусе, — это температурно-нечувствительные нейроны. Это, безусловно, самые многочисленные нейроны в этих ядрах, составляющие более 60 процентов нейронов в POAH. Хотя по определению они не чувствительны к изменениям температуры, эти нейроны играют решающую роль в выработке/сохранении тепла, как обсуждается ниже.
Нейронный механизм задания температуры тела. Щелкайте по восьмиугольникам. Чувствительные к теплу нейроны также получают возбуждающие импульсы от кожных и спинальных терморецепторов. Как показано на рис. 3.4, входные сигналы от кожных рецепторов индуцируют левое смещение в частоте возбуждения теплочувствительных нейронов гипоталамуса, так что исходная скорость разряда значительно повышается. Интересно, что хотя скорость возбуждения этих клеток продолжает увеличиваться с повышением температуры тела, наклон этого увеличения уменьшается. Таким образом, стремление рассеивать тепло активно управляется поступлениями от тепловых рецепторов. Неясно, как обстоит дело с выработкой и сохранением тепла. Чувствительные к холоду нейроны, по-видимому, не имеют собственных термочувствительных рецепторов. Скорее, увеличение разряда, наблюдаемое в чувствительных к холоду клетках при охлаждении, является результатом уменьшения разряда чувствительных к теплу нейронов и последующего растормаживания, так что чувствительные к холоду нейроны теперь управляются тоническими входами от нечувствительных к теплу нейронов.
Чувствительные к теплу нейроны также получают возбуждающие импульсы от кожных и спинальных терморецепторов. Как показано на рис. 3.4, входные сигналы от кожных рецепторов индуцируют левое смещение в частоте возбуждения теплочувствительных нейронов гипоталамуса, так что исходная скорость разряда значительно повышается. Интересно, что хотя скорость возбуждения этих клеток продолжает увеличиваться с повышением температуры тела, наклон этого увеличения уменьшается. Таким образом, стремление рассеивать тепло активно управляется поступлениями от тепловых рецепторов. Неясно, как обстоит дело с выработкой и сохранением тепла. Чувствительные к холоду нейроны, по-видимому, не имеют собственных термочувствительных рецепторов. Скорее, увеличение разряда, наблюдаемое в чувствительных к холоду клетках при охлаждении, является результатом уменьшения разряда чувствительных к теплу нейронов и последующего растормаживания, так что чувствительные к холоду нейроны теперь управляются тоническими входами от нечувствительных к теплу нейронов.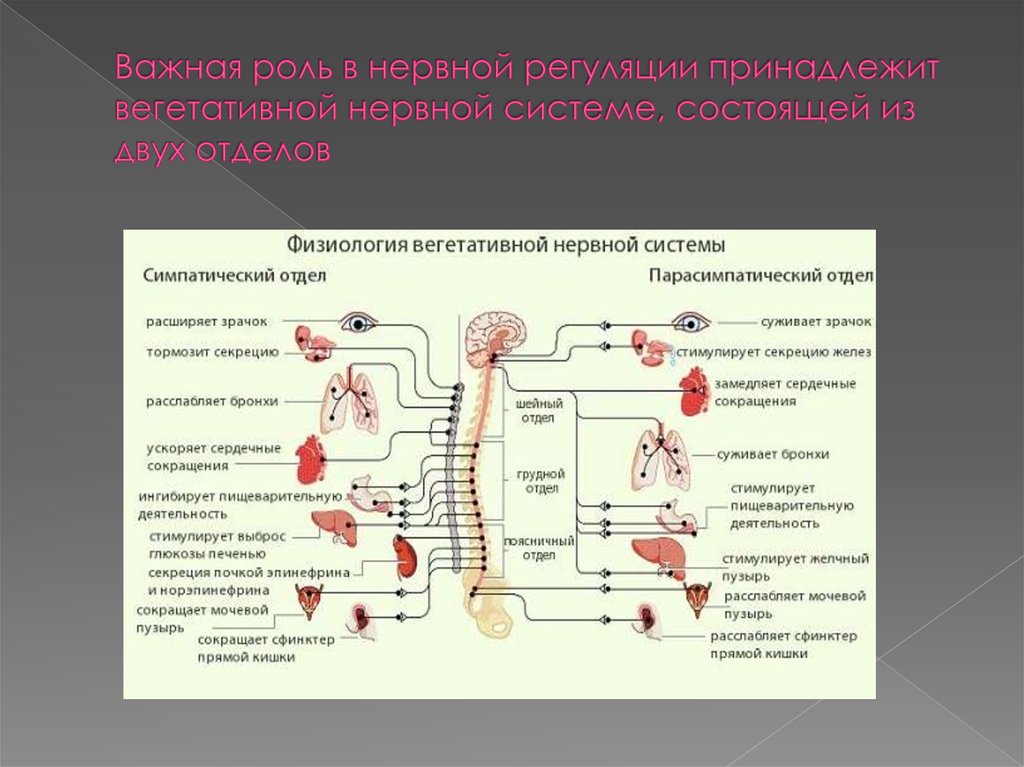 Таким образом, заданная температура в основном зависит от активности теплочувствительных нейронов POAH. Краткосрочные эффекты активности как чувствительных к теплу, так и холодочувствительных нейронов на температуру тела возникают в результате изменений вегетативного тонуса кожных артериол и, следовательно, объема кожного кровотока. Изменения симпатического оттока к потовым железам и жировой ткани обеспечивают дополнительные мишени, используемые для рассеивания и генерации тепла. Долгосрочные эффекты этих групп нейронов в ответ на устойчивые изменения температуры окружающей среды включают индукцию поведенческих и нейроэндокринных реакций на изменения температуры окружающей среды.
Таким образом, заданная температура в основном зависит от активности теплочувствительных нейронов POAH. Краткосрочные эффекты активности как чувствительных к теплу, так и холодочувствительных нейронов на температуру тела возникают в результате изменений вегетативного тонуса кожных артериол и, следовательно, объема кожного кровотока. Изменения симпатического оттока к потовым железам и жировой ткани обеспечивают дополнительные мишени, используемые для рассеивания и генерации тепла. Долгосрочные эффекты этих групп нейронов в ответ на устойчивые изменения температуры окружающей среды включают индукцию поведенческих и нейроэндокринных реакций на изменения температуры окружающей среды.
Механизм изменения заданной температуры тела во время лихорадки. Щелкайте по восьмиугольникам.
3.8 Нарушения терморегуляции Приведенное выше утверждение хорошо подчеркивает тот факт, что лихорадка была бедствием, с которым врачи боролись с древних времен. Однако недавно было признано, что лихорадка фактически является лишь одним из созвездия физиологических адаптаций, происходящих во время инфекции, называемых «болезнью» или «острой фазой реакции». Болезненная реакция включает в себя поведенческие, когнитивные, метаболические и нейроэндокринные адаптации, которые направлены на то, чтобы сделать организм менее восприимчивым к патогенам и в наибольшей степени ориентированным на оптимизацию иммунологической защиты. Таким образом, лихорадка инициируется тем, что большинство бактерий плохо размножаются при температуре выше 39°С.градусов, тогда как функция лимфоидных клеток оптимальна при этой температуре. Лихорадка начинается во время инфекции после активации макрофагов и последующего синтеза и высвобождения эндогенных пирогенных веществ, включая интерлейкин-1 (ИЛ-1), фактор некроза опухоли (ФНО), интерлейкин-6 (ИЛ-6) и интерфероны.
Приведенное выше утверждение хорошо подчеркивает тот факт, что лихорадка была бедствием, с которым врачи боролись с древних времен. Однако недавно было признано, что лихорадка фактически является лишь одним из созвездия физиологических адаптаций, происходящих во время инфекции, называемых «болезнью» или «острой фазой реакции». Болезненная реакция включает в себя поведенческие, когнитивные, метаболические и нейроэндокринные адаптации, которые направлены на то, чтобы сделать организм менее восприимчивым к патогенам и в наибольшей степени ориентированным на оптимизацию иммунологической защиты. Таким образом, лихорадка инициируется тем, что большинство бактерий плохо размножаются при температуре выше 39°С.градусов, тогда как функция лимфоидных клеток оптимальна при этой температуре. Лихорадка начинается во время инфекции после активации макрофагов и последующего синтеза и высвобождения эндогенных пирогенных веществ, включая интерлейкин-1 (ИЛ-1), фактор некроза опухоли (ФНО), интерлейкин-6 (ИЛ-6) и интерфероны. ИФН). Эти пирогены попадают в кровоток и оказывают свое действие на ЦНС в сосудистом органе терминальной пластинки (OVLT). Как обсуждалось в предыдущем разделе, OVLT является одним из нескольких участков в ЦНС, где гематоэнцефалический барьер относительно проницаем и, таким образом, позволяет мозгу «пробовать» внутреннюю среду тела. Эндотелиальные клетки OVLT имеют рецепторы эндогенных пирогенов, которые при активации вызывают как синтез, так и высвобождение в ЦНС простаноидов, в частности, простагландина Е2 (PGE2), а также синтез и высвобождение в ЦНС ИЛ-1, ИЛ-6, ФНО и ИФН. PGE2 получает доступ к чувствительным к теплу клеткам POAH, непосредственно прилегающим к OVLT, где он связывается с поверхностными рецепторами и вызывает повышение клеточных уровней циклического АМФ. Повышенный уровень цАМФ активирует систему протеинкиназы А, что приводит к снижению возбудимости теплочувствительных нейронов и снижению скорости их разряда. Это позволяет увеличить скорость разряда чувствительных к холоду нейронов, тем самым устанавливая новую, более высокую заданную температуру.
ИФН). Эти пирогены попадают в кровоток и оказывают свое действие на ЦНС в сосудистом органе терминальной пластинки (OVLT). Как обсуждалось в предыдущем разделе, OVLT является одним из нескольких участков в ЦНС, где гематоэнцефалический барьер относительно проницаем и, таким образом, позволяет мозгу «пробовать» внутреннюю среду тела. Эндотелиальные клетки OVLT имеют рецепторы эндогенных пирогенов, которые при активации вызывают как синтез, так и высвобождение в ЦНС простаноидов, в частности, простагландина Е2 (PGE2), а также синтез и высвобождение в ЦНС ИЛ-1, ИЛ-6, ФНО и ИФН. PGE2 получает доступ к чувствительным к теплу клеткам POAH, непосредственно прилегающим к OVLT, где он связывается с поверхностными рецепторами и вызывает повышение клеточных уровней циклического АМФ. Повышенный уровень цАМФ активирует систему протеинкиназы А, что приводит к снижению возбудимости теплочувствительных нейронов и снижению скорости их разряда. Это позволяет увеличить скорость разряда чувствительных к холоду нейронов, тем самым устанавливая новую, более высокую заданную температуру. Использование жаропонижающих средств, таких как аспирин и индометацин, противодействует лихорадке, прерывая синтез PGE2 за счет антагонизма ферментной системы циклооксигеназы в эндотелии OVLT.
Использование жаропонижающих средств, таких как аспирин и индометацин, противодействует лихорадке, прерывая синтез PGE2 за счет антагонизма ферментной системы циклооксигеназы в эндотелии OVLT.
— Уильям Ослер
Механизм изменения заданной температуры тела во время лихорадки
Тепловой удар. Длительное воздействие или перенапряжение в очень теплой среде может привести к чрезмерной потере жидкости и электролитов, что может привести к мышечным судорогам, головокружению, рвоте и обмороку. В экстремальных условиях может развиться гипотензия. Однако тепловое истощение отличается от теплового удара тем, что заданная температура тела остается хорошо регулируемой, а механизмы, обеспечивающие рассеивание тепла, не повреждены. Таким образом, кожа прохладная и влажная, а температура тела нормальная или несколько ниже нормальной. Отдых и замена жидкостей и электролитов быстро устраняют это состояние.
Таким образом, кожа прохладная и влажная, а температура тела нормальная или несколько ниже нормальной. Отдых и замена жидкостей и электролитов быстро устраняют это состояние. Может возникнуть острая олигурическая почечная недостаточность. Развитие комы и синдрома диссеминированного внутрисосудистого свертывания крови являются очень плохими прогностическими факторами.
Может возникнуть острая олигурическая почечная недостаточность. Развитие комы и синдрома диссеминированного внутрисосудистого свертывания крови являются очень плохими прогностическими факторами.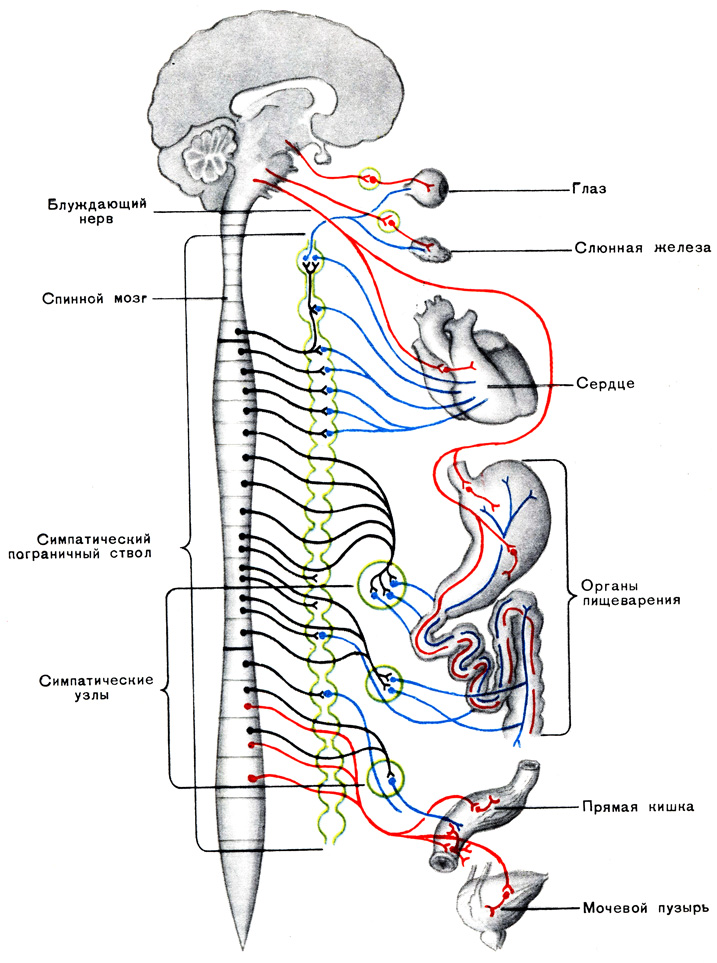 У некоторых пациентов наблюдается повышенный уровень креатининфосфокиназы, но у большинства он остается нормальным между приступами. Биопсия мышц покажет аномальное сокращение при воздействии кофеина или газового анестетика, но это, очевидно, неуклюжий способ скрининга состояния. Тщательный сбор анамнеза хирургических осложнений у родственников и выявление других сопутствующих состояний является лучшим способом выявления и предотвращения злокачественной гипертермии. Возникновение требует неотложной медицинской помощи и требует немедленного введения протокола лечения, предписанного Американским обществом анестезиологов. Операция и газовая анестезия прекращаются, все трубки от анестезиологических устройств заменяются, и начинается внешнее охлаждение. Дают стопроцентный кислород, 1-2 мг/кг бикарбоната натрия и 1 мг/кг дантролена натрия. Лекарства от сердечной аритмии назначаются по мере необходимости.
У некоторых пациентов наблюдается повышенный уровень креатининфосфокиназы, но у большинства он остается нормальным между приступами. Биопсия мышц покажет аномальное сокращение при воздействии кофеина или газового анестетика, но это, очевидно, неуклюжий способ скрининга состояния. Тщательный сбор анамнеза хирургических осложнений у родственников и выявление других сопутствующих состояний является лучшим способом выявления и предотвращения злокачественной гипертермии. Возникновение требует неотложной медицинской помощи и требует немедленного введения протокола лечения, предписанного Американским обществом анестезиологов. Операция и газовая анестезия прекращаются, все трубки от анестезиологических устройств заменяются, и начинается внешнее охлаждение. Дают стопроцентный кислород, 1-2 мг/кг бикарбоната натрия и 1 мг/кг дантролена натрия. Лекарства от сердечной аритмии назначаются по мере необходимости.  7
7
Аварийная терморегуляция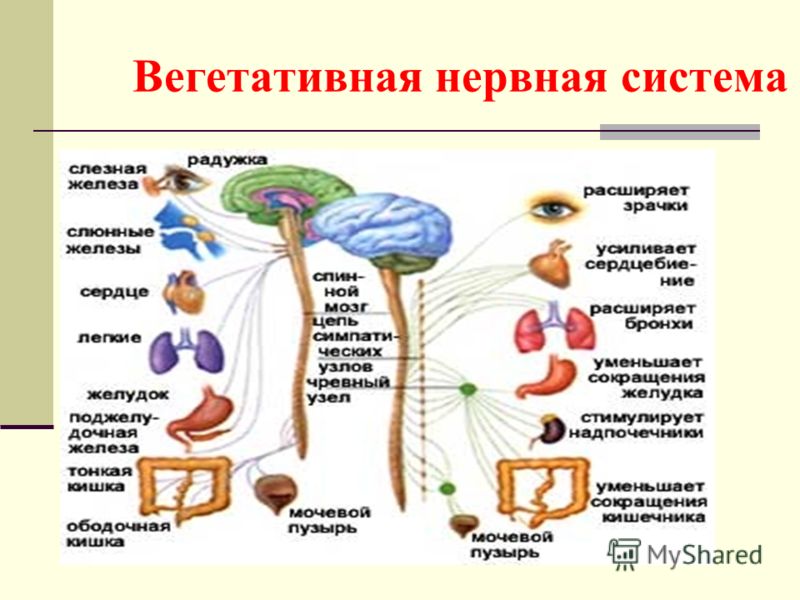 Лечение требует восстановления проходимости дыхательных путей и подачи кислорода. Объем крови можно увеличить с помощью подогретой глюкозы, в то время как газы крови и сердечный ритм тщательно контролируются. Внешнее согревание применяется только к грудной клетке, чтобы конечности оставались суженными, чтобы предотвратить резкое падение артериального давления.
Лечение требует восстановления проходимости дыхательных путей и подачи кислорода. Объем крови можно увеличить с помощью подогретой глюкозы, в то время как газы крови и сердечный ритм тщательно контролируются. Внешнее согревание применяется только к грудной клетке, чтобы конечности оставались суженными, чтобы предотвратить резкое падение артериального давления.  Терморегуляция в основном является функцией теплочувствительных нейронов преоптического переднего гипоталамуса, которые непосредственно контролируют рассеивание тепла.
Терморегуляция в основном является функцией теплочувствительных нейронов преоптического переднего гипоталамуса, которые непосредственно контролируют рассеивание тепла. переднее ядро
переднее ядро  перивентрикулярное ядро
перивентрикулярное ядро
9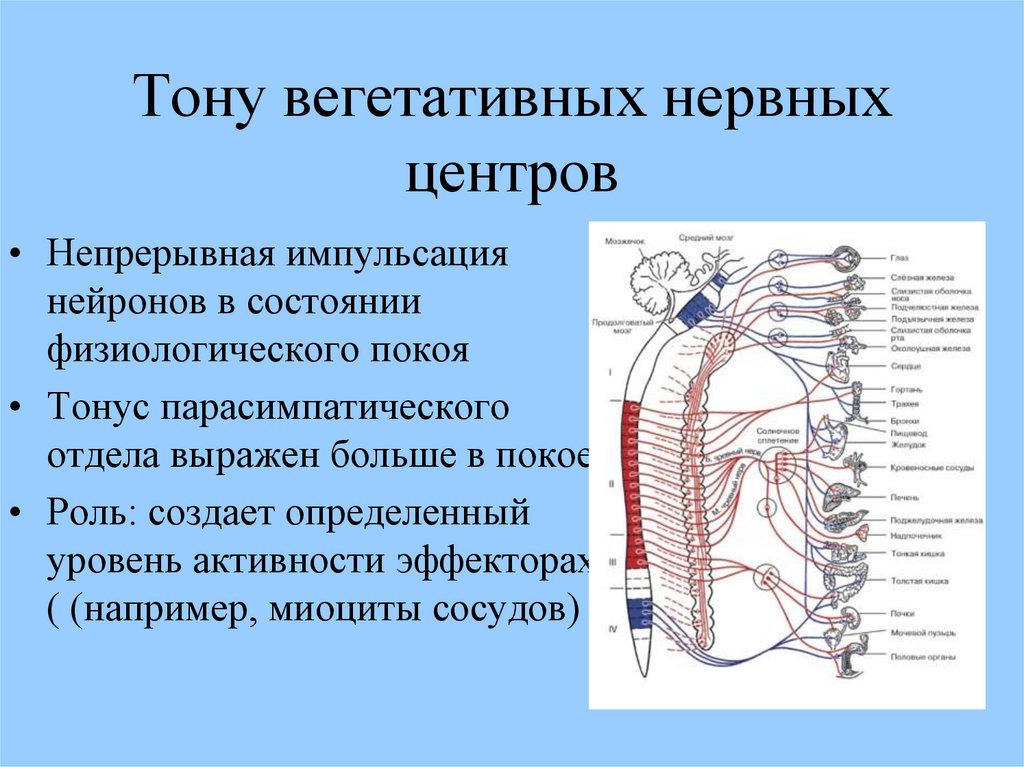 заднее ядро
заднее ядро 9
 вентромедиальное ядро Это НЕВЕРНЫЙ ответ.
вентромедиальное ядро Это НЕВЕРНЫЙ ответ.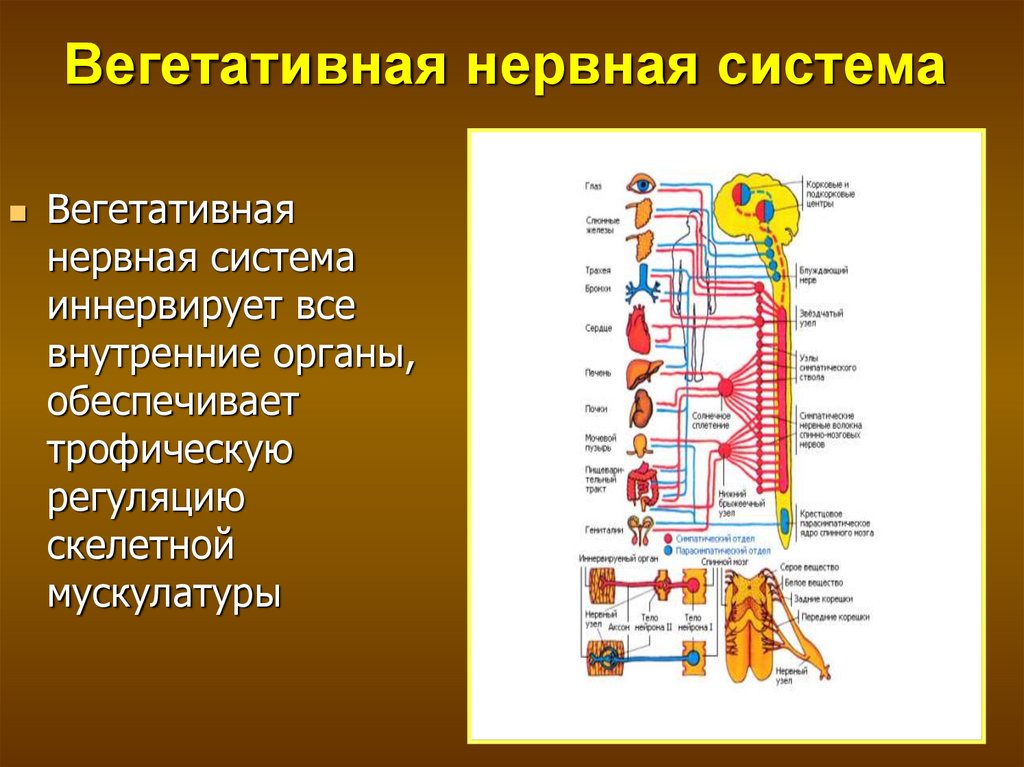 дугообразное ядро Этот ответ НЕВЕРЕН.
дугообразное ядро Этот ответ НЕВЕРЕН.  преоптическое переднее ядро Это ПРАВИЛЬНЫЙ ответ!
преоптическое переднее ядро Это ПРАВИЛЬНЫЙ ответ!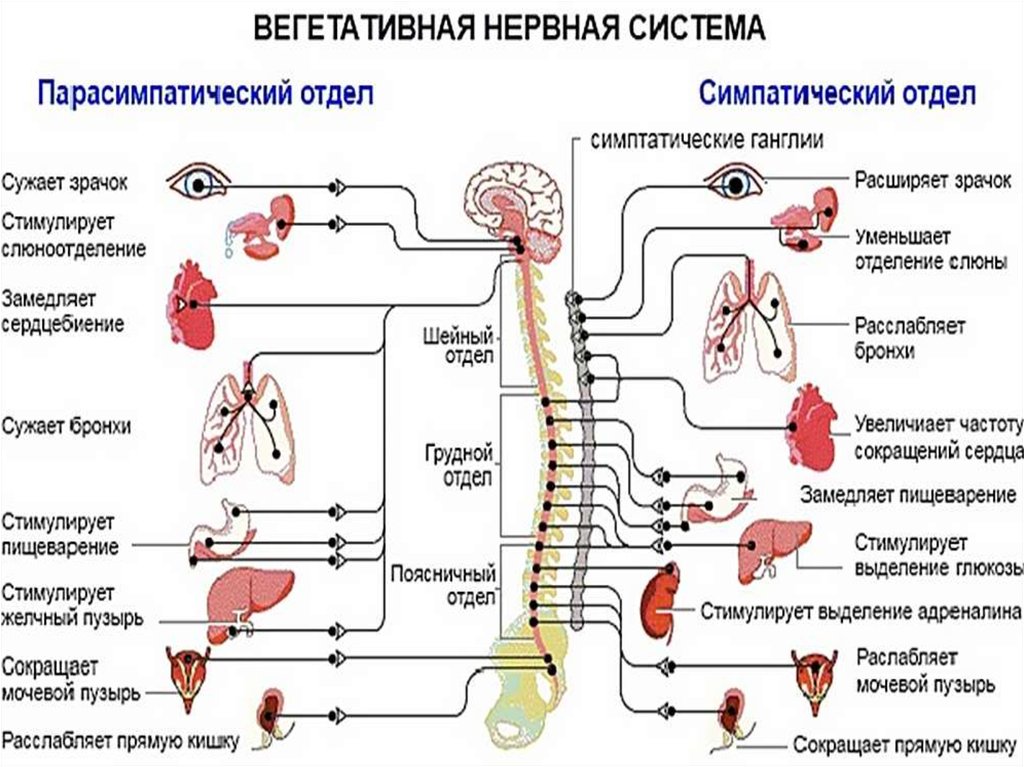 заднее ядро
заднее ядро 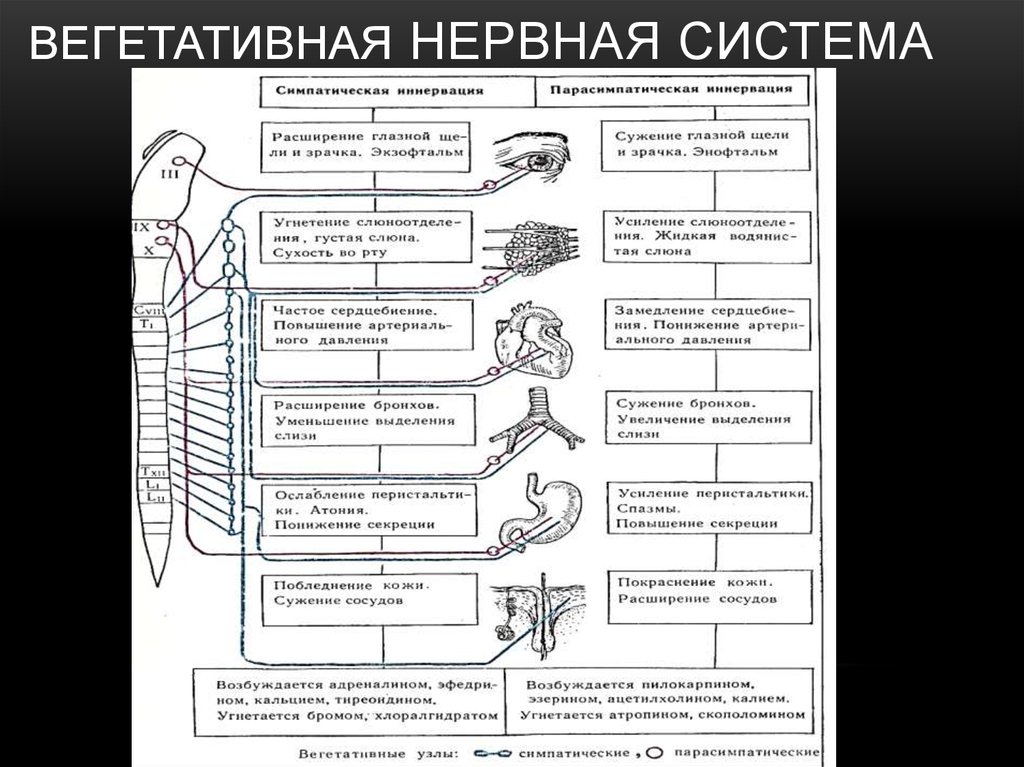 преоптическое переднее ядро
преоптическое переднее ядро  медиальный пучок переднего мозга
медиальный пучок переднего мозга спино-гипоталамический тракт
спино-гипоталамический тракт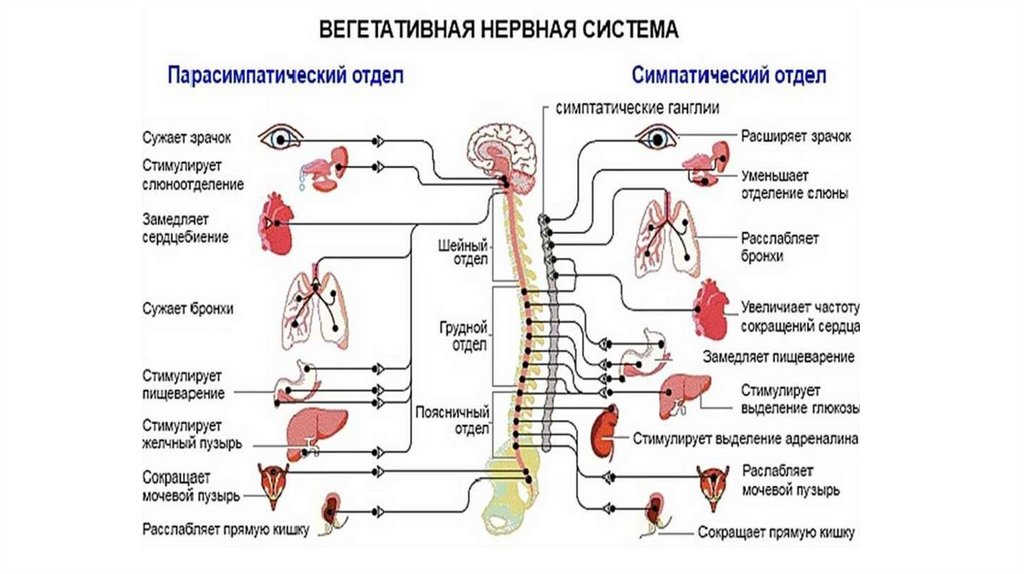 терминальная полоска
терминальная полоска 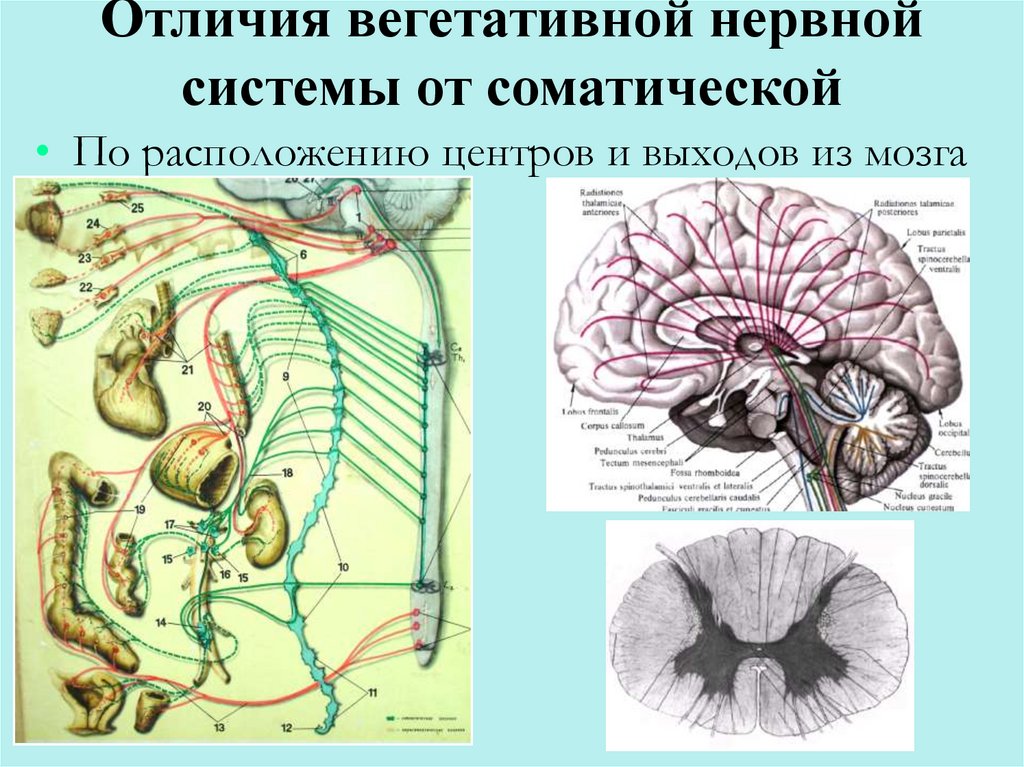
 Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла.
Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла.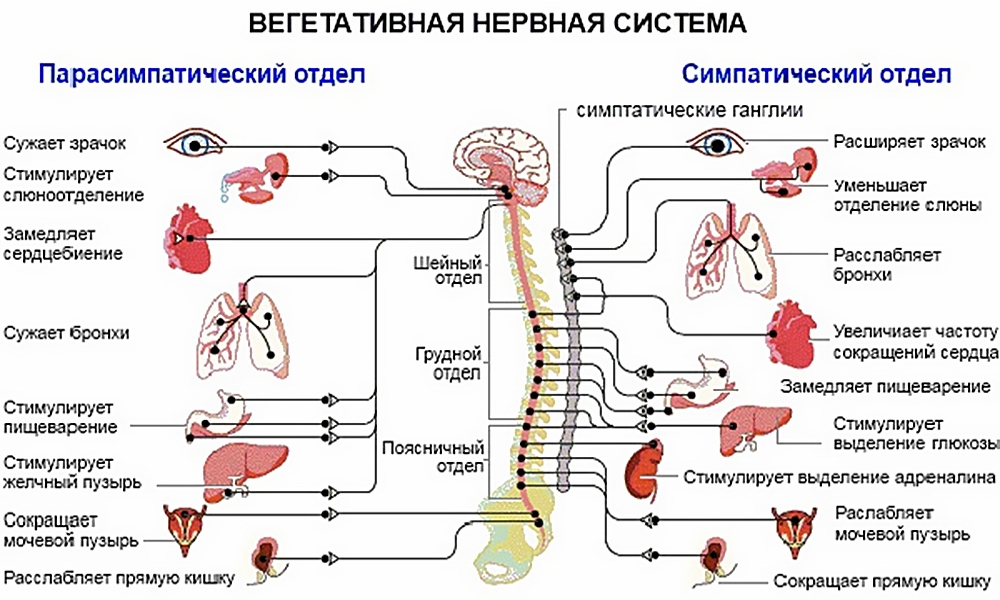 Этот ответ ПРАВИЛЬНЫЙ!
Этот ответ ПРАВИЛЬНЫЙ!  Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла.
Нейроны, чувствительные к холоду, ингибируются IL-1 и уменьшают потерю тепла. ЭКСПЛУАТАЦИЯ АВТОМИЧЕСКОЙ НЕРЕВОЙ СИСТЕМЫ У пациентов с гипертонией и сбытом: роли и терапевтические последствия | Сердечно-сосудистая диабетология
Abstract
 Вегетативная нервная система вовлечена в патофизиологию гипертензии, и были разработаны методы лечения, нацеленные на симпатическую нервную систему (СНС), ключевой компонент вегетативной нервной системы; однако текущие рекомендации содержат мало указаний по их использованию. В этом обзоре обсуждается этиология артериальной гипертензии и, в частности, роль СНС в патофизиологии артериальной гипертензии и связанных с ней заболеваний. Кроме того, изучается влияние современных антигипертензивных стратегий, включая фармакотерапию, на СНС, с акцентом на агонисты имидазолиновых рецепторов.
Вегетативная нервная система вовлечена в патофизиологию гипертензии, и были разработаны методы лечения, нацеленные на симпатическую нервную систему (СНС), ключевой компонент вегетативной нервной системы; однако текущие рекомендации содержат мало указаний по их использованию. В этом обзоре обсуждается этиология артериальной гипертензии и, в частности, роль СНС в патофизиологии артериальной гипертензии и связанных с ней заболеваний. Кроме того, изучается влияние современных антигипертензивных стратегий, включая фармакотерапию, на СНС, с акцентом на агонисты имидазолиновых рецепторов. Введение
 Артериальная гипертензия часто сочетается с другими факторами риска сердечно-сосудистых заболеваний, такими как сахарный диабет, дислипидемия/гиперхолестеринемия, ожирение и хроническая болезнь почек [1, 3, 4]. Несмотря на несколько действий, направленных на улучшение диагностики, лечения и осведомленности о гипертонии, заболеваемость и распространенность все еще растут [5, 6]. Распространенность артериальной гипертензии выше в странах с низким и средним уровнем дохода [5] и увеличивается с возрастом [1].
Артериальная гипертензия часто сочетается с другими факторами риска сердечно-сосудистых заболеваний, такими как сахарный диабет, дислипидемия/гиперхолестеринемия, ожирение и хроническая болезнь почек [1, 3, 4]. Несмотря на несколько действий, направленных на улучшение диагностики, лечения и осведомленности о гипертонии, заболеваемость и распространенность все еще растут [5, 6]. Распространенность артериальной гипертензии выше в странах с низким и средним уровнем дохода [5] и увеличивается с возрастом [1].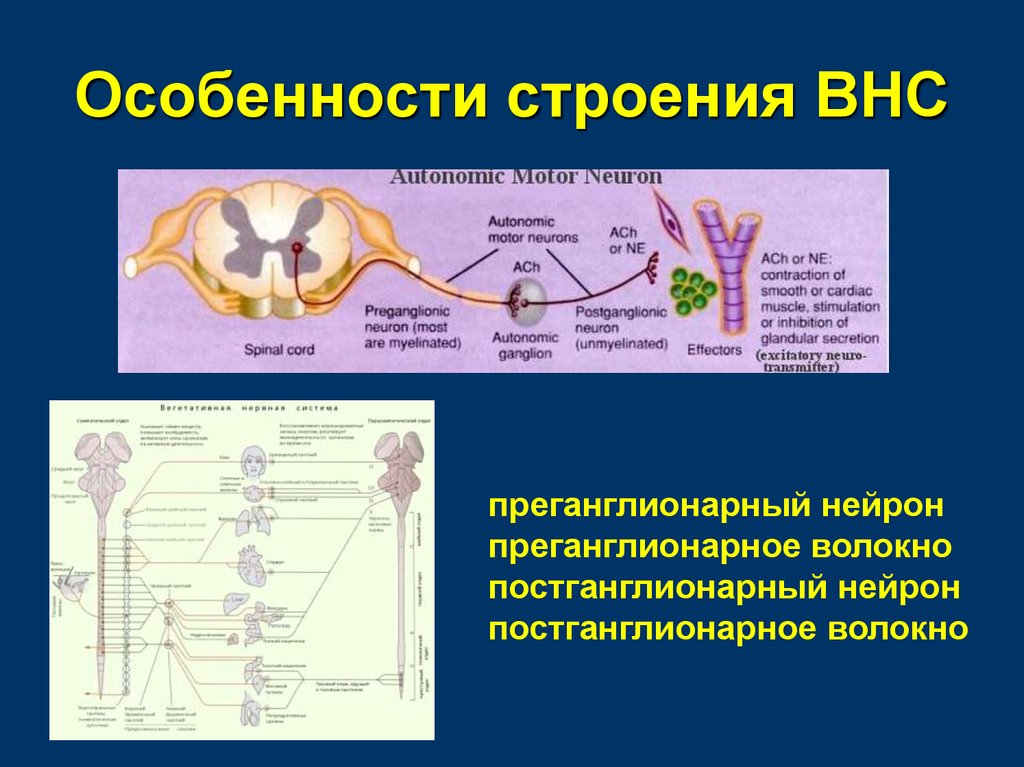 Поиск в PubMed проводился с использованием таких поисковых терминов, как «гипертония», «артериальное давление», «симпатическая нервная система» и «СНС», без ограничений по дате публикации. При необходимости проводился дополнительный целенаправленный специальный поиск.
Поиск в PubMed проводился с использованием таких поисковых терминов, как «гипертония», «артериальное давление», «симпатическая нервная система» и «СНС», без ограничений по дате публикации. При необходимости проводился дополнительный целенаправленный специальный поиск. Артериальная гипертензия
 Кроме того, в патогенезе АГ принимают участие генетические факторы и активация нейрогормональных систем. Нейрогормональная система отвечает за поддержание сердечно-сосудистого гомеостаза, при этом симпатическая нервная система (СНС) и ренин-ангиотензин-альдостероновая система (РААС) являются двумя ключевыми компонентами [14]. РААС участвует в поддержании артериального давления, концентрации натрия в плазме и внеклеточного объема и необходима для работы сердца и почек. Дисфункция РААС может привести к развитию хронических заболеваний, таких как артериальная гипертензия или сердечная недостаточность [15, 16].
Кроме того, в патогенезе АГ принимают участие генетические факторы и активация нейрогормональных систем. Нейрогормональная система отвечает за поддержание сердечно-сосудистого гомеостаза, при этом симпатическая нервная система (СНС) и ренин-ангиотензин-альдостероновая система (РААС) являются двумя ключевыми компонентами [14]. РААС участвует в поддержании артериального давления, концентрации натрия в плазме и внеклеточного объема и необходима для работы сердца и почек. Дисфункция РААС может привести к развитию хронических заболеваний, таких как артериальная гипертензия или сердечная недостаточность [15, 16]. Симпатическая нервная система
Физиологическая роль симпатической нервной системы
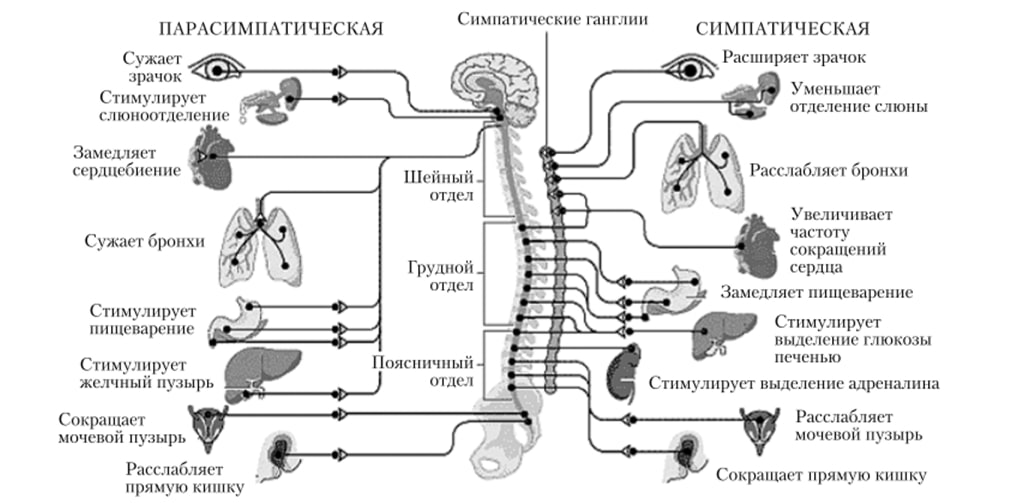 При нормальном функционировании вегетативная нервная система, включающая симпатическую, парасимпатическую и энтеральную нервные системы, бессознательно регулирует региональный кровоток и сердечный выброс и координирует свои действия с центральной дыхательной сетью, чтобы реагировать на различные метаболические и терморегуляторные потребности [19].]. СНС активируется, когда барорецепторы, специализированные рецепторы растяжения, расположенные в тонких участках кровеносных сосудов и камер сердца, ощущают изменения давления [20]. При падении артериального давления немедленно активируется СНС, что приводит к увеличению сердечного выброса и вазоконстрикции периферических сосудов (рис. 1) [20]. Последующее сужение почечных афферентных артериол приводит к активации ренин-ангиотензин-альдостероновой системы и секреции ренина [14].
При нормальном функционировании вегетативная нервная система, включающая симпатическую, парасимпатическую и энтеральную нервные системы, бессознательно регулирует региональный кровоток и сердечный выброс и координирует свои действия с центральной дыхательной сетью, чтобы реагировать на различные метаболические и терморегуляторные потребности [19].]. СНС активируется, когда барорецепторы, специализированные рецепторы растяжения, расположенные в тонких участках кровеносных сосудов и камер сердца, ощущают изменения давления [20]. При падении артериального давления немедленно активируется СНС, что приводит к увеличению сердечного выброса и вазоконстрикции периферических сосудов (рис. 1) [20]. Последующее сужение почечных афферентных артериол приводит к активации ренин-ангиотензин-альдостероновой системы и секреции ренина [14]. В целом, СНС увеличивает выработку глюкозы печенью и мобилизует метаболическое топливо для использования тканями [21]. В поджелудочной железе островки Лангерганса иннервируются волокнами вегетативной нервной системы, что приводит к модуляции секреции инсулина парасимпатическими нервами, стимулирующими секрецию инсулина, и симпатическими нервами, имеющими противоположный эффект [22, 23]. Усиленный липолиз в жировой ткани с помощью СНС является частью механизма контроля, предназначенного для расщепления жиров [24].
В целом, СНС увеличивает выработку глюкозы печенью и мобилизует метаболическое топливо для использования тканями [21]. В поджелудочной железе островки Лангерганса иннервируются волокнами вегетативной нервной системы, что приводит к модуляции секреции инсулина парасимпатическими нервами, стимулирующими секрецию инсулина, и симпатическими нервами, имеющими противоположный эффект [22, 23]. Усиленный липолиз в жировой ткани с помощью СНС является частью механизма контроля, предназначенного для расщепления жиров [24]. Перегрузка СНС при гипертензии
 ,27,28,29]. СНС также влияет на гемостаз, при этом острая активация СНС приводит к гиперкоагуляции из-за повышенной агрегации тромбоцитов [29, 30].
,27,28,29]. СНС также влияет на гемостаз, при этом острая активация СНС приводит к гиперкоагуляции из-за повышенной агрегации тромбоцитов [29, 30].
 И наоборот, свободные жирные кислоты могут усиливать симпатическую активность [33]. Если симпатическая активность хронически повышена, это может привести к развитию инсулинорезистентности и артериальной гипертензии, увеличивая риск сердечно-сосудистых заболеваний. Роль терапевтического ингибирования симпатической перегрузки в предотвращении метаболических нарушений и связанных с ними неблагоприятных исходов требует адекватного тестирования в рандомизированных контролируемых исследованиях соответствующего размера [8, 21, 24, 31, 34, 35, 36, 37, 38].
И наоборот, свободные жирные кислоты могут усиливать симпатическую активность [33]. Если симпатическая активность хронически повышена, это может привести к развитию инсулинорезистентности и артериальной гипертензии, увеличивая риск сердечно-сосудистых заболеваний. Роль терапевтического ингибирования симпатической перегрузки в предотвращении метаболических нарушений и связанных с ними неблагоприятных исходов требует адекватного тестирования в рандомизированных контролируемых исследованиях соответствующего размера [8, 21, 24, 31, 34, 35, 36, 37, 38].
Ожирение, гипертензия, связанная с ожирением, и перегрузка СНС
 В частности, было показано, что активность СНС коррелирует с висцеральным ожирением [46]. Такая перегрузка СНС может способствовать метаболическим нарушениям в виде инсулинорезистентности с последующей гиперинсулинемией, нарушением метаболизма глюкозы, сахарным диабетом, дислипидемией [47, 48]. Ожирение также часто связано с резистентной гипертензией, характеризующейся неспособностью контролировать артериальное давление, несмотря на назначение как минимум трех антигипертензивных средств, включая диуретик [48].
В частности, было показано, что активность СНС коррелирует с висцеральным ожирением [46]. Такая перегрузка СНС может способствовать метаболическим нарушениям в виде инсулинорезистентности с последующей гиперинсулинемией, нарушением метаболизма глюкозы, сахарным диабетом, дислипидемией [47, 48]. Ожирение также часто связано с резистентной гипертензией, характеризующейся неспособностью контролировать артериальное давление, несмотря на назначение как минимум трех антигипертензивных средств, включая диуретик [48].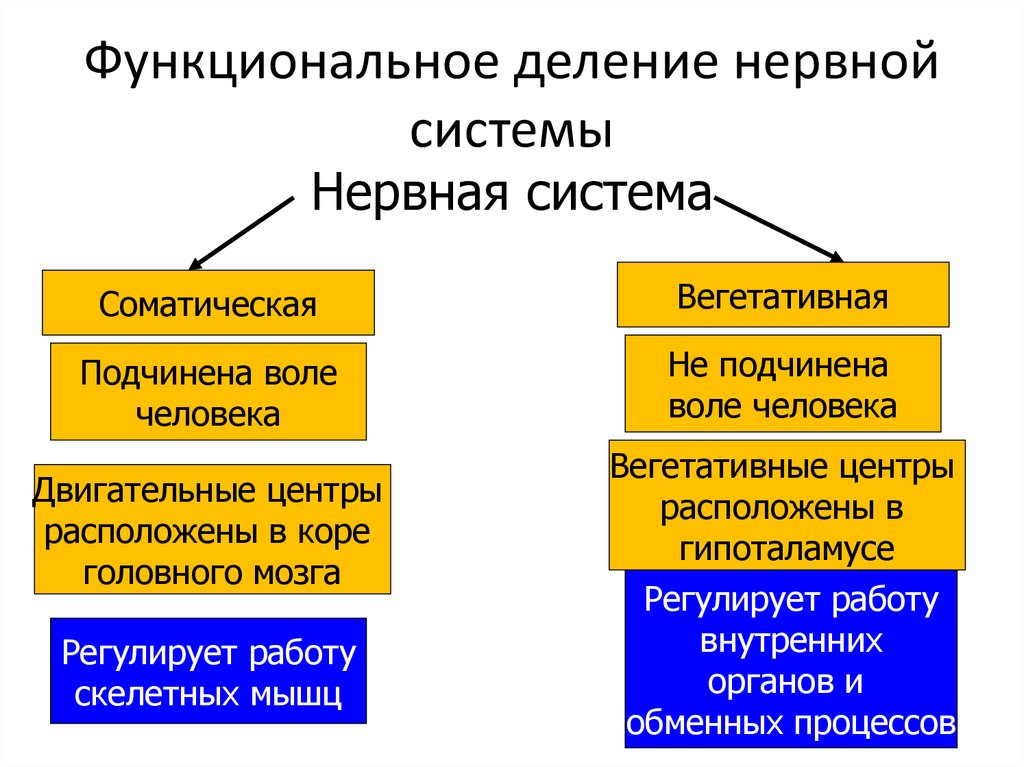 52], а также более низкий вазоконстрикторный ответ на симпатическую активацию во время вдоха [53]. Такой притупленный симпатический ответ или симпатический резерв может способствовать увеличению веса и усугублять резистентность к инсулину и последующую гиперинсулинемию и, таким образом, поддерживать порочный круг: увеличение веса — резистентность к инсулину — симпатическая активация с притупленным ответом — увеличение веса и т. д. Повышенная секреция лептина адипоцитами у больных с ожирением способствует развитию сосудистой и системной инсулинорезистентности и дисфункции СНС [3, 4]. Помимо того, что он является важным регулятором накопления жира, приема пищи, нейроэндокринного оттока и обмена веществ, лептин, гормон адипоцитов, играет роль в развитии гипертензии за счет повышения активности СНС в тканях, участвующих в сердечно-сосудистой регуляции, таких как почки и кровеносные сосуды [54, 55]. Лептин играет ключевую роль в регуляции расхода энергии через СНС, поскольку он нацелен на аркуатное ядро для активации соответствующих сигнальных путей [47].
52], а также более низкий вазоконстрикторный ответ на симпатическую активацию во время вдоха [53]. Такой притупленный симпатический ответ или симпатический резерв может способствовать увеличению веса и усугублять резистентность к инсулину и последующую гиперинсулинемию и, таким образом, поддерживать порочный круг: увеличение веса — резистентность к инсулину — симпатическая активация с притупленным ответом — увеличение веса и т. д. Повышенная секреция лептина адипоцитами у больных с ожирением способствует развитию сосудистой и системной инсулинорезистентности и дисфункции СНС [3, 4]. Помимо того, что он является важным регулятором накопления жира, приема пищи, нейроэндокринного оттока и обмена веществ, лептин, гормон адипоцитов, играет роль в развитии гипертензии за счет повышения активности СНС в тканях, участвующих в сердечно-сосудистой регуляции, таких как почки и кровеносные сосуды [54, 55]. Лептин играет ключевую роль в регуляции расхода энергии через СНС, поскольку он нацелен на аркуатное ядро для активации соответствующих сигнальных путей [47]. Нарушение секреции адипонектина у пациентов с ожирением также считается вовлеченным в активацию СНС и развитие резистентности к инсулину [4]. Кроме того, сообщалось об индуцированном инсулином ингибировании липолиза у пациентов с ожирением и диабетом 2 типа после модулирования активности СНС [37]. Результаты исследований на животных и людях позволяют предположить, что центральная симпатическая гиперактивность участвует в этиологии и осложнениях метаболического синдрома и связанных с ним компонентов (например, абдоминального ожирения, резистентности к инсулину, гипергликемии, дислипидемии, гипертонии, системного воспаления) [43].
Нарушение секреции адипонектина у пациентов с ожирением также считается вовлеченным в активацию СНС и развитие резистентности к инсулину [4]. Кроме того, сообщалось об индуцированном инсулином ингибировании липолиза у пациентов с ожирением и диабетом 2 типа после модулирования активности СНС [37]. Результаты исследований на животных и людях позволяют предположить, что центральная симпатическая гиперактивность участвует в этиологии и осложнениях метаболического синдрома и связанных с ним компонентов (например, абдоминального ожирения, резистентности к инсулину, гипергликемии, дислипидемии, гипертонии, системного воспаления) [43]. Считается, что эти изменения опосредованы повышенным уровнем лептина в сыворотке из-за увеличения жировой массы в сочетании с селективной резистентностью к лептину [55]. Имеются данные о том, что снижение массы тела, вызванное изменением образа жизни, может улучшить липидный профиль, метаболизм глюкозы, чувствительность к инсулину и привести к снижению систолического и диастолического артериального давления [61]. Также было показано, что некоторые специализированные диеты снижают симпатическую активность и улучшают барорефлекс и чувствительность к инсулину [61]. Кроме того, активность как СНС, так и парасимпатической нервной системы (ПНС) улучшается, когда диетические меры сочетаются с физическими упражнениями [62]. Тем не менее, для пациентов с гипертонией, связанной с ожирением (OHT), диетические меры недостаточны для контроля артериального давления, и необходимо применять фармакологические стратегии [48].
Считается, что эти изменения опосредованы повышенным уровнем лептина в сыворотке из-за увеличения жировой массы в сочетании с селективной резистентностью к лептину [55]. Имеются данные о том, что снижение массы тела, вызванное изменением образа жизни, может улучшить липидный профиль, метаболизм глюкозы, чувствительность к инсулину и привести к снижению систолического и диастолического артериального давления [61]. Также было показано, что некоторые специализированные диеты снижают симпатическую активность и улучшают барорефлекс и чувствительность к инсулину [61]. Кроме того, активность как СНС, так и парасимпатической нервной системы (ПНС) улучшается, когда диетические меры сочетаются с физическими упражнениями [62]. Тем не менее, для пациентов с гипертонией, связанной с ожирением (OHT), диетические меры недостаточны для контроля артериального давления, и необходимо применять фармакологические стратегии [48]. Симпатический перегруз у пациентов с ОГТ часто усиливается у пациентов с синдромом апноэ во сне. Лептин, инсулин и РААС могут способствовать повышению активности СНС. Действительно, клэмп-исследования у здоровых людей и лиц с ожирением показали, что гиперинсулинемия может активировать СНС и снижать активность ПНС [63, 64] и, таким образом, может способствовать ОГТ, а гиперинсулинемия и неадекватная активация СНС способствуют увеличению реабсорбции натрия в почках [4]. Кроме того, при инсулинорезистентности также наблюдается резистентность сосудов к сосудорасширяющему действию инсулина, что способствует развитию артериальной гипертензии [64]. Точно так же эндотелиальная дисфункция, связанная с ожирением, может нарушать сосудорасширяющий эффект лептина, а также способствовать гипертонии [65] (рис. 2).
Симпатический перегруз у пациентов с ОГТ часто усиливается у пациентов с синдромом апноэ во сне. Лептин, инсулин и РААС могут способствовать повышению активности СНС. Действительно, клэмп-исследования у здоровых людей и лиц с ожирением показали, что гиперинсулинемия может активировать СНС и снижать активность ПНС [63, 64] и, таким образом, может способствовать ОГТ, а гиперинсулинемия и неадекватная активация СНС способствуют увеличению реабсорбции натрия в почках [4]. Кроме того, при инсулинорезистентности также наблюдается резистентность сосудов к сосудорасширяющему действию инсулина, что способствует развитию артериальной гипертензии [64]. Точно так же эндотелиальная дисфункция, связанная с ожирением, может нарушать сосудорасширяющий эффект лептина, а также способствовать гипертонии [65] (рис. 2). . Действительно, у крыс с поражением вентромедиального гипоталамуса гипертония не наблюдается, несмотря на массивное ожирение, повышенный уровень катехоламинов в плазме и нормальную бета-адренорецепторов сердца. В этой модели предполагалось, что повышенный тонус блуждающего нерва защищает от развития гипертонии [67].
. Действительно, у крыс с поражением вентромедиального гипоталамуса гипертония не наблюдается, несмотря на массивное ожирение, повышенный уровень катехоламинов в плазме и нормальную бета-адренорецепторов сердца. В этой модели предполагалось, что повышенный тонус блуждающего нерва защищает от развития гипертонии [67]. ГПП-1 и перегрузка СНС
 Помимо гликемического контроля, ГПП-1 играет роль в контроле частоты сердечных сокращений [72, 73], при этом исследования на животных предполагают, что этот опосредованный ГПП-1 контроль частоты сердечных сокращений связан с симпатической активацией и/или подавлением парасимпатической модуляции [74]. ,75,76] и что агонисты рецептора GLP1 вызывают увеличение частоты сердечных сокращений [69].]. Кроме того, исследования на животных предполагают, что GLP-1 усиливает симпатическую активность и увеличивает термогенез бурой жировой ткани [70]. Однако при лечении агонистами рецептора GLP1 наблюдается небольшое снижение артериального давления в результате потери веса и, возможно, за счет других механизмов, включая улучшение функции эндотелия [77] .
Помимо гликемического контроля, ГПП-1 играет роль в контроле частоты сердечных сокращений [72, 73], при этом исследования на животных предполагают, что этот опосредованный ГПП-1 контроль частоты сердечных сокращений связан с симпатической активацией и/или подавлением парасимпатической модуляции [74]. ,75,76] и что агонисты рецептора GLP1 вызывают увеличение частоты сердечных сокращений [69].]. Кроме того, исследования на животных предполагают, что GLP-1 усиливает симпатическую активность и увеличивает термогенез бурой жировой ткани [70]. Однако при лечении агонистами рецептора GLP1 наблюдается небольшое снижение артериального давления в результате потери веса и, возможно, за счет других механизмов, включая улучшение функции эндотелия [77] . Апноэ во сне и перегрузка СНС
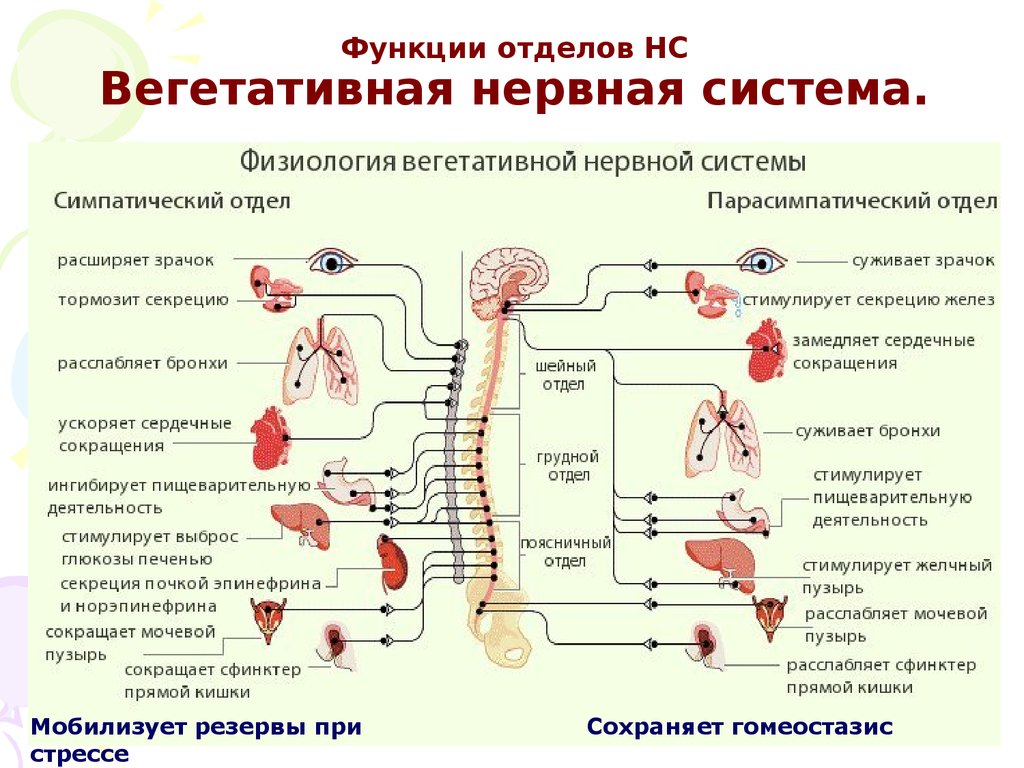 Было высказано предположение, что кардиозащитные эффекты парасимпатической активности снижаются за счет острой симпатической активации, связанной с индукцией сброса барорецепторов вниз при апноэ во сне [78]. Нарушение барорецепторных рефлексов и симпатическая гиперактивность также наблюдались при сердечной недостаточности, которая также тесно связана с апноэ во сне [79].].
Было высказано предположение, что кардиозащитные эффекты парасимпатической активности снижаются за счет острой симпатической активации, связанной с индукцией сброса барорецепторов вниз при апноэ во сне [78]. Нарушение барорецепторных рефлексов и симпатическая гиперактивность также наблюдались при сердечной недостаточности, которая также тесно связана с апноэ во сне [79].]. Таким образом, оправдан скрининг апноэ во сне у больных сахарным диабетом с резистентной артериальной гипертензией даже при отсутствии симптомов для оптимизации снижения артериального давления [82].
Таким образом, оправдан скрининг апноэ во сне у больных сахарным диабетом с резистентной артериальной гипертензией даже при отсутствии симптомов для оптимизации снижения артериального давления [82]. Оценка активности СНС
Микронейрография
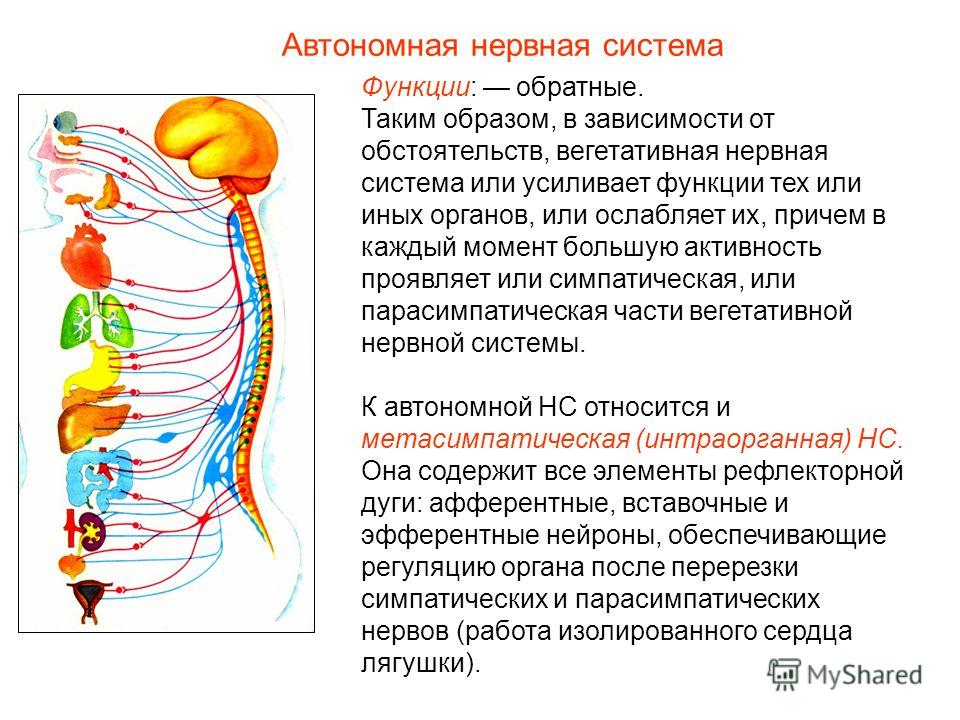
Измерения, полученные с помощью радиоактивных индикаторов
Другие методы
Вариабельность сердечного ритма
 Снижение ВСР наблюдается при гиперактивности СНС, коррелирует с повышенным риском сердечной смертности и является предиктором сердечно-сосудистых событий [40].
Снижение ВСР наблюдается при гиперактивности СНС, коррелирует с повышенным риском сердечной смертности и является предиктором сердечно-сосудистых событий [40]. Вариабельность артериального давления

Чувствительность артериального барорефлекса

Влияние стратегий лечения артериальной гипертензии на СНС
Изменение образа жизни
 Кроме того, было показано, что потеря веса снижает активность СНС, что приводит к улучшению клиренса инсулина и снижению периферического сосудистого сопротивления [38]. Центральный симпатический отток также участвует в физиологии солечувствительных изменений артериального давления [101], а высокое потребление натрия связано с парасимпатическим торможением, дислипидемией и воспалением у пациентов с легкой гипертензией [102].
Кроме того, было показано, что потеря веса снижает активность СНС, что приводит к улучшению клиренса инсулина и снижению периферического сосудистого сопротивления [38]. Центральный симпатический отток также участвует в физиологии солечувствительных изменений артериального давления [101], а высокое потребление натрия связано с парасимпатическим торможением, дислипидемией и воспалением у пациентов с легкой гипертензией [102].
Катетерная почечная денервация
 Что касается воздействия на почки, было показано, что почечная денервация снижает выброс норадреналина в почки и выброс ренина в плазму [109].]. Интересно, что недавняя статья показала, что исходная 24-часовая частота сердечных сокращений выше медианы (73,5 ударов в минуту), что свидетельствует о более высокой симпатической активности, предсказывает большее снижение АД после почечной денервации и может позволить врачам отобрать пациентов, которые, вероятно, ответят на процедуру [108]. ].
Что касается воздействия на почки, было показано, что почечная денервация снижает выброс норадреналина в почки и выброс ренина в плазму [109].]. Интересно, что недавняя статья показала, что исходная 24-часовая частота сердечных сокращений выше медианы (73,5 ударов в минуту), что свидетельствует о более высокой симпатической активности, предсказывает большее снижение АД после почечной денервации и может позволить врачам отобрать пациентов, которые, вероятно, ответят на процедуру [108]. ]. Фармакологические стратегии
 Хотя ингибиторы АПФ и БРА действуют путем антагонизма ренин-ангиотензин-альдостероновой системы, они, по-видимому, практически не влияют на СНС [110, 111].
Хотя ингибиторы АПФ и БРА действуют путем антагонизма ренин-ангиотензин-альдостероновой системы, они, по-видимому, практически не влияют на СНС [110, 111]. Бета-блокаторы
Селективные агонисты имидазолиновых рецепторов.
 Считается, что рецептор I 1 может принадлежать к семейству нейроцитокиновых рецепторов, так как его сигнальные пути сходны с таковыми у интерлейкинов [114]. Из агонистов имидазолина клонидин стимулирует как α 2 рецепторов и имидазолиновых I 1 рецепторов, тогда как моксонидин и рилменидин считаются селективными агонистами имидазолиновых рецепторов (СИРА), активирующими только имидазолиновые I 1 рецепторов в RVLM [9, 116], что позволяет избежать побочных эффектов, наблюдаемых при клонидин (в основном усталость, сонливость и седативный эффект). Повышение активности нейронов в RVLM за счет прямой стимуляции рецепторов I 1 агонистами имидазолина снижает симпатический отток, что приводит к падению артериального давления (рис. 3) [115]. я 9Рецепторы 0535 1 локализованы также на плазматической мембране нейронов мозгового вещества надпочечников, почечного эпителия, панкреатических островков, тромбоцитов и предстательной железы [114, 117].
Считается, что рецептор I 1 может принадлежать к семейству нейроцитокиновых рецепторов, так как его сигнальные пути сходны с таковыми у интерлейкинов [114]. Из агонистов имидазолина клонидин стимулирует как α 2 рецепторов и имидазолиновых I 1 рецепторов, тогда как моксонидин и рилменидин считаются селективными агонистами имидазолиновых рецепторов (СИРА), активирующими только имидазолиновые I 1 рецепторов в RVLM [9, 116], что позволяет избежать побочных эффектов, наблюдаемых при клонидин (в основном усталость, сонливость и седативный эффект). Повышение активности нейронов в RVLM за счет прямой стимуляции рецепторов I 1 агонистами имидазолина снижает симпатический отток, что приводит к падению артериального давления (рис. 3) [115]. я 9Рецепторы 0535 1 локализованы также на плазматической мембране нейронов мозгового вещества надпочечников, почечного эпителия, панкреатических островков, тромбоцитов и предстательной железы [114, 117]. В соответствии с этими выводами рилменидин продемонстрировал ингибирование симпатической активности сердечного барорефлекса с последующим снижением частоты сердечных сокращений [118], а благоприятные эффекты моксонидина включают усиление экскреции натрия, улучшение резистентности к инсулину (клэмп-исследование) [119] и толерантность к глюкозе и защита от гипертензивного повреждения органов-мишеней (например, заболевания почек, гипертрофия сердца) [120]. Было также показано, что моксонидин замедляет прогрессирование почечной недостаточности, уменьшает гипертрофию левого желудочка и улучшает функцию эндотелия (первый шаг к развитию атеросклероза) у пациентов с артериальной гипертензией [116, 120]. В исследовании MERSY [121] было показано, что прием моксонидина ежедневно (0,2–0,4 мг) в течение 6 месяцев в виде монотерапии или в сочетании с другим антигипертензивным средством у больных АГ с метаболическим синдромом улучшает контроль артериального давления, снижает массу тела и воздействовать на метаболические параметры, такие как липидные фракции и глюкоза плазмы натощак (рис.
В соответствии с этими выводами рилменидин продемонстрировал ингибирование симпатической активности сердечного барорефлекса с последующим снижением частоты сердечных сокращений [118], а благоприятные эффекты моксонидина включают усиление экскреции натрия, улучшение резистентности к инсулину (клэмп-исследование) [119] и толерантность к глюкозе и защита от гипертензивного повреждения органов-мишеней (например, заболевания почек, гипертрофия сердца) [120]. Было также показано, что моксонидин замедляет прогрессирование почечной недостаточности, уменьшает гипертрофию левого желудочка и улучшает функцию эндотелия (первый шаг к развитию атеросклероза) у пациентов с артериальной гипертензией [116, 120]. В исследовании MERSY [121] было показано, что прием моксонидина ежедневно (0,2–0,4 мг) в течение 6 месяцев в виде монотерапии или в сочетании с другим антигипертензивным средством у больных АГ с метаболическим синдромом улучшает контроль артериального давления, снижает массу тела и воздействовать на метаболические параметры, такие как липидные фракции и глюкоза плазмы натощак (рис. 4). Недавно международное реальное медицинское исследование показало, что в опрошенных странах врачи рассматривали SIRA как полезный терапевтический вариант, часто назначаемый пациентам с гипертонической болезнью с метаболическими исходами [122].
4). Недавно международное реальное медицинское исследование показало, что в опрошенных странах врачи рассматривали SIRA как полезный терапевтический вариант, часто назначаемый пациентам с гипертонической болезнью с метаболическими исходами [122]. Conclusions

Наличие данных и материалов
Сокращения
Каталожные номера
«>
 2010;30:365–401.
2010;30:365–401.
 2000;43:393–410.
2000;43:393–410. Диабет метаб. 2009; 35: 364–70.
Диабет метаб. 2009; 35: 364–70. Роль свободных жирных кислот в вегетативной нервной системе сердца у пациентов с инсулинзависимым диабетом: эффекты метаболического контроля. J Clin Endocrinol Metab. 2001;86:6.
Роль свободных жирных кислот в вегетативной нервной системе сердца у пациентов с инсулинзависимым диабетом: эффекты метаболического контроля. J Clin Endocrinol Metab. 2001;86:6. Диабет. 2017;66:823–34.
Диабет. 2017;66:823–34. М., Уилсон К.Л., Саджа Дж., Зиглер М.Г., Миллс П.Дж. Влияние на артериальное давление и функцию вегетативной нервной системы 12-недельных упражнений или упражнений в сочетании с диетой DASH у людей с повышенным артериальным давлением. Acta Physiol Oxf англ. 2011; 203:343–50.
М., Уилсон К.Л., Саджа Дж., Зиглер М.Г., Миллс П.Дж. Влияние на артериальное давление и функцию вегетативной нервной системы 12-недельных упражнений или упражнений в сочетании с диетой DASH у людей с повышенным артериальным давлением. Acta Physiol Oxf англ. 2011; 203:343–50. , Парьес Дж., Аттали Дж. Р., Валенси П. Связь между сердечной автономной невропатией и гипертонией и ее потенциальное влияние на диабетические осложнения. Diabet Med J Br Diabet Assoc. 2010; 27:804–11.
, Парьес Дж., Аттали Дж. Р., Валенси П. Связь между сердечной автономной невропатией и гипертонией и ее потенциальное влияние на диабетические осложнения. Diabet Med J Br Diabet Assoc. 2010; 27:804–11. Гипертония. 2000; 36: 538–42.
Гипертония. 2000; 36: 538–42. ;89:27–36.
;89:27–36. Hypertens Dallas Tex. 1979; 2009 (53): 473–9.
Hypertens Dallas Tex. 1979; 2009 (53): 473–9. Регул Пепт. 1996; 67: 63–8.
Регул Пепт. 1996; 67: 63–8. 2019;45:91–101.
2019;45:91–101. Оксфорд: ОУП Оксфорд; 2013.
Оксфорд: ОУП Оксфорд; 2013. Diabetes Metab Res Rev. 2011;27:654–64.
Diabetes Metab Res Rev. 2011;27:654–64. Связь между ожирением и индексами вариабельности сердечного ритма: интуиция в отношении вегетативных изменений сердца — риск сердечно-сосудистых заболеваний. Diabetes Metab Syndr Obes Targets Ther. 2017;10:57–64.
Связь между ожирением и индексами вариабельности сердечного ритма: интуиция в отношении вегетативных изменений сердца — риск сердечно-сосудистых заболеваний. Diabetes Metab Syndr Obes Targets Ther. 2017;10:57–64. и др. Оптимальное и ступенчатое стандартизированное антигипертензивное лечение с денервацией почек или без нее при резистентной гипертензии (DENERHTN): многоцентровое открытое рандомизированное контролируемое исследование. Ланцет Лонд англ. 2015;385:1957–65.
и др. Оптимальное и ступенчатое стандартизированное антигипертензивное лечение с денервацией почек или без нее при резистентной гипертензии (DENERHTN): многоцентровое открытое рандомизированное контролируемое исследование. Ланцет Лонд англ. 2015;385:1957–65. Европейское сердце J. 2019; 40: 743–51.
Европейское сердце J. 2019; 40: 743–51. Am J Physiol Heart Circ Physiol. 2006;290:h2706-1712.
Am J Physiol Heart Circ Physiol. 2006;290:h2706-1712. Ам Дж Гипертенс. 2000;13:89С-98С.
Ам Дж Гипертенс. 2000;13:89С-98С. Благодарности
Финансирование
Информация об авторе
Авторы и организации
Contributions

Автор, ответственный за переписку
Декларации этики
Одобрение этики и согласие на участие
Согласие на публикацию
Конкурирующие интересы
Дополнительная информация
Примечание издателя
Права и разрешения
 0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Related Posts


 Установлено участие мозжечка в регуляции
таких вегетативных функций, как зрачковый
рефлекс, трофика кожи (скорость заживления
ран), сокращение мышц, поднимающих
волосы.
Установлено участие мозжечка в регуляции
таких вегетативных функций, как зрачковый
рефлекс, трофика кожи (скорость заживления
ран), сокращение мышц, поднимающих
волосы.


 Крестцовый отдел состоит из 4 узлов, расположенных на передней поверхности крестца. Внизу
цепочки узлов правого и левого симпатических стволов соединяются в одном
копчиковом непарном узле. Все эти образования объединяются под названием
тазового отдела симпатических стволов. От них идут ветви, участвующие в
образовании вегетативных сплетений таза.
Крестцовый отдел состоит из 4 узлов, расположенных на передней поверхности крестца. Внизу
цепочки узлов правого и левого симпатических стволов соединяются в одном
копчиковом непарном узле. Все эти образования объединяются под названием
тазового отдела симпатических стволов. От них идут ветви, участвующие в
образовании вегетативных сплетений таза. В составе
ветвей лицевого и тройничного нервов парасимпа-тические волокна достигают
слезной железы, желез слизистой оболочки носовой и ротовой полостей,
переключаясь в крылонебном узле, лежащем в крылонебной ямке, и
поднижнечелюстной и подъязычной желез, переключаясь в поднижнечелюстном узле. Самое
большое количество парасимпатических волокон в составе блуждающего нерва. Они
начинаются от его парасимпатического дорсального ядра и иннервируют все органы
шеи, грудной и брюшной полостей до поперечной ободочной кишки включительно. В
грудной и брюшной полостях волокна блуждающих нервов присоединяются к
симпатическим сплетениям и вместе с ними входят в органы. Переключаются волокна
блуждающих нервов в узлах сплетений, расположенных в стенках органов
(интрамуральные узлы).
В составе
ветвей лицевого и тройничного нервов парасимпа-тические волокна достигают
слезной железы, желез слизистой оболочки носовой и ротовой полостей,
переключаясь в крылонебном узле, лежащем в крылонебной ямке, и
поднижнечелюстной и подъязычной желез, переключаясь в поднижнечелюстном узле. Самое
большое количество парасимпатических волокон в составе блуждающего нерва. Они
начинаются от его парасимпатического дорсального ядра и иннервируют все органы
шеи, грудной и брюшной полостей до поперечной ободочной кишки включительно. В
грудной и брюшной полостях волокна блуждающих нервов присоединяются к
симпатическим сплетениям и вместе с ними входят в органы. Переключаются волокна
блуждающих нервов в узлах сплетений, расположенных в стенках органов
(интрамуральные узлы). Например, раздражение парасимпатического нерва — барабанной струны,
вызывает секрецию слюны; раздражение блуждающего нерва — секрецию
поджелудочного сока.
Например, раздражение парасимпатического нерва — барабанной струны,
вызывает секрецию слюны; раздражение блуждающего нерва — секрецию
поджелудочного сока.

 Центральный отдел образуют клетки боковых рогов спинного мозга на
уровне всех его грудных и верхних трех поясничных сегментов. Периферический
отдел представлен нервными волокнами и симпатическими нервными узлами (ганглиями).
Нервные узлы подразделяются на две группы: околопозвоночные
(паравертебральные), расположенные двумя цепочками по бокам от позвоночника и
образующие правый и левый симпатические стволы, и предпозвоночные
(превертебральные) — узлы периферических нервных сплетений, лежащие в грудной и
брюшной полостях.
Центральный отдел образуют клетки боковых рогов спинного мозга на
уровне всех его грудных и верхних трех поясничных сегментов. Периферический
отдел представлен нервными волокнами и симпатическими нервными узлами (ганглиями).
Нервные узлы подразделяются на две группы: околопозвоночные
(паравертебральные), расположенные двумя цепочками по бокам от позвоночника и
образующие правый и левый симпатические стволы, и предпозвоночные
(превертебральные) — узлы периферических нервных сплетений, лежащие в грудной и
брюшной полостях. Кроме этого, они могут образовывать
самостоятельно идущие нервы (например, чревный нерв) и входить в состав
периферических разветвлений спинномозговых и черепных нервов.
Кроме этого, они могут образовывать
самостоятельно идущие нервы (например, чревный нерв) и входить в состав
периферических разветвлений спинномозговых и черепных нервов. Нижний шейный нередко сливается с первым грудным, образуя шейно-грудной,
или звездчатый, узел. От верхнего шейного узла отходят ветви, за счет которых
осуществляется иннервация органов головы и шеи. Эти ветви образуют сплетения на
внутренней и наружной сонных артериях и по ходу их ветвей достигают слезной
железы, слюнных желез, желез слизистой оболочки глотки, гортани, языка, мышцы,
расширяющей зрачок. От трех шейных узлов, обоих симпатических стволов отходят
шейные сердечные нервы, которые спускаются в грудную полость и там вместе с
ветвями блуждающих нервов на восходящей части аорты и легочном стволе образуют
сердечное сплетение, от которого идут нервы к сердцу.
Нижний шейный нередко сливается с первым грудным, образуя шейно-грудной,
или звездчатый, узел. От верхнего шейного узла отходят ветви, за счет которых
осуществляется иннервация органов головы и шеи. Эти ветви образуют сплетения на
внутренней и наружной сонных артериях и по ходу их ветвей достигают слезной
железы, слюнных желез, желез слизистой оболочки глотки, гортани, языка, мышцы,
расширяющей зрачок. От трех шейных узлов, обоих симпатических стволов отходят
шейные сердечные нервы, которые спускаются в грудную полость и там вместе с
ветвями блуждающих нервов на восходящей части аорты и легочном стволе образуют
сердечное сплетение, от которого идут нервы к сердцу. Они несут преганглионарные волокна к
клеткам чревных узлов.
Они несут преганглионарные волокна к
клеткам чревных узлов.
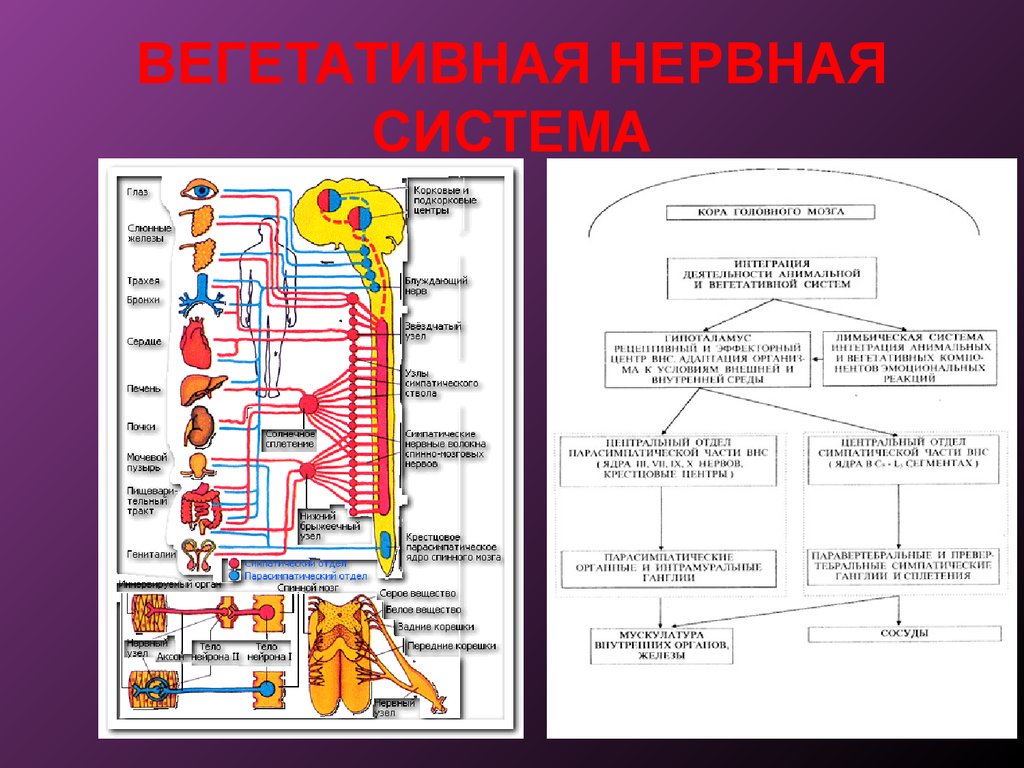
 В его состав входят два чревных нервных узла,
лежащих по бокам от начала чревного ствола, и верхний брыжеечный узел,
расположенный у места отхождения верхней брыжеечной артерии. Преганглионарные
волокна, несут к ним большой и малый внутренностные нервы. В этих узлах
происходит их переключение, и постганглионарные волокна, образуя сплетения на
сосудах, расходятся во все стороны к органам. К чревному сплетению подходят
также ветви блуждающих нервов, но не переключаются в его узлах, а в составе
сплетений следуют в органы, где переключаются в интрамуральных узлах.
В его состав входят два чревных нервных узла,
лежащих по бокам от начала чревного ствола, и верхний брыжеечный узел,
расположенный у места отхождения верхней брыжеечной артерии. Преганглионарные
волокна, несут к ним большой и малый внутренностные нервы. В этих узлах
происходит их переключение, и постганглионарные волокна, образуя сплетения на
сосудах, расходятся во все стороны к органам. К чревному сплетению подходят
также ветви блуждающих нервов, но не переключаются в его узлах, а в составе
сплетений следуют в органы, где переключаются в интрамуральных узлах.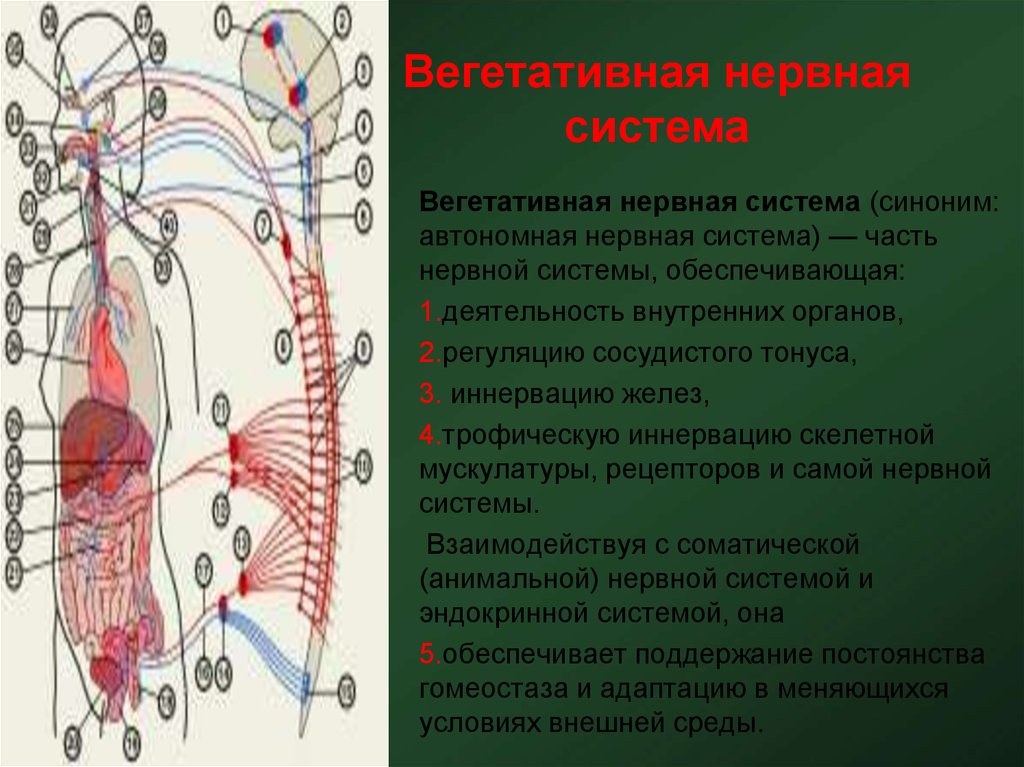 Из ветвей этих сплетений в
органах таза и рядом с ними формируются нервные сплетения: пузырное,
маточно-влагалищное и др. В составе этих сплетений проходят чувствительные
волокна от внутренних органов.
Из ветвей этих сплетений в
органах таза и рядом с ними формируются нервные сплетения: пузырное,
маточно-влагалищное и др. В составе этих сплетений проходят чувствительные
волокна от внутренних органов. Раздражение симпатических нервов увеличивает частоту и силу
сердечных сокращений, повышает его возбудимость. Раздражение парасимпатического
нерва ослабляет эти функции. Трофическое влияние симпатической нервной системы,
изменяющее обмен веществ в органе и приспосабливающее деятельность органа к
потребностям целого организма, JI. А. Орбели назвал,
«адаптационно-трофическим» влиянием. В лаборатории JI. А. Орбели было
доказано, что если раздражением двигательного нерва довести скелетную мышцу до
утомления, а затем присоединить раздражение симпатического нерва, то
работоспособность мышцы восстанавливается. Симпатические нервы повышают обмен
веществ и снижают утомление мышцы.
Раздражение симпатических нервов увеличивает частоту и силу
сердечных сокращений, повышает его возбудимость. Раздражение парасимпатического
нерва ослабляет эти функции. Трофическое влияние симпатической нервной системы,
изменяющее обмен веществ в органе и приспосабливающее деятельность органа к
потребностям целого организма, JI. А. Орбели назвал,
«адаптационно-трофическим» влиянием. В лаборатории JI. А. Орбели было
доказано, что если раздражением двигательного нерва довести скелетную мышцу до
утомления, а затем присоединить раздражение симпатического нерва, то
работоспособность мышцы восстанавливается. Симпатические нервы повышают обмен
веществ и снижают утомление мышцы.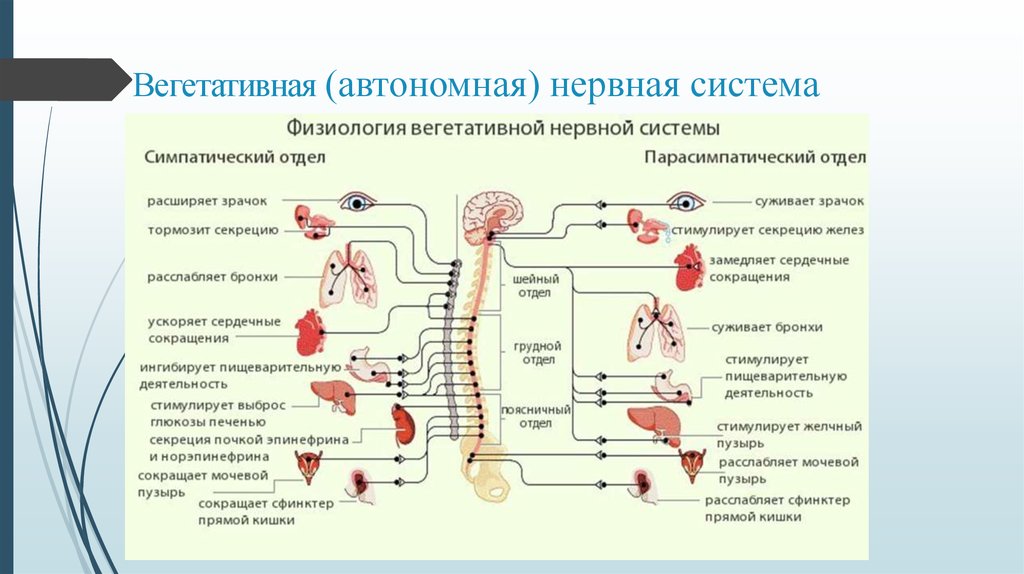 е.
оказывает влияние на все вегетативные функции. Так, например, мышечная работа
координируется с деятельностью внутренних органов, обеспечивающих
энерге-тические ресурсы для ее выполнения. Это согласование достигается путем
безусловных и условных рефлексов. Они обеспечивают единство организма,
поддерживают гомеостаз.
е.
оказывает влияние на все вегетативные функции. Так, например, мышечная работа
координируется с деятельностью внутренних органов, обеспечивающих
энерге-тические ресурсы для ее выполнения. Это согласование достигается путем
безусловных и условных рефлексов. Они обеспечивают единство организма,
поддерживают гомеостаз.
 Включает в себя ядро Якубовича и центральное хвостовое ядро Перлиа, волокна, которых следуют в составе глазодвигательных нервов.
Включает в себя ядро Якубовича и центральное хвостовое ядро Перлиа, волокна, которых следуют в составе глазодвигательных нервов. , Инк.)
Также на Испанский
, Инк.)
Также на Испанский gov: Заболевания вегетативной нервной системы
(Национальные институты здоровья)
gov: Заболевания вегетативной нервной системы
(Национальные институты здоровья) gov: Множественная системная атрофия
(Национальные институты здоровья)
gov: Множественная системная атрофия
(Национальные институты здоровья) ..
.. ..
..