Терапевтическая гипотермия в неонатологии
По данным ВОЗ, ежегодно в мире рождается 4 млн детей в асфиксии, 1 млн — в последующем имеют стойкие нервно-психические отклонения. При тяжелых формах гипоксического повреждения головного мозга летальность превышает 50 %, половина детей погибает в первый месяц. Часть детей с тяжелыми неврологическими нарушениями погибают в младенчестве в основном от сопутствующих инфекций. На сегодняшний день нет ни одного препарата, который может с 100 % эффективностью прервать каскад разрушающих нейроны процессов, вызывающих их гибель и неврологический дефицит. Перспективной методикой, позволяющей снизить неблагоприятные последствия перенесенной асфиксии при рождении, является терапевтическая гипотермия.
История вопроса
Первое упоминание о применении гипотермии у новорожденного относится к 1697 году, когда французский врач Бернар де Гордон опустил в бадью с ледяной водой младенца, родившегося по современным представлениям в асфиксии. Ребенок выжил, получил имя в честь оживившего его доктора, а спасительное действие низких температур стало поводом для исследований.
Ребенок выжил, получил имя в честь оживившего его доктора, а спасительное действие низких температур стало поводом для исследований.
В 1954 году Марин Лакомм из Франции применила управляемую гипотермию в лечении 29 недоношенных детей. Ее опыт не имел положительного результата, однако помог другим ученым в постижении данного вопроса. В 1958 году Джеймс Миллер из Нового Орлеана провел исследование, включившее 10 новорожденных с оценкой по шкале Апгар 0–1 балл на первой минуте жизни. Он опускал новорожденных в ванну с ледяной водой (над поверхностью оставались нос, рот и пуповина ребенка), в которую вводились инфузионные растворы и препараты крови. Девять из 10 малышей выжили.
Ученые из СССР также пытались применить перспективную методику. В 1965 году был создан аппарат для гипотермии «Холод 2Ф», а в 1985-м модифицирована техника охлаждения — избирательное воздействие на голову холодной водой, циркулирующей по резиновым трубкам в шлеме. Однако методика не получила широкого распространения из-за часто возникавших тяжелых осложнений.
Новая стратегия — индуцированная гипотермия
Очередной виток исследований по применению гипотермии начался в 21-м веке. Благодаря техническому прогрессу и клинико-лабораторным возможностям появилась отдельная терапевтическая стратегия: умеренная аппаратная терапевтическая гипотермия (ТГ). Она подразумевает контролируемое индуцируемое снижение температуры тела пациента до 33–34 °С.
Метаанализ 11 рандомизированных контролируемых исследований, включавших в общей сложности 1 505 детей, подтвердил благотворное влияние ТГ на доношенных и поздних недоношенных детей с гипоксически-ишемической энцефалопатией (ГИЭ). Международный комитет по содействию в области реанимации (ILCOR) отнес ТГ к жизненно необходимым мероприятиям и внедрил ее в стандарты оказания неотложной помощи новорожденным. С 2015 года методика управляемой ТГ включена в обновленные руководства по сердечно-легочной реанимации Европейского и Американского обществ реаниматологов, а впоследствии и в национальные протоколы многих стран мира.
Повреждающее действие гипоксии на клетки
Наиболее уязвимым к повреждающему действию гипоксии является головной мозг, что объясняется интенсивностью метаболизма нейронов. Лишь несколько минут отделяют начало острой гипоксии от старта масштабной церебральной катастрофы. Острый период гипоксически-ишемического повреждения длится первые 6 часов. Основные патофизиологические механизмы, происходящие на этом этапе:
- глубокий метаболический дисбаланс;
- некроз — разрушение клетки с поступлением разрушенных фрагментов ядер, органелл и др. во внеклеточное пространство, привлечением в очаг повреждения макрофагов, вырабатывающих процитокины и цитокины;
- апоптоз — запрограммированная клеточная гибель, запускаемая острой церебральной гипоксией, объем клетки постепенно уменьшается, межклеточные контракты пропадают.
У новорожденных основной путь гибели нейронов — апоптоз. Происходит он двумя путями.
Как замедлить патогенетические механизмы?
К сожалению, остановить начавшийся процесс клеточного разрушения невозможно. Тем не менее можно попытаться уберечь еще жизнеспособные нейроны. Для этого в первую очередь нужно замедлить метаболизм: охлаждение головного мозга всего на 1 °С значительно снижает метаболические потребности клетки, замедляет прогрессирование метаболического дисбаланса и делает нейроны менее чувствительными к гипоксии. Кроме того, охлаждение противодействует накоплению макрофагов в очаге поражения, предотвращая выброс провоспалительных цитокинов и отек, способный усугубить ишемию.
По современным представлениям, ТГ блокирует экспрессию каспазы — самого главного белка, связанного с апоптозом.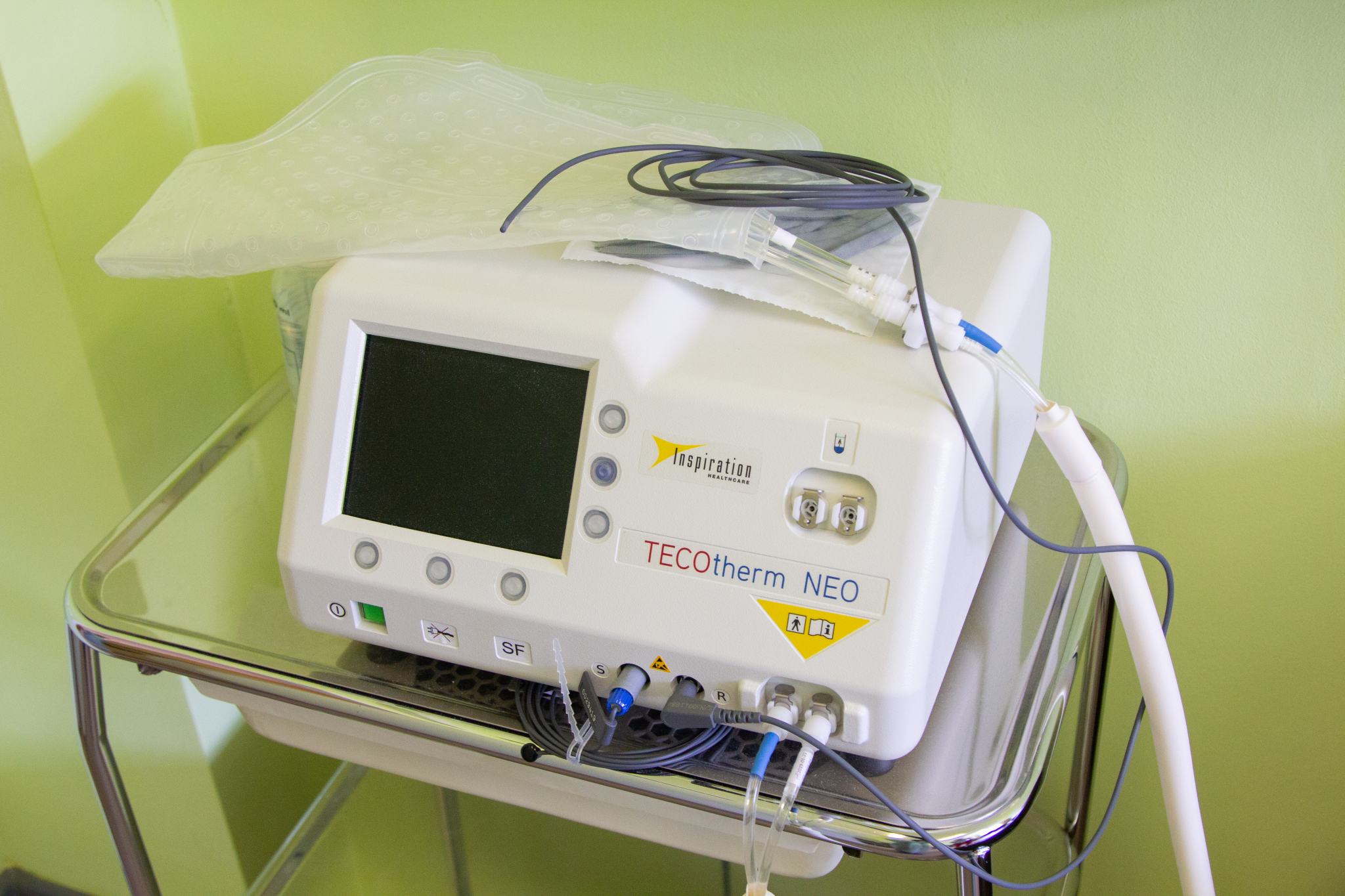 Хотя апоптоз стартует в остром периоде гипоксического повреждения мозга, клинические проявления несколько запаздывают и приходятся уже на следующий этап — подострый. Он начинается спустя 6 часов с момента гипоксии и длится несколько суток, максимально — до недели. Восстановление кровообращения после длительной ишемии сопровождается реперфузионным повреждением: происходит вторая волна гибели нейронов, по своей силе в десятки раз превышающая первую. Воздействуя на процессы, происходящие в остром периоде, ТГ уменьшает интенсивность вторичного повреждения.
Хотя апоптоз стартует в остром периоде гипоксического повреждения мозга, клинические проявления несколько запаздывают и приходятся уже на следующий этап — подострый. Он начинается спустя 6 часов с момента гипоксии и длится несколько суток, максимально — до недели. Восстановление кровообращения после длительной ишемии сопровождается реперфузионным повреждением: происходит вторая волна гибели нейронов, по своей силе в десятки раз превышающая первую. Воздействуя на процессы, происходящие в остром периоде, ТГ уменьшает интенсивность вторичного повреждения.
Таким образом, ТГ блокирует большинство патофизиологических механизмов гипоксически-ишемического повреждения головного мозга и одновременно усиливает нейропротективные процессы (см. табл. 2).Терапевтическое окно, в течение которого должна быть начата гипотермия, составляет 6 часов: это тот самый «светлый» промежуток, после завершения которого прогрессирует вторичное повреждение головного мозга.
Белорусский опыт
С 2018 года в условиях отделения анестезиологии и реанимации новорожденных детей (ОАиРН) 5-й ГКБ Минска с использованием методики ТГ пролечено 10 новорожденных, родившихся в состоянии тяжелой асфиксии.
На факт наличия тяжелой интранатальной асфиксии указывали следующие анамнестические данные: разрыв матки, отслойка плаценты, тугое трехкратное обвитие пуповины вокруг шеи ребенка, рождение ребенка с помощью акушерских щипцов, антенатальное инфицирование и развитие синдрома фетального воспалительного ответа.
Критерии отбора для проведения ребенку ТГ определялись на основании регламентированных документов Российской ассоциации специалистов перинатальной медицины, центра неонатологии Вильнюса, европейских и американских рекомендаций и отражены в таблице (см. табл. 1).
Таблица 1. Критерии для проведения общей терапевтической гипотермииОбщими критериями отбора на ТГ для новорожденных являлись: гестационный возраст более 35 недель и масса тела при рождении более 1 800 г. Далее новорожденные последовательно оценивались по трем группам критериев.
Результаты наблюдений показали максимальную эффективность ТГ при более раннем начале от момента рождения. Исходя из этого мы оценивали возможность включения ребенка в группу исследования на этапе первичной реанимации в течение первых 10 минут жизни. Это определяло аспекты первичного ухода за новорожденным и его транспортировки в отделение.
Исходя из этого мы оценивали возможность включения ребенка в группу исследования на этапе первичной реанимации в течение первых 10 минут жизни. Это определяло аспекты первичного ухода за новорожденным и его транспортировки в отделение.
Стабилизация состояния в отделении реанимации
При поступлении в ОАиРН дети помещались в открытую реанимационную систему Babytherm 8004. Реанимация и стабилизация состояния проводились в соответствии с клиническими протоколами, утвержденными приказом Минздрава Республики Беларусь от 28.01.2011 № 81. Дети получали стандартную посиндромную терапию, гемодинамика поддерживалась с помощью волемических нагрузок, инотропных и вазопрессорных препаратов в различных комбинациях (дофамин, добутамин, адреналин, норадреналин). Гемодинамический мониторинг осуществлялся инвазивным и неинвазивным методами.
С 2021 года используем методику функциональной прикроватной эхокардиографии, которая также дает ценную информацию о состоянии гемодинамики и волемичского статуса. В течение часа повторно определялись критерии из групп А и В, у всех детей присутствовало как минимум по 2 критерия каждой группы.
В течение часа повторно определялись критерии из групп А и В, у всех детей присутствовало как минимум по 2 критерия каждой группы.
Пациентам была проведена нейросонография (НСГ) с допплерометрией мозгового кровотока с целью исключения массивных внутричерепных кровоизлияний и оценки состояния церебральной гемодинамики. В связи с возможной технической задержкой для проведения и расшифровки ЭЭГ начинали нейромониторинг уже на фоне проведения ТГ. С родителями проводили подробную беседу, объясняли суть методики с целью максимально раннего получения информированного согласия на проведение манипуляций, в т. ч. ТГ.
Алгоритм индуцированного снижения температуры
Для достижения контролируемой гипотермии применяем аппарат Blancetrol III. Температуру тела новорожденных постепенно снижаем до 33,5 ± 0,5 °C и поддерживаем на таком уровне в течение 72 часов с последующим согреванием до нормального уровня в течение 6 часов со скоростью 0,5 °C в час. У всех детей группы ТГ была начата в течение первого часа жизни, ко второму часу были достигнуты значения ректальной температуры в диапазоне от 33,2 до 33,8 °C.
У всех детей группы ТГ была начата в течение первого часа жизни, ко второму часу были достигнуты значения ректальной температуры в диапазоне от 33,2 до 33,8 °C.
Динамика показателей на фоне проводимой ТГ
При поступлении в ОАиРН оценивались степень тяжести ГИЭ с использованием модифицированной шкалы Sarnat и дальнейшая неврологическая динамика, наличие судорог, динамика кислотно-щелочного баланса, параметры ИВЛ (фракция кислорода во вдыхаемой смеси FiO2, среднее давление в дыхательных путях MAP до и во время процедуры охлаждения).
У всех детей при поступлении отмечался декомпенсированный метаболический ацидоз (гиперлактатацидоз). На фоне проводимой ТГ уже через 3 часа удалось уменьшить метаболические расстройства, что сопровождалось снижением уровня дефицита оснований и лактата крови. К концу первых суток у всех детей были достигнуты приемлемые показатели газового состава крови и в дальнейшем не было значимых нарушений кислотно-щелочного равновесия.
Все дети при рождении имели неэффективное дыхание, что потребовало проведения ИВЛ, у половины — высокочастотной, пролонгировалась более 5 суток. По нашим наблюдениям, FiO2 и MAP снижались к 12-му часу жизни и доходили до минимума к концу 3-х суток.
Гемодинамические нарушения различной степени выраженности отмечались во всех клинических случаях, в двух диагностирован комбинированный гиповолемический и перераспределительный шок. Высокие и средние терапевтические дозы кардиотоников и вазопрессоров для стабилизации гемодинамики использовались у всех пациентов. Средняя длительность инотропной поддержки составила 5 дней (индивидуально максимальная — 17 дней, минимальная — 3 дня).
Нарушения коагуляции разной степени выраженности наблюдались во всех случаях и проявлялись повышенной кровоточивостью из мест инъекций, контактной кровоточивостью слизистых желудка и трахеобронхиального дерева, изменениями коагулограммы в виде гипофибриногенемии менее 1,5 г/л и удлинения показателей активированного частичного тромбопластинового времени и тромбинового времени (у 90 % детей). Всем детям проводились трансфузия факторов свертывания крови (свежезамороженная плазма, «Октаплас») и введение витамина К.
Всем детям проводились трансфузия факторов свертывания крови (свежезамороженная плазма, «Октаплас») и введение витамина К.
Противопоказаниями для применения ТГ являются: гестационный возраст менее 35 недель, вес ≤1 800 г, массивные внутричерепные геморрагии, повреждение мягких тканей головы или переломы костей свода черепа, атрезия ануса или множественные пороки развития, возраст старше 6 часов.
Случаи из практики
1. Анамнез матери: монохориальная диамниотическая двойня. Срочные роды через естественные родовые пути первым плодом. Острая гипоксия второго плода. Экстренное кесарево сечение.
Оценка по шкале Апгар 1/ИВЛ. В родильном зале проводился комплекс реанимационных мероприятий. Восстановление сердечной деятельности на 4-й минуте. С родзала ребенок не согревался. На 10-й минуте — глубокое угнетение ЦНС, зрачки широкие, реакция зрачков на свет (РЗС) отсутствовала.
ТГ начата в течение первого часа.
Из обследования: ОАК — анемический синдром, БАК — повышение АсАТ, АлАТ. КЩС: декомпенсированный метаболический лактат-ацидоз (рН 6,8; ВЕ -22,0; лактат 18 ммоль/л). НСГ: выраженная перивентрикулярная инфильтрация, ИР ПМА 0,58, затруднение венозного оттока.
ЭЭГ на 1-е сутки (на фоне ТГ): постоянный фоновый паттерн с крайне низким вольтажом (см. рис. 1). Клинически — кома. РЗС за период лечения отсутствует. Выраженные вегетативно-висцеральные нарушения. Длительная потребность в инотропной помощи.
Рисунок 1. Тяжелые нарушения фоновой активности (макс. амплитуда ≤ 10 мкВ; мин. амплитуда ≤ 5 мкВ)Наличие бульбарных расстройств, невозможность экстубации.
КТ: снижение плотности мозговой паренхимы, мультифокальные кортикальные и субкортикальные очаги пониженной плотности.
Исход: тяжелое органическое поражение ЦНС, паллиативная помощь.
2. Анамнез матери: женщина поступила в приемный покой в потужном периоде 4-х самопроизвольных родов. Длительный безводный период (18 ч). Тугое обвитие пуповины вокруг шеи плода.
Длительный безводный период (18 ч). Тугое обвитие пуповины вокруг шеи плода.
Оценка по шкале Апгар 1/ИВЛ. В родзале — комплекс реанимационных мероприятий. Восстановление сердечной деятельности на 5-й минуте. Глубокое угнетение ЦНС. Через 3 часа после рождения появился легкий тремор, реакция на осмотр в виде вздрагиваний, восстановилась РЗС.
Из обследования: ОАК, БАК: возрастная норма. КЩС: декомпенсированный метаболический лактат-ацидоз (рН 6,9; ВЕ -26,0; лактат 23). НСГ: ПВИ. Снижение ИР и скорости артериального кровотока, кровоток в вене Галена не определяется.
ЭЭГ (2-е сутки): прерывистый паттерн с нормальным вольтажом (см. рис. 2).
Рисунок 2.
Экстубирован на 5-е сутки. Переведен в ПО на 8-е сутки. С 10-х суток совместное пребывание с матерью, приложен к груди.
КТ, МРТ: без структурной патологии.
Растет и развивается по возрасту.
3. Анамнез матери: Роды первые, срочные, слабость потуг. Острая гипоксия плода. Извлечение плода с использованием вакуум-экстрактора. Тугое обвитие пуповины вокруг шеи плода.
Острая гипоксия плода. Извлечение плода с использованием вакуум-экстрактора. Тугое обвитие пуповины вокруг шеи плода.
Оценка по шкале Апгар 3/ИВЛ. В родильном зале — комплекс реанимационных мероприятий. На фоне ИВЛ со 2-й минуты восстановление нормальной сердечной деятельности.
Из обследования: ОАК: лейкоцитоз без сдвига лейкоформулы. БАК: повышен АсАТ. КЩС: декомпенсированный метаболический лактат-ацидоз (рН 7,0; ВЕ -26,0, лактат 15). НСГ: ПВИ. Отек ГМ. Выраженная дисциркуляция мозгового кровотока — маятникообразный характер артериального кровотока, резко снижена скорость венозного кровотока. Раннее появление тонико-клонических судорог. РЗС сохранена, симметрична. Исключены травматические повреждения черепа и головного мозга, массивные ВЧК.
ЭЭГ: судорожная активность (см. рис. 3).
Рисунок 3.
Увеличена доза мидазолама до максимальной. Мультифокальные клонические судороги. Ребенок введен в барбитуровую кому. С 3-х суток — фенобарбитал перорально. Судороги не повторялись.
С 3-х суток — фенобарбитал перорально. Судороги не повторялись.
Экстубирован на 7-е сутки.
ЭЭГ на 7-е сутки: прерывистый паттерн с нормальным вольтажом без судорожной готовности.
НСГ: восстановление допплерометрических характеристик по артериальному и венозному кровотоку.
Переведен в ПО на 9-е сутки. С 10-х суток совместное пребывание с матерью, сосет из рожка.
КТ, МРТ: без структурной патологии.
Растет и развивается по возрасту.
Результаты
У всех пациентов из группы наблюдения отмечена положительная динамика состояния, летальных исходов в неонатальном периоде не было. У большинства детей — положительная динамика по неврологическому статусу. Экстубированы 8 пациентов (70 %), переведены в педиатрическое отделение (ПО). Два пациента на фоне продолжающейся ИВЛ были переведены в реанимационное отделение 3-й ГДКБ.
Анализ катамнестических данных показывает наличие тяжелого органического поражения ЦНС к концу 1-го года жизни у 2 пациентов. Пятеро из 10 детей на данный момент здоровы, растут и развиваются по возрасту (отдаленные последствия пока неизвестны).
Пятеро из 10 детей на данный момент здоровы, растут и развиваются по возрасту (отдаленные последствия пока неизвестны).
Вне сомнения, некорректно делать какие-либо выводы, опираясь всего на 10 исследований. Доказательная медицина не знает сослагательного наклонения, наша команда использовала мировой опыт и внедрила его в свою работу.
Аппарат для гипотермии новорожденных Tecotherm Neo
РЗН 2016/4602
блок обогрева / одеяло, для новорожденных, подогрев 12 — 39 °C, размеры 37.3×19×30.7 см, вес 6.95 кг
TEC COM GmbH, Германия
ОКП/ОКПД2: 94 4490
Характеристики
| Вид | блок обогрева / одеяло |
| Назначение | для новорожденных |
| Подогрев | 12 — 39 °C |
| Размеры | 37.3×19×30.7 см |
| Вес | 6.95 кг |
Дополнительные характеристики
Система терморегуляции Tecotherm Neo – это гипо/гипертермический аппарат, разработанный для охлаждения и согревания новорожденных пациентов весом до 50 кг при помощи специальных водяных матрасиков или одеял. Охлаждающая терапия применяется для новорожденных пациентов: Особенности системы Tecotherm Neo ‣ Интеллектуальная система тревожной сигнализации: при отклонении от установленной температуры, низком уровне жидкости, отсутствии питания и прекращении потока жидкости.  Сигнализирует об отклонении температуры тела более чем на 0.5°С от установленной. Сигнализирует об отклонении температуры тела более чем на 0.5°С от установленной.‣ Большой цветной дисплей четко показывает температуру, а изменения цветов предупреждают медперсонал о любой проблеме. Принцип работы системы Ректальный зонд вводится пациенту (примерно на 5 см), после чего показания измеряемой температуры тела передаются на прибор Tecotherm Neo. С помощью специального водного матрасика/одеялка тепло или холод подводятся к телу пациента. Охлажденная вода, контактируя с ребенком, забирает часть тепла, далее возвращается в аппарат, где затем охлаждается. Происходит постоянная циркуляция жидкости по контуру и таким образом поддерживается требуемая температура тела пациента. Tecotherm Neo имеет три режима работы: 1. Программируемый режим сервоконтроля. Врач может запрограммировать длительность процедуры охлаждения, предел повышения температуры, а также установить целевое значение температуры. При данном режиме прибор Tecotherm Neo выполняет полный курс лечения без вмешательства персонала.  2. Серво-контролируемая ректальная температура. Прибор Tecotherm Neo поддерживает температуру, которую устанавливает врач с использованием ректального датчика. Диапазон изменений может быть установлен как для повышения температуры, так и охлаждения. 3. Постоянная температура матрасика Жидкость циркулирует по матрасику и поддерживает постоянную заданную температуру вне зависимости от состояния пациента. Данный режим может применяться в исследовательских целях, либо опытный пользователь самостоятельно отслеживает состояние пациента. |
Терапевтическая гипотермия у новорожденных
Введение
Асфиксия новорожденных является серьезной проблемой здравоохранения во всем мире. В развитых странах асфиксия поражает 3-5 человек на 1000 живорождений. Последующее развитие умеренной и тяжелой гипоксически-ишемической энцефалопатии (ГИЭ) происходит в 0,5-1 случае на 1000 живорожденных, при этом до 60% этих детей умирают в неонатальном периоде, а 25% выживших имеют серьезные долгосрочные проблемы развития нервной системы.
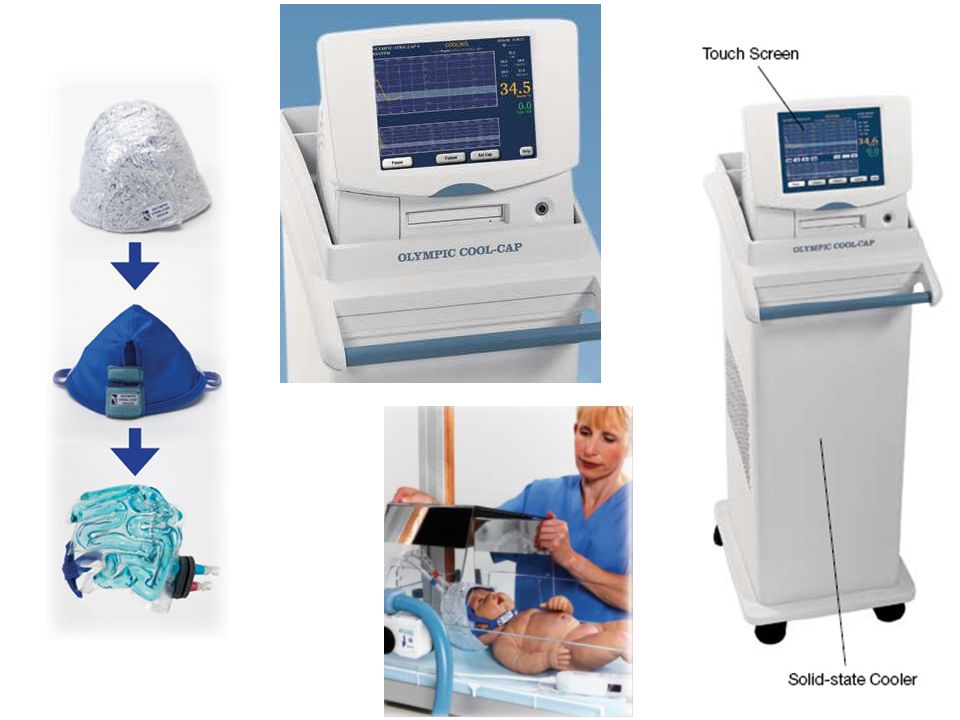
Многие экспериментальные модели на животных и систематические обзоры рандомизированных контролируемых испытаний показали, что как гипотермия всего тела, так и избирательное охлаждение головы обладают нейропротекторным эффектом. Он модифицирует клетки, запрограммированные на апоптоз, что приводит к их выживанию.
Цель
Целью данного руководства является описание ведения пациента, подвергающегося терапевтической гипотермии в отделении интенсивной терапии интенсивной терапии.
Определение терминов
- Апоптоз : Запрограммированная гибель клеток.
 Клетки умирают в ответ на различные раздражители, и во время апоптоза они делают это контролируемым и регулируемым образом. Апоптоз — это процесс, в котором клетки играют активную роль в собственной гибели, и его часто называют клеточным самоубийством.
Клетки умирают в ответ на различные раздражители, и во время апоптоза они делают это контролируемым и регулируемым образом. Апоптоз — это процесс, в котором клетки играют активную роль в собственной гибели, и его часто называют клеточным самоубийством. - Контролируемый
Пассивная гипотермия : это метод, используемый в отделениях специального ухода, позволяющий ребенку естественным образом охладиться во время процесса стабилизации и перед переводом в отделение интенсивной терапии.
- Энцефалопатия : Заболевание головного мозга, повреждение или неисправность. В целом энцефалопатия проявляется измененным психическим состоянием, которое может сопровождаться физическими проявлениями, например. аномальные движения конечностей.
- Глюкоза
Скорость инфузии (GIR) : Скорость введения глюкозы рассчитывается с учетом жидкостей и кормления при различных концентрациях и скоростях, чтобы обеспечить получение младенцем достаточного количества глюкозы.

- Гипоксически-ишемический
Энцефалопатия (HIE) : Недостаток кислорода в головном мозге и уменьшение количества крови, перфузирующей мозг. Это приводит к подавлению электрической активности и корковой депрессии.
- Система гипер/гипотермии Medi-Therm III ® : Обеспечивает средства для регулирования температуры пациента путем подачи воды с регулируемой температурой через одеяло, подложенное под пациента.
Ключевые моменты
- Немедленная смерть при тяжелом поражении. Это связано с клеточной гипоксией, приводящей к недостаточности первичной энергии и клеточной деполяризации.
- После латентного периода (6-100 часов) гибель нейронов может быть инициирована каскадом патологических процессов и связана с выраженной энцефалопатией. Это включает цитотоксический отек, митохондриальную недостаточность, накопление эксайтотоксинов, активную гибель клеток, азотистое
синтез оксидов и цитотоксическое действие активированной микроглии.

- Нейропротекция у детей ≥ 35 недель гестации с умеренной или тяжелой гипоксически-ишемической энцефалопатией (ГИЭ) оптимизируется путем начала лечения терапевтической гипотермией как можно раньше после реанимации, между 1-6 часами жизни.
- Гипотермию всего тела необходимо строго контролировать и ориентировать на диапазон ректальной температуры 33°C-34°C.
- Следует избегать гипертермии ≥38°C, так как это неблагоприятно влияет на исходы у младенцев с ГИЭ.
- ≥ 35 недель гестационного возраста и более 1,8 кг.
- < 6 часов после рождения.
- Признаки асфиксии, определяемые наличием как минимум двух из следующих четырех критериев:
- Оценка относительных противопоказаний и планы полного ухода. Например: неконтролируемая легочная гипертензия, неконтролируемая клиническая коагулопатия (т.
 е. активное кровотечение), серьезные врожденные аномалии, выживание маловероятно (это
следует обсудить с третичным неонатологом или консультантом PIPER). Персистирующая легочная гипертензия (PPHN) не должна рассматриваться как противопоказание к началу терапевтической гипотермии при ГИЭ.
е. активное кровотечение), серьезные врожденные аномалии, выживание маловероятно (это
следует обсудить с третичным неонатологом или консультантом PIPER). Персистирующая легочная гипертензия (PPHN) не должна рассматриваться как противопоказание к началу терапевтической гипотермии при ГИЭ. - Клинически определяемая умеренная или тяжелая ГИЭ (стадия 2 или 3 на основе модифицированной классификации Sarnat). Наличие умеренной/тяжелой ГИЭ определяется как припадки ИЛИ присутствие признаков как минимум в трех из шести следующих категорий:
- Активный охлаждение — в течение 72 часов с начала охлаждения.
- Подогрев — 12 часов активного постепенного разогрева после завершения 72 часов охлаждения.
- Система гипер/гипотермии Medi-Therm III TM (Установка и использование системы гипер/гипотермии Medi-Therm III TM в соответствии с для использования Medi-Therm III ® Система гипер/гипотермии )
- Ректальный датчик температуры
- Кормите младенца обнаженным на лучистом обогревателе при выключенном обогревателе.
 Не кормите грудью в инкубаторе.
Не кормите грудью в инкубаторе. - Младенцам обычно требуется искусственная вентиляция легких для поддержания адекватной оксигенации и вентиляции. Гипотермия сдвигает кривую оксигемоглобина и может привести к снижению доставки кислорода, но скорость метаболизма также снижается, что снижает потребление кислорода и углерода.
производство диоксида. Если ребенок не вентилируется, то скорость метаболизма может увеличиться без увеличения доставки кислорода.
- Используйте увлажненный нагретый газ как обычно в вентиляционном контуре.
- При 33,5°C средняя ЧСС составляет приблизительно 80-100 ударов в минуту (уд/мин). ЧСС изменяется на 15 уд/мин при изменении температуры на 1°С.
- Мониторинг АД – дети с гипотермией подвержены риску гиповолемии, поскольку холод может вызвать вытеснение воды в ткани.
 Младенцам могут потребоваться пломбы и инотропы (сначала устранить гиповолемию).
Младенцам могут потребоваться пломбы и инотропы (сначала устранить гиповолемию). - Целевые уровни SaO2 и артериального давления должны устанавливаться медицинской бригадой и обсуждаться во время обхода палаты.
- Следите за аритмиями – синусовая брадикардия является наиболее распространенной аритмией
- Вставьте ректальный зонд 9FR на 5 см в задний проход и на расстоянии 10 см привяжите зонд к верхней части бедра. Отметьте 5 см и 10 см на датчике перед введением. Крайне важно, чтобы датчик был правильно вставлен, чтобы обеспечить точный мониторинг температуры.
- Установите пределы аварийного сигнала температуры на уровне 33,5°C (низкая) и 34,5°C (высокая) во время охлаждения.
- Ежечасно проверяйте ректальный датчик.
- Регулярно контролируйте температуру подмышечной впадины.

- Начать мониторинг АЭЭГ (приступы возникают у 43-56% новорожденных с ГИЭ, подвергающихся охлаждению). Пик большинства приступов приходится на первые 48 часов. Следуйте алгоритму лечения приступов.
- Проверьте зрачки, оцените уровень сознания и наличие признаков повышенного внутричерепного давления
- Потребуется формальная ЭЭГ и МРТ позже (через 3-7 дней после согревания). Ранняя МРТ может быть сделана, чтобы помочь принять решение о паллиативной помощи.
- Кровь обычно берут при поступлении, до начала охлаждения, затем через 4, 8, 12, 24 и 72 часа
- Младенцы с ГИЭ подвержены риску множественного дисбаланса электролитов и нуждаются в частом наблюдении и коррекции на основе лабораторных показателей, как указано в назначении лечения.

- Коагулопатия может быть вызвана гипотермией из-за снижения функции тромбоцитов
- Минимизируйте риск отека мозга, поддерживая уровень натрия на верхнем пределе нормы
- Магний поддерживается на верхних границах нормы, так как обладает нейропротекторным действием.
- Целевые уровни газов крови должны устанавливаться медицинской бригадой и обсуждаться во время обхода палаты.
- Общее потребление жидкости обычно составляет 40-60 мл/кг/день.
- GIR необходимо рассчитать, чтобы обеспечить адекватный уровень сахара при непрерывных инфузиях, поскольку они подвержены риску гипогликемии.
- Может потребоваться концентрация глюкозы выше 10% декстрозы, поэтому необходим доступ к центральной линии.
- Начало энтерального питания младенцев во время терапевтической гипотермии следует рассматривать на индивидуальной основе с учетом общего клинического состояния.

- Местный мочевой катетер. Необходим строгий баланс жидкости. Если диурез падает ниже 1 мл/кг/час, необходимо уведомить медицинскую бригаду.
- См. «Оценка боли у новорожденных» и «Руководство по лечению боли у новорожденных».
- Неадекватная седация может привести к увеличению скорости метаболизма, что снижает эффективность стратегии охлаждения.
- Для обеспечения адекватного обезболивания вмешательства следует проводить при более низких баллах боли. Младенцы, подвергающиеся терапевтической гипотермии, могут быть не в состоянии демонстрировать типичные поведенческие признаки боли, а физиологические параметры также могут быть изменены.
- Через 48 часов следует рассмотреть вопрос об отмене морфина, чтобы снизить риск накопления и токсичности.
 Следите за признаками неадекватной седации: увеличение ЧСС, озноб, затрудненное дыхание.
Следите за признаками неадекватной седации: увеличение ЧСС, озноб, затрудненное дыхание. - Гипотермия может вызвать иммунную дисфункцию, поэтому переохлажденных младенцев часто профилактически вводят внутривенно антибиотиками
- Строгий инфекционный контроль – лечение сердечно-сосудистых заболеваний и постоянный катетер
- Ежедневный осмотр на наличие признаков инфекции (см. анализы крови и мониторинг выше, осмотр живота на предмет вздутия)
- Требуется частый осмотр кожи и изменение положения – в соответствии с руководством по травмам от давления
- Младенца можно кормить на спине с наклоном на 30° вправо или влево. Во избежание ухудшения возврата мозгового кровотока держите голову на одной линии с позвоночником (нос на средней линии тела)
- Мониторинг кожи на предмет цвета, перфузии, повреждения кожи и признаков некроза подкожной жировой клетчатки
- Хотя некроз подкожной жировой клетчатки встречается редко, он характеризуется уплотнением эритематозных узелков и бляшек на костных выступах, таких как спина, руки, ягодицы, бедра и грудь.
 Это происходит редко, предположительно потому, что бурый жир более чувствителен к гипоксии и
ухудшается при охлаждении. Это также может привести к гиперкальциемии, гиперлипидемии и тромбоцитопении
Это происходит редко, предположительно потому, что бурый жир более чувствителен к гипоксии и
ухудшается при охлаждении. Это также может привести к гиперкальциемии, гиперлипидемии и тромбоцитопении - Повышайте температуру на 0,5ºC каждые 2 часа, как указано в медицинских предписаниях EMR и заметках о проделанной работе, до 37°C +/- 0,2.
- Часто контролируйте температуру после согревания, чтобы предотвратить рикошетную гипертермию.
- Лучистый обогреватель должен оставаться выключенным до конца периода повторного нагрева, чтобы избежать любых возможных неблагоприятных последствий быстрого повторного нагрева.
- Медленное повторное нагревание может помочь сохранить все преимущества охлаждения.
- Внимательно наблюдайте за ребенком на предмет осложнений на этапе согревания, так как у него может быть более высокий риск судорог, гипотензии или ПЛГН.

- Зафиксировать время включения активного охлаждения. Документируйте запрограммированную температуру и фактическую температуру в EMR.
- Регулярно документируйте переносимость пациентом охлаждения, включая наблюдения, mPATS, оценку кожи и доказательства осложнений.
- Сердечно-сосудистые осложнения – (брадикардия, удлинение интервала QT, желудочковые аритмии, снижение сердечного выброса, артериальная гипотензия)
- Снижение продукции сурфактанта, повышение сопротивления легочных сосудов, увеличение потребления кислорода и потребности в кислороде
- Электролитный дисбаланс: гипокалиемия, гипомагнезия, гипофосфатемия
- Коагулопатия, особенно функция тромбоцитов
- Риск заражения увеличивается из-за ингибирования провоспалительной реакции (повышение частоты сепсиса, внутрисуставных и раневых инфекций)
- Изменение фармакокинетики из-за изменений функции печени и почек
- Продлевает действие и увеличивает концентрацию в крови многих лекарств, включая опиаты и седативные средства, при использовании стандартных доз и интервалов дозирования
- Продлевает действие и увеличивает концентрацию в крови многих лекарств, включая опиаты и седативные средства, при использовании стандартных доз и интервалов дозирования
- Задержка опорожнения желудка и повышение уровня амилазы в сыворотке
- Переносимость энтерального питания может быть плохой, и его обычно прекращают во время охлаждения
- Рассмотреть план питания и необходимость парентерального питания
- Переносимость энтерального питания может быть плохой, и его обычно прекращают во время охлаждения
- Как пользоваться системой гипер/гипотермии Medi-Therm III.
- Руководство по профилактике и лечению пролежневых травм
- Руководство по уходу за больными с помощью вспомогательной терморегуляции
- Управление судорогами в отделении интенсивной терапии новорожденных, руководство
- Учебный пакет Butterfly Brainz
- Руководство по уходу за новорожденными с гипогликемией
- Рекомендации медсестер по оценке боли у новорожденных
- Руководство по медицинскому обслуживанию новорожденных в отделении интенсивной терапии новорожденных
- Аззопарди, Д., Стром, Б., Эдвардс, А.Д. (2009) Уход асфиксии новорожденных с умеренной гипотермией в рутинной клинической практика: как осуществляется охлаждение в Великобритании вне клинических испытаний . Архивы болезней у детей. Fetal and Neonatal Edition 94. 260–264.
- Аззопарди, Д., Броклхерст, П., Эдвардс, Д., Халлидей, Х. Левен, М., Торесен, М., Уайтлоу, А. (2008) Исследование TOBY. Гипотермия всего тела для лечения перинатальной асфиксии энцефалопатия: рандомизированное контролируемое исследование . БМЦ Педиатрия. 8: 17
- Чанг.М.К., Джонг.Ю.Дж., Лин. C-H (2017) Терапевтическая гипотермия новорожденных с гипоксически-ишемической эцефалопотией, педиатрия и неонатология, 58, 475-483.
- Терапевтическая гипотермия при гипоксически-ишемической энцефалопатии: введение в ясли особого ухода, Safer Care Victoria, обновлено 17 th Feb 2021
- Эйхер, Д.
 Дж., Вагнер, К.Л., Катиканени, Л.П., Халси, Т.С., Басс, В.Т., Кауфман, Д.А. и др. . (2005) Умеренная гипотермия при неонатальной энцефалопатии: эффективность
результаты. Детская неврология. 32: 11-7 . Гипотермическая нейропротекция. 27 74.
Дж., Вагнер, К.Л., Катиканени, Л.П., Халси, Т.С., Басс, В.Т., Кауфман, Д.А. и др. . (2005) Умеренная гипотермия при неонатальной энцефалопатии: эффективность
результаты. Детская неврология. 32: 11-7 . Гипотермическая нейропротекция. 27 74. - Глюкман, П.Д., Вятт, Дж.С., Аззопарди, Д., Баллард, Р., Эдвардс, А.Д., Ферриеро, Д.М. и др. . (2005) Селективный охлаждение головы с легкой системной гипотермией после неонатальной энцефалопатии: многоцентровое рандомизированное исследование . Ланцет. 365. 663-670.
- Джейкобс С.Э., Берг М., Хант Р., Тарнов Морди В.О., Индер Т.Е., Дэвис П.Г. (2013). Охлаждение новорожденных с гипоксически-ишемической энцефалопатией . Систематический обзор Кокрановской базы данных. 31 (1).
- Лутц. IC, Allegaert.K, Hoon.JN и Marynissen.H, 2020, Фармакокинетика во время терапевтической гипотермии при неонатальной гипоксической ишемической эцефалопотии: обзор литературы.
 Открытие педиатрии BMJ.
Открытие педиатрии BMJ. - Мосалли, Р. (2012) Охлаждение всего тела для Младенцы с гипоксически-ишемической энцефалопатией. Журнал клинической неонатологии. 1 (2). 101-106.
- Нассеф, С.К., Бленноу, М., Джирве, М. (2012). Опыт родителей, чьи Новорожденные проходят лечение гипотермией после перинатальной асфиксии . JOGNN, 42 (1): 38-47.
- Сакр. М., Баласундарам, 2022 г., Неонатальная терапевтическая гипотермия, Стат. жемчуг.
- Sarnat, H., Sarnat, M. (1976) Неонатальная энцефалопатия после бедствие . Архив неврологии. 33. 695-705.
- Сарнат. HB, Flores-Sarnat.L, Fajardo.C, Leijser.LM, Wusthoff.C, Mohammad.K, 2020, Шкала оценки Сарнат для неонатальной эцефалопатии через 45 лет: обновленное предложение, Детская неврология, 113, 75-79 .
- Шах П.С., Олссон А., Перлман М. (2007). Гипотермия для лечения
неонатальная гипоксически-ишемическая энцефалопатия: систематический обзор .
 Архив детской подростковой медицины, 161: 951-8.
Архив детской подростковой медицины, 161: 951-8. - Шанкаран С., Лаптук А.Р., Эренкранц Р.А., Тайсон Дж.Е., Макдональд С.А., Донован Э.Ф., и др. (2005 ). Национальный Сеть неонатальных исследований Института здоровья и развития ребенка. Гипотермия всего тела у новорожденных с гипоксически-ишемической энцефалопатией . Медицинский журнал Новой Англии. 353. 1574-1584.
- Клинические рекомендации Квинсленда, Гипоксическая ишемическая энцефалопатия (ГИЭ), Queensland Health 2021
Не забудьте прочитать отказ от ответственности.
Разработку этого руководства по сестринскому делу координировала Элисон Кендрик, преподаватель клинической медсестры отделения Butterfly Ward, и оно было одобрено Комитетом по клинической эффективности сестринского дела. Обновлено в январе 2023 г.
Возникновение неонатальной гипотермии и связанных с ней факторов риска среди новорожденных с низкой массой тела при рождении (НМТ) в Аккре, Гана
Цели в области устойчивого развития (ЦУР) признают детскую смертность серьезной глобальной проблемой здравоохранения и направлены на прекращение предотвратимой неонатальной и детской смертности к 2030 году.
 1 Только в 2020 году во всем мире умерло около 5 миллионов детей в возрасте до 5 лет. ; из них 2,4 миллиона умерли в неонатальный период, в первые 28 дней жизни. 2 Глобальный коэффициент неонатальной смертности (NMR) составляет 17 смертей на 1000 живорождений, причем этот показатель непропорционально выше в странах Африки к югу от Сахары (27 смертей на 1000 живорождений). 2 Ведущими причинами неонатальной смертности являются преждевременные роды (35%), интранатальные осложнения (24%) и инфекции (15%). 3 ЦУР 3 включает задачи по снижению ЧСС до 12 смертей на 1000 живорождений и коэффициента смертности детей в возрасте до 5 лет (U5MR) до 25 смертей на 1000 живорождений во всех странах к 2030 году. 1 Прогресс в достижении этих целей была заметно неравномерной по странам и между регионами, и пандемия COVID-19, вероятно, может свести на нет недавние достижения в области выживаемости детей. 2,4 В целом, лишь несколько стран находятся на пути к достижению целей NMR и U5MR к 2030 году.
1 Только в 2020 году во всем мире умерло около 5 миллионов детей в возрасте до 5 лет. ; из них 2,4 миллиона умерли в неонатальный период, в первые 28 дней жизни. 2 Глобальный коэффициент неонатальной смертности (NMR) составляет 17 смертей на 1000 живорождений, причем этот показатель непропорционально выше в странах Африки к югу от Сахары (27 смертей на 1000 живорождений). 2 Ведущими причинами неонатальной смертности являются преждевременные роды (35%), интранатальные осложнения (24%) и инфекции (15%). 3 ЦУР 3 включает задачи по снижению ЧСС до 12 смертей на 1000 живорождений и коэффициента смертности детей в возрасте до 5 лет (U5MR) до 25 смертей на 1000 живорождений во всех странах к 2030 году. 1 Прогресс в достижении этих целей была заметно неравномерной по странам и между регионами, и пандемия COVID-19, вероятно, может свести на нет недавние достижения в области выживаемости детей. 2,4 В целом, лишь несколько стран находятся на пути к достижению целей NMR и U5MR к 2030 году. Если нынешние тенденции сохранятся, две трети стран Африки к югу от Сахары не достигнут целей. 5 Ускоренный прогресс в достижении незавершенной повестки дня в области устойчивого развития требует новых парадигм, стратегического мышления и инновационных подходов для снижения детской смертности, особенно в критический неонатальный период.
Если нынешние тенденции сохранятся, две трети стран Африки к югу от Сахары не достигнут целей. 5 Ускоренный прогресс в достижении незавершенной повестки дня в области устойчивого развития требует новых парадигм, стратегического мышления и инновационных подходов для снижения детской смертности, особенно в критический неонатальный период.Неонатальная гипотермия, определяемая как внутренняя температура тела ниже 36,5°C, способствует неонатальной смертности. 6–8 Всемирная организация здравоохранения (ВОЗ) классифицирует гипотермию на три группы в зависимости от ее тяжести: легкая гипотермия (36,0–36,4°C), умеренная гипотермия (32,0–35,9°C) и тяжелая гипотермия (<32,0°C) . 7 Независимо от гестационного возраста и массы тела при рождении гипотермия новорожденных увеличивает риск смерти в пять раз. 9 При снижении температуры тела новорожденного на каждый градус Цельсия риск смертности увеличивается на 80%. 10 Хотя нерешенная и нелеченная неонатальная гипотермия не является непосредственной причиной смертности, она может увеличить риск развития сопутствующих заболеваний, таких как гипоксия, сепсис, гипогликемия, апноэ и плохая прибавка в весе, которые увеличивают риск смертности.
 11 Младенцы теряют тепло в результате излучения, испарения, теплопроводности и конвекции, и очень важно бороться с этими формами потери энергии, чтобы новорожденные оставались теплыми. 7 Тепловая защита признана ключевым компонентом основного ухода за новорожденными. Эффективные стратегии предотвращения развития неонатальной гипотермии состоят из теплого родильного зала, укутывания и сушки сразу после рождения, телесного контакта и метода кенгуру (KMC), грудного вскармливания, откладывания купания и взвешивания новорожденного, использования соответствующей одежды и постельные принадлежности, содержание новорожденного с матерью, обеспечение теплой транспортировки и реанимации в случае необходимости, а также повышение осведомленности и обучение методам неонатальной гипотермии. 7 Регулярный мониторинг температуры способствует раннему выявлению и лечению гипотермии. Однако регулярный мониторинг температуры в условиях ограниченных ресурсов остается сложной задачей из-за нехватки персонала и переполненности палат.
11 Младенцы теряют тепло в результате излучения, испарения, теплопроводности и конвекции, и очень важно бороться с этими формами потери энергии, чтобы новорожденные оставались теплыми. 7 Тепловая защита признана ключевым компонентом основного ухода за новорожденными. Эффективные стратегии предотвращения развития неонатальной гипотермии состоят из теплого родильного зала, укутывания и сушки сразу после рождения, телесного контакта и метода кенгуру (KMC), грудного вскармливания, откладывания купания и взвешивания новорожденного, использования соответствующей одежды и постельные принадлежности, содержание новорожденного с матерью, обеспечение теплой транспортировки и реанимации в случае необходимости, а также повышение осведомленности и обучение методам неонатальной гипотермии. 7 Регулярный мониторинг температуры способствует раннему выявлению и лечению гипотермии. Однако регулярный мониторинг температуры в условиях ограниченных ресурсов остается сложной задачей из-за нехватки персонала и переполненности палат. 6,11 Недостаток обученного персонала, дорогие ресурсы, плохое предоставление и качество ухода, а также ограниченное обучение матерей уходу за новорожденным еще больше затрудняют профилактику, выявление и лечение гипотермии. 6,10 Следовательно, неонатальная гипотермия плохо выявляется и остается невидимой проблемой общественного здравоохранения.
6,11 Недостаток обученного персонала, дорогие ресурсы, плохое предоставление и качество ухода, а также ограниченное обучение матерей уходу за новорожденным еще больше затрудняют профилактику, выявление и лечение гипотермии. 6,10 Следовательно, неонатальная гипотермия плохо выявляется и остается невидимой проблемой общественного здравоохранения.Распространенность неонатальной гипотермии варьируется в зависимости от страны и составляет от 11% до 95%, при этом самые высокие показатели распространенности наблюдаются в странах Африки к югу от Сахары. 12,13 Различия в дизайне исследования, исследуемой популяции, инструментах и месте измерения температуры, а также контекстуальные факторы между странами могут объяснить различия в распространенности гипотермии. Понимание распространенности и факторов, вызывающих неонатальную гипотермию в различных местных условиях, имеет важное значение. Предыдущие исследования выявили факторы, связанные с неонатальной гипотермией, в том числе неонатальные факторы (например, гестационный возраст, пол и масса тела при рождении), материнские факторы (например, образование, профессия и семейное положение) и факторы, связанные с беременностью (например, способ родов и местонахождение).
 доставки). 12–17 Недоношенные и маловесные дети подвергаются наибольшему риску гипотермии, поскольку у них меньше бурого жира, меньше подкожного жира и неэффективное метаболическое производство тепла. 8,13
доставки). 12–17 Недоношенные и маловесные дети подвергаются наибольшему риску гипотермии, поскольку у них меньше бурого жира, меньше подкожного жира и неэффективное метаболическое производство тепла. 8,13 Несмотря на то, что гипотермия является значительным фактором риска неонатальной смертности, она по-прежнему недостаточно изучена в условиях ограниченных ресурсов, а исследований, документирующих возникновение неонатальной гипотермии и идентифицирующих местные факторы риска, недостаточно. 12–17 Целью этого исследования было описание распространения неонатальной гипотермии и изучение факторов риска, связанных с неонатальной гипотермией у маловесных детей в Аккре, Гана. По оценкам, в Гане уровень неонатальной смертности составляет 23,1 случая смерти на 1000 живорождений, а 14% детей рождаются маловесными. 18
В настоящем исследовании проанализированы первичные данные, собранные в ходе исследования по оценке точности BEMPU® TempWatch (BEMPU Health, Бангалор, Карнатака, Индия), браслета для непрерывного мониторинга температуры, используемого для выявления неонатальной гипотермии.
 BEMPU® TempWatch состоит из силиконовой ленты с металлической чашкой термистора, которая издает звуковой сигнал и мигает оранжевым, когда температура тела падает ниже 36,5°C (рис. 1). 19 Браслет подходит для новорожденных весом до 3500 граммов. Эффективность BEMPU® TempWatch как инструмента для предупреждения лиц, осуществляющих уход, о неонатальной гипотермии оценивалась в нескольких исследованиях. Чувствительность и специфичность TempWatch при обнаружении гипотермии были 98,6% и 95% соответственно. 20 Новые данные свидетельствуют о том, что устройство улучшает раннее распознавание гипотермии и может увеличить прибавку в весе и способствовать развитию кенгуру. 19–23 Тем не менее, необходима дальнейшая проверка устройства. 23
BEMPU® TempWatch состоит из силиконовой ленты с металлической чашкой термистора, которая издает звуковой сигнал и мигает оранжевым, когда температура тела падает ниже 36,5°C (рис. 1). 19 Браслет подходит для новорожденных весом до 3500 граммов. Эффективность BEMPU® TempWatch как инструмента для предупреждения лиц, осуществляющих уход, о неонатальной гипотермии оценивалась в нескольких исследованиях. Чувствительность и специфичность TempWatch при обнаружении гипотермии были 98,6% и 95% соответственно. 20 Новые данные свидетельствуют о том, что устройство улучшает раннее распознавание гипотермии и может увеличить прибавку в весе и способствовать развитию кенгуру. 19–23 Тем не менее, необходима дальнейшая проверка устройства. 23 Рисунок 1. BEMPU TempWatch
Источник изображения: https://www.bempu.com/tempwatch
Настоящее исследование было проведено в клинической больнице Корле Бу в Аккре, Гана. Больница является крупнейшим специализированным центром в Западной Африке, вместимостью более 2000 коек и средней посещаемостью 1500 пациентов в день.
 Отделение интенсивной терапии новорожденных (ОИТН) клинической больницы Корле-Бу (KBTH) обеспечивает уход за недоношенными и тяжелобольными доношенными детьми и имеет номинальную вместимость 60 коек, подогревающих платформ и инкубаторов, хотя это количество часто превышается. Подразделение получает направления из медицинских учреждений в южной части страны. С 2011 по 2015 год среднее количество госпитализаций составляло 1843 человека в год, а общий уровень смертности — 19 человек..2%. 24 Как правило, младенцев, поступающих в отделение интенсивной терапии новорожденных, сортируют по их весу, при этом младенцы с массой тела менее 2000 граммов содержатся в инкубаторах с минимальной одеждой. Мониторы, прикрепленные к инкубаторам, отображают температуру воздуха в инкубаторе и регулируются по мере необходимости. Клинически стабильные дети с массой тела 2000 г находятся в кроватках, одеты и завернуты. Матерям младенцев разрешается находиться в отделении интенсивной терапии новорожденных в установленное время кормления младенцев для сцеживания грудного молока или непосредственного кормления грудью своих младенцев.
Отделение интенсивной терапии новорожденных (ОИТН) клинической больницы Корле-Бу (KBTH) обеспечивает уход за недоношенными и тяжелобольными доношенными детьми и имеет номинальную вместимость 60 коек, подогревающих платформ и инкубаторов, хотя это количество часто превышается. Подразделение получает направления из медицинских учреждений в южной части страны. С 2011 по 2015 год среднее количество госпитализаций составляло 1843 человека в год, а общий уровень смертности — 19 человек..2%. 24 Как правило, младенцев, поступающих в отделение интенсивной терапии новорожденных, сортируют по их весу, при этом младенцы с массой тела менее 2000 граммов содержатся в инкубаторах с минимальной одеждой. Мониторы, прикрепленные к инкубаторам, отображают температуру воздуха в инкубаторе и регулируются по мере необходимости. Клинически стабильные дети с массой тела 2000 г находятся в кроватках, одеты и завернуты. Матерям младенцев разрешается находиться в отделении интенсивной терапии новорожденных в установленное время кормления младенцев для сцеживания грудного молока или непосредственного кормления грудью своих младенцев. Пристроенная комната KMC вмещает до 6 пар мать-младенец.
Пристроенная комната KMC вмещает до 6 пар мать-младенец.Младенцы имели право участвовать в исследовании, если они соответствовали критериям включения: возраст менее 28 дней, поступление в отделение интенсивной терапии, маловесный вес и клиническая стабильность. Младенцы, матери которых были моложе 18 лет или которые должны были быть выписаны из отделения интенсивной терапии новорожденных в течение 24 часов, были исключены. Потенциально подходящие младенцы были определены местными медсестрами, проводившими исследование, которые затем обратились к их матерям, чтобы определить заинтересованность в участии в проверочном исследовании. Исследование было полностью разъяснено всем заинтересованным матерям. Перед сбором данных было получено письменное информированное согласие на участие в исследовании у матерей подходящих детей. Требуемый размер выборки, равный 255, был определен с помощью одновыборочного теста эквивалентности для пропорций с порогом эквивалентности, установленным на уровне 15 процентных пунктов, и при условии чувствительности 90 %, мощность 80 %, частота ошибок типа I 5 % и потери для последующего наблюдения 15 %.

После получения информированного согласия медицинские сестры-исследователи задавали матерям стандартную анкету для сбора социально-демографических данных об уровне образования, профессии, семейном положении, религии и этнической принадлежности. Анкета также собирала данные об анамнезе репродуктивной функции и здоровья матери (беременность, паритет, антенатальный уход (ДНП), осложнения беременности, способ родов и тип родов) и послеродовом анамнезе (пол ребенка, масса тела при рождении, баллы по шкале Апгар). через 1 и 5 минут после рождения). После заполнения вопросника медсестры-исследователи прикладывали часы BEMPU® TempWatch к запястьям младенцев и записывали исходную информацию о методах теплового ухода; в частности, был ли ребенок завернут или покрыт одеялом или тканью, был ли он в шапке или кепке, в подгузнике, в носках, в варежках или перчатках и проходил ли лечение в инкубаторе. Медсестры-исследователи затем регистрировали подмышечную температуру младенцев каждые 4 часа с помощью цифровых термометров в течение 24-часового периода наблюдения.
 Цифровые термометры имеют точность около 0,02 ° C при использовании для измерения из подмышечной области. 25 Всякий раз, когда звучал сигнал тревоги на BEMPU® TempWatch, указывающий на эпизод гипотермии, медсестры, проводившие исследование, измеряли температуру в подмышечной впадине у младенца, снова документировали практику теплового ухода и записывали все предпринятые клинические действия. У каждого младенца в течение 24-часового периода наблюдения было зафиксировано не менее семи температурных показателей. Данные собирались и хранились на планшетах Android с помощью программного обеспечения Open Data Kit (ODK), а затем загружались на защищенный сервер.
Цифровые термометры имеют точность около 0,02 ° C при использовании для измерения из подмышечной области. 25 Всякий раз, когда звучал сигнал тревоги на BEMPU® TempWatch, указывающий на эпизод гипотермии, медсестры, проводившие исследование, измеряли температуру в подмышечной впадине у младенца, снова документировали практику теплового ухода и записывали все предпринятые клинические действия. У каждого младенца в течение 24-часового периода наблюдения было зафиксировано не менее семи температурных показателей. Данные собирались и хранились на планшетах Android с помощью программного обеспечения Open Data Kit (ODK), а затем загружались на защищенный сервер.Первичным результатом этого анализа была подмышечная температура, измеренная цифровым термометром. Изучались независимые переменные: беременность, паритет, одноплодные или многоплодные роды, способ родоразрешения (вагинальные или кесарево сечение), пол младенца, возраст, масса тела при рождении, гестационный возраст при рождении, оценка по шкале Апгар на 1-й и 5-й минутах, текущее кормление и тепловые практики.
 в момент рождения и в момент регистрации температуры. Одномерные и многомерные линейные регрессии были выполнены для изучения связи между температурой и различными независимыми переменными. В связи с многократными наблюдениями за каждым младенцем мы использовали обобщенные оценочные уравнения (GEE). Одномерные ассоциации с P <0,1 были включены в исходную многомерную модель. Для выбора окончательной многомерной модели использовалась пошаговая процедура с критерием включения 0,05. Уровень статистической значимости был установлен на уровне P <0,05. Изменения температуры, доверительные интервалы и p-значения сообщались для каждой независимой переменной. Все статистические анализы проводились с использованием STATA 17.0 (StataCorp LLC, Колледж-Стейшн, Техас, США).
в момент рождения и в момент регистрации температуры. Одномерные и многомерные линейные регрессии были выполнены для изучения связи между температурой и различными независимыми переменными. В связи с многократными наблюдениями за каждым младенцем мы использовали обобщенные оценочные уравнения (GEE). Одномерные ассоциации с P <0,1 были включены в исходную многомерную модель. Для выбора окончательной многомерной модели использовалась пошаговая процедура с критерием включения 0,05. Уровень статистической значимости был установлен на уровне P <0,05. Изменения температуры, доверительные интервалы и p-значения сообщались для каждой независимой переменной. Все статистические анализы проводились с использованием STATA 17.0 (StataCorp LLC, Колледж-Стейшн, Техас, США).Вопросы этики
Этическое одобрение исследований на людях получено от Institutional Review Boards (IRB) Университета Южной Каролины (Pro 00095600) и клинической больнице Корле Бу (KBTH-IRB/00052/2020).
 Письменное информированное согласие на участие в исследовании было получено от матерей младенцев на местном языке или английском языке до включения в исследование.
Письменное информированное согласие на участие в исследовании было получено от матерей младенцев на местном языке или английском языке до включения в исследование.В период с мая 2021 г. по январь 2022 г. 255 соответствующих критериям младенцев в клинической больнице Корле Бу были зарегистрированы и наблюдались в течение 24 часов. Из-за отсутствия данных о температуре один младенец был исключен из настоящего анализа. Из 254 включенных новорожденных большинство были недоношенными (92,9%), родоразрешены с помощью кесарева сечения (53,9%).%), находились на исключительно грудном вскармливании (70,5 %) и имели оценку по шкале APGAR ≤6 через 1 минуту после рождения (69,2 %) (таблица 1). Менее половины младенцев были мужского пола (42,1%), ОНМТ (< 1500 г) (49,6%), часть многоплодных родов (24,0%), крайне недоношенных (<28 недель гестации, 8,3%) и в возрасте семи дней или менее в возрасте охват (47,6%). Большинство матерей младенцев были старше 25 лет (71,7%), состояли в браке (64,8%), имели среднее или высшее образование (71,3%), посещали по крайней мере одно посещение ДРП во время беременности (9).
 4,5%), были повторнородящими (52,6%) и повторнобеременными (65,3%).
4,5%), были повторнородящими (52,6%) и повторнобеременными (65,3%).Таблица 1. Характеристики участников исследования клинической больницы Корле-Бу в Аккре, Гана (n=254)
п % Характеристики матери Возраст 18-25 лет 72 28,3 26-32 года 79 31,1 33 года и старше 103 40,6 Высшее законченное образование Без образования 10 3,9 Первичный 13 5.1 Средний 50 19,7 Среднее или выше 181 71,3 Семейное положение Никогда не был женат 49 19,4 Женат 164 65,1 Жить вместе 39 15,5 Работающий 179 70,8 Характеристики родов и беременности Первородящая 88 34,7 Первенство 120 47,4 Посещали как минимум 1 дородовой визит 239 94,5 Многоплодие 61 24,0 Способ доставки Вагинальный 117 46,1 С-секция 137 53,9 Характеристики младенцев Мужской 107 42,1 Возраст при зачислении 0-6 дней 121 47,6 7-28 дней 133 52,3 Гестационный возраст при рождении 236 92,9 Крайне недоношенные (<28 недель) 21 8,3 Очень недоношенные (28-32 недели) 117 54,3 От средней до поздней недоношенности (33-36 недель) 98 38,6 Срок (≥37 недель) 18 7,1 Очень низкая масса тела при рождении (<1500 г) 126 49,6 Оценка по шкале Апгар на 1-й минуте ≤ 6 171 69,2 Оценка по шкале Апгар через 5 минут ≤ 6 83 33,6 Подача тока Исключительно грудное вскармливание 179 70,5 Формула 7 2,8 Смесь и грудное вскармливание 9 3,5 Внутривенные жидкости 59 23,2 Из 1948 показаний аксиллярной температуры, полученных у 254 младенцев, 44,5% были гипотермическими (<36,5°C).
 26,5% показателей температуры соответствовали критериям легкой гипотермии (36,0-36,4°С), а 18,0% — критериям умеренной гипотермии (32,0-35,9°С). Ни одно из показаний не соответствовало критериям тяжелой гипотермии (<32,0°C). В целом в этой популяции преобладала легкая и умеренная гипотермия: у 85,8% младенцев хотя бы одно значение температуры было ниже 36,5 °C в течение 24-часового периода наблюдения. Частота гипотермии была выше среди детей с ОНМТ (86,3%) и крайне недоношенных детей (100%).
26,5% показателей температуры соответствовали критериям легкой гипотермии (36,0-36,4°С), а 18,0% — критериям умеренной гипотермии (32,0-35,9°С). Ни одно из показаний не соответствовало критериям тяжелой гипотермии (<32,0°C). В целом в этой популяции преобладала легкая и умеренная гипотермия: у 85,8% младенцев хотя бы одно значение температуры было ниже 36,5 °C в течение 24-часового периода наблюдения. Частота гипотермии была выше среди детей с ОНМТ (86,3%) и крайне недоношенных детей (100%).Модели одномерной линейной регрессии выявили факторы, в значительной степени связанные с температурой новорожденных (таблица 2). Многоплодие, ОНМТ и более низкий гестационный возраст при рождении ассоциировались с более низкими температурами, в то время как первородство в среднем ассоциировалось с более высокими температурами. Из рассмотренных тепловых практик только контакт кожа к коже, обертывание во время регистрации температуры, ношение подгузника во время регистрации температуры и пребывание в инкубаторе во время измерения температуры защищали от более низких температур ( P <0,05).
 Не было выявлено значимой связи между температурой и ношением шапки/кепки, носков или перчаток/рукавиц ( P >0,05). После поправки на значимые ковариаты модель многомерной линейной регрессии показала, что по сравнению с детьми, находящимися на исключительно грудном вскармливании, у детей на смешанном вскармливании (смеси и грудного молока) температура была ниже на 1,08°C, а у детей на искусственном вскармливании температура была выше на 0,38°C. . Младенцы с ОНМТ имели более низкую среднюю температуру по сравнению с детьми, не имевшими ОНМТ при рождении (β=-0,14°C), в то время как у крайне недоношенных детей температура была ниже, чем у доношенных детей (β=-0,70°C). Младенцы, имевшие контакт кожа к коже при рождении, были завернуты и помещены в инкубатор, у них была более высокая температура (0,20°C, 0,36°C и 0,67°C соответственно).
Не было выявлено значимой связи между температурой и ношением шапки/кепки, носков или перчаток/рукавиц ( P >0,05). После поправки на значимые ковариаты модель многомерной линейной регрессии показала, что по сравнению с детьми, находящимися на исключительно грудном вскармливании, у детей на смешанном вскармливании (смеси и грудного молока) температура была ниже на 1,08°C, а у детей на искусственном вскармливании температура была выше на 0,38°C. . Младенцы с ОНМТ имели более низкую среднюю температуру по сравнению с детьми, не имевшими ОНМТ при рождении (β=-0,14°C), в то время как у крайне недоношенных детей температура была ниже, чем у доношенных детей (β=-0,70°C). Младенцы, имевшие контакт кожа к коже при рождении, были завернуты и помещены в инкубатор, у них была более высокая температура (0,20°C, 0,36°C и 0,67°C соответственно).Таблица 2. Результаты одномерной и многомерной линейной регрессии для связи младенцев, родов и беременности, а также практики теплового ухода с температурой
Одномерный Многомерный β (95% ДИ) р β (95% ДИ) р Характеристики родов и беременности Первородящая 0,06 (-0,04, 0,16) 0,3 Первенство 0,12 (0,02, 0,21) 0,02 Многоплодие -0,24 (-0,35, -0,13) <0,001 Способ доставки Вагинальный Артикул С-секция -0,08 (-0,18, 0,01) 0,1 Характеристики младенцев Мужской -0,03 (-0,12, 0,07) 0,6 Менее 7 дней при регистрации 0,03 (-0,38, 0,09) 0,4 Гестационный возраст при рождении Крайне недоношенные (<28 недель) -0,44 (-0,61, -0,28) <0,001 -0,73 (-0,90, 0,57) <0,001 Очень недоношенные (28-32 недели) -0,08 (-0,21, 0,06) 0,3 -0,25 (-0,38, -0,12) 0,001 От средней до поздней недоношенности (33-36 недель) -0,17 (-0,30, -0,03) 0,02 -0,26 (-0,39, -0,14) <0,001 Срок (≥37 недель) Ссылка Артикул Очень низкая масса тела при рождении (<1500 г) -0,07 (-0,14, -0,002) 0,04 -0,11 (-0,18, -0,04) 0,003 Оценка по шкале Апгар на 1-й минуте ≤ 6 0,03 (-0,07, 0,14) 0,6 Оценка по шкале Апгар через 5 минут ≤ 6 0,07 (-0,03, 0,17) 0,2 Подача тока Исключительно грудное вскармливание Артикул Артикул Формула 0,41 (0,12, 0,70) 0,005 0,38 (0,19, 0,57) <0,001 Смесь и грудное вскармливание -1,20 (-0,14, 0,97) <0,001 -1,06 (-1,22, -0,91) <0,001 Внутривенные жидкости -0,06 (-0,17, 0,05) 0,3 -0,08 (-0,15, -0,006) <0,001 Практика термального ухода Кожа к коже при рождении 0,26 (0,17,0,36) <0,001 0,21 (0,15, 0,27) <0,001 Упаковано при измерении температуры 0,12 (0,008, 0,22) 0,04 0,37 (0,27, 0,47) <0,001 Инкубатор при считывании температуры 0,39 (029, 0,49) <0,001 0,68 (0,58, 0,78) <0,001 Ношение шляпы/кепки при измерении температуры -0,04 (-0,17, 0,09) 0,5 Ношение перчаток при измерении температуры -0,12 (-0,51, 0,28) 0,6 Ношение подгузника при измерении температуры 0,61 (0,13, 1,08) 0,01 Ношение носков при измерении температуры -0,12 (-0,36, 0,12) 0,3 Целью этого исследования было описание распространенности неонатальной гипотермии и связанных с ней факторов риска в Аккре, Гана.
 Некоторые из результатов исследования имеют значение для теплового ухода за маловесными младенцами в условиях ограниченных ресурсов. Во-первых, у 85,8% новорожденных хотя бы один раз в течение 24-часового периода наблюдения наблюдалась гипотермия. Этот показатель распространенности находится в пределах диапазона, ранее описанного в других условиях (от 8,1% до 9%).4,9%). 13 Однако коэффициент распространенности находится на верхней границе диапазона, скорее всего, потому, что LBW был одним из критериев включения в это исследование. Около половины (49,6%) младенцев в этом исследовании были ОНМТ, и большинство (92,9%) были недоношенными. У 86,3% новорожденных с ОНМТ был эпизод гипотермии в течение 24-часового периода наблюдения; среди глубоконедоношенных новорожденных у всех (100%) был эпизод гипотермии в течение 24-часового периода наблюдения. После поправки на другие ковариаты, включая использование инкубатора, разница в неонатальной температуре между ОНМТ и другими младенцами составила 0,11 °C, а разница между крайне недоношенными и доношенными детьми составила 0,73 °C.
Некоторые из результатов исследования имеют значение для теплового ухода за маловесными младенцами в условиях ограниченных ресурсов. Во-первых, у 85,8% новорожденных хотя бы один раз в течение 24-часового периода наблюдения наблюдалась гипотермия. Этот показатель распространенности находится в пределах диапазона, ранее описанного в других условиях (от 8,1% до 9%).4,9%). 13 Однако коэффициент распространенности находится на верхней границе диапазона, скорее всего, потому, что LBW был одним из критериев включения в это исследование. Около половины (49,6%) младенцев в этом исследовании были ОНМТ, и большинство (92,9%) были недоношенными. У 86,3% новорожденных с ОНМТ был эпизод гипотермии в течение 24-часового периода наблюдения; среди глубоконедоношенных новорожденных у всех (100%) был эпизод гипотермии в течение 24-часового периода наблюдения. После поправки на другие ковариаты, включая использование инкубатора, разница в неонатальной температуре между ОНМТ и другими младенцами составила 0,11 °C, а разница между крайне недоношенными и доношенными детьми составила 0,73 °C. Эти результаты согласуются с предыдущими исследованиями, которые показали более высокую частоту гипотермии среди детей с низкой массой тела и недоношенных детей. 12–17
Эти результаты согласуются с предыдущими исследованиями, которые показали более высокую частоту гипотермии среди детей с низкой массой тела и недоношенных детей. 12–17 В исследовании также подчеркивается важность теплового ухода для профилактики и лечения неонатальной гипотермии. Неудивительно, что младенцы, у которых был контакт кожа к коже при рождении, были завернуты и находились в инкубаторе во время измерения температуры, у них была более высокая температура. Кроме того, у детей, находящихся на смешанном вскармливании, температура тела была значительно ниже, чем у детей, находящихся на исключительно грудном вскармливании. Недостаточное финансирование систем здравоохранения, нехватка кадровых ресурсов для здравоохранения, отсутствие надежного электричества и ограниченные финансовые ресурсы препятствуют использованию инкубаторов и других технологий в условиях ограниченных ресурсов. 26 Тем не менее, телесный контакт широко известен как недорогой, эффективный и безопасный способ достижения и поддержания стабильной температуры новорожденного и предотвращения гипотермии, особенно среди клинически стабильных маловесных и недоношенных детей в условиях ограниченных ресурсов.
 27 Уход за матерями методом кенгуру (KMC), который включает ранний, непрерывный и длительный телесный контакт и грудное вскармливание, снижает гипотермию, частоту инфекций и риск смертности, одновременно способствуя увеличению веса и вскармливанию привязанность родитель-ребенок. 28–30 Несмотря на призывы к всеобщему охвату кенгуру для маловесных и недоношенных детей во всем континууме учреждение-сообщество, внедрение и расширение масштабов кенгуру было медленным из-за структурных, экономических, логистических и социальных барьеров. 31 Должен быть достигнут прогресс в расширении МК и вмешательств, дополняющих МК, таких как непрерывный мониторинг температуры.
27 Уход за матерями методом кенгуру (KMC), который включает ранний, непрерывный и длительный телесный контакт и грудное вскармливание, снижает гипотермию, частоту инфекций и риск смертности, одновременно способствуя увеличению веса и вскармливанию привязанность родитель-ребенок. 28–30 Несмотря на призывы к всеобщему охвату кенгуру для маловесных и недоношенных детей во всем континууме учреждение-сообщество, внедрение и расширение масштабов кенгуру было медленным из-за структурных, экономических, логистических и социальных барьеров. 31 Должен быть достигнут прогресс в расширении МК и вмешательств, дополняющих МК, таких как непрерывный мониторинг температуры.Это исследование имеет несколько ограничений. В результате исследования могли быть затронуты методы термального ухода. Период мониторинга составлял 24 часа, и никакой дополнительной информации о младенцах после этого периода не поступало. Поскольку в исследование были включены только младенцы с низкой массой тела, поступившие в отделение интенсивной терапии одной третичной больницы, результаты не могут быть распространены на другие медицинские учреждения и младенцев в общественных условиях.

Несмотря на ограничения, большое бремя неонатальной гипотермии требует приоритизации этой невидимой проблемы общественного здравоохранения. Будущие исследования должны оценить обучение медсестер и матерей по тепловой защите в учреждениях в странах с низким уровнем ресурсов, чтобы повысить осведомленность и снизить частоту гипотермии. В исследованиях также следует оценить более широкое использование контакта кожа к коже для усиления тепловой защиты младенцев с малым весом. Медицинские работники должны признать гипотермию у маловесных детей грудного возраста невидимой проблемой общественного здравоохранения и работать над оптимальным управлением температурным режимом.
Благодарности
Авторы хотели бы поблагодарить сотрудников клинической больницы Корле-Бу, а также матерей и новорожденных, включенных в исследование.
Финансирование
Работа выполнена при поддержке Исследовательского фонда Thrasher (грант 15194).

Критерии терапевтической гипотермии:
Классификация Шкала гипоксически-ишемической энцефалопатии
| Легкая Энцефалопатия | Умеренная энцефалопатия | Тяжелая энцефалопатия | |
| Уровень сознания | Гипероповещение | Летаргический | Ступор/кома |
| Спонтанная активность | Обычный | Снижение активности | Нет активности |
| Поза | Нормальное легкое дистальное сгибание | Дистальное сгибание/полное разгибание | Децеребрация |
| Тон | Гипотонический | Вялый | |
| Примитивные рефлексы | Слабое сосание/Сильное муро | Слабое сосание/неполный Моро | Отсутствие сосания/отсутствие Моро |
| Вегетативная система: Зрачок Частота сердечных сокращений Дыхание | Нормальная тахикардия | Ограниченная брадикардия Периодическое дыхание | Расширенное/нереактивное вариабельное апноэ |
Таблица адаптирована из Sarnat el al Pediatric Neurology 113 (2020) 75-79
6. Умеренная или резко выраженная аномальная фоновая активность на амплитудно-интегрированной ЭЭГ, т. е. прерывистая, подавление всплесков или низкий вольтаж +/-
Умеренная или резко выраженная аномальная фоновая активность на амплитудно-интегрированной ЭЭГ, т. е. прерывистая, подавление всплесков или низкий вольтаж +/-
7. По усмотрению консультанта по неонатологии, чтобы начать терапевтическое охлаждение
Индуцирование гипотермии
Целью охлаждения является достижение целевой температуры в течение 1 часа после начала (ректальная температура между 33,0°C – 34,0°C). Общий период охлаждения и согревания составляет 84 часа, состоит из 2 фаз:
Оборудование:
Оценка и управление сестринским делом
Мониторинг
Системные эффекты
Температура мониторинг должен быть непрерывным на протяжении всего лечения
Тщательное неврологическое наблюдение
Доступ : Линии локализации перед охлаждением по мере снижения перфузии: предпочтительнее двухпросветная УФС и UAC/периферическая артериальная линия.
Анализы крови : ABG, электролиты, LFTS, глюкоза, коагуляция, FBE
Жидкости : Большинству младенцев ограничивают потребление жидкости, чтобы избежать перегрузки жидкостью и отека мозга.
Седация : Младенцам может потребоваться инфузия низких доз морфина для оптимизации комфорта и эффективности процесса охлаждения. Контролируйте комфорт с помощью модифицированного инструмента оценки боли (mPAT).
Сепсис
Кожа
Согревание
Документация
Осложнения
Осложнения чаще возникают или ухудшаются при более низких температурах. Избегайте переохлаждения пациента.
Семейный уход
Объясните членам семьи причины использования гипотермии и ожидаемую продолжительность лечения. Объясните семье, что их ребенку будет холодно во время лечения, и заверите их, что их ребенку будет комфортно во время лечения. Поощряйте сближение, позволяя родителям прикасаться к своему ребенку, делать
смена подгузников и т. д.
Объясните семье, что их ребенку будет холодно во время лечения, и заверите их, что их ребенку будет комфортно во время лечения. Поощряйте сближение, позволяя родителям прикасаться к своему ребенку, делать
смена подгузников и т. д.
Сопутствующая документация
Звенья
Таблица фактических данных
Таблицу фактических данных для данного руководства можно найти здесь.


 Клетки умирают в ответ на различные раздражители, и во время апоптоза они делают это контролируемым и регулируемым образом. Апоптоз — это процесс, в котором клетки играют активную роль в собственной гибели, и его часто называют клеточным самоубийством.
Клетки умирают в ответ на различные раздражители, и во время апоптоза они делают это контролируемым и регулируемым образом. Апоптоз — это процесс, в котором клетки играют активную роль в собственной гибели, и его часто называют клеточным самоубийством. 
 е. активное кровотечение), серьезные врожденные аномалии, выживание маловероятно (это
следует обсудить с третичным неонатологом или консультантом PIPER). Персистирующая легочная гипертензия (PPHN) не должна рассматриваться как противопоказание к началу терапевтической гипотермии при ГИЭ.
е. активное кровотечение), серьезные врожденные аномалии, выживание маловероятно (это
следует обсудить с третичным неонатологом или консультантом PIPER). Персистирующая легочная гипертензия (PPHN) не должна рассматриваться как противопоказание к началу терапевтической гипотермии при ГИЭ. Не кормите грудью в инкубаторе.
Не кормите грудью в инкубаторе. Младенцам могут потребоваться пломбы и инотропы (сначала устранить гиповолемию).
Младенцам могут потребоваться пломбы и инотропы (сначала устранить гиповолемию). 

 Следите за признаками неадекватной седации: увеличение ЧСС, озноб, затрудненное дыхание.
Следите за признаками неадекватной седации: увеличение ЧСС, озноб, затрудненное дыхание.  Это происходит редко, предположительно потому, что бурый жир более чувствителен к гипоксии и
ухудшается при охлаждении. Это также может привести к гиперкальциемии, гиперлипидемии и тромбоцитопении
Это происходит редко, предположительно потому, что бурый жир более чувствителен к гипоксии и
ухудшается при охлаждении. Это также может привести к гиперкальциемии, гиперлипидемии и тромбоцитопении
 Дж., Вагнер, К.Л., Катиканени, Л.П., Халси, Т.С., Басс, В.Т., Кауфман, Д.А. и др. . (2005) Умеренная гипотермия при неонатальной энцефалопатии: эффективность
результаты. Детская неврология. 32: 11-7 . Гипотермическая нейропротекция. 27 74.
Дж., Вагнер, К.Л., Катиканени, Л.П., Халси, Т.С., Басс, В.Т., Кауфман, Д.А. и др. . (2005) Умеренная гипотермия при неонатальной энцефалопатии: эффективность
результаты. Детская неврология. 32: 11-7 . Гипотермическая нейропротекция. 27 74. Открытие педиатрии BMJ.
Открытие педиатрии BMJ. Архив детской подростковой медицины, 161: 951-8.
Архив детской подростковой медицины, 161: 951-8.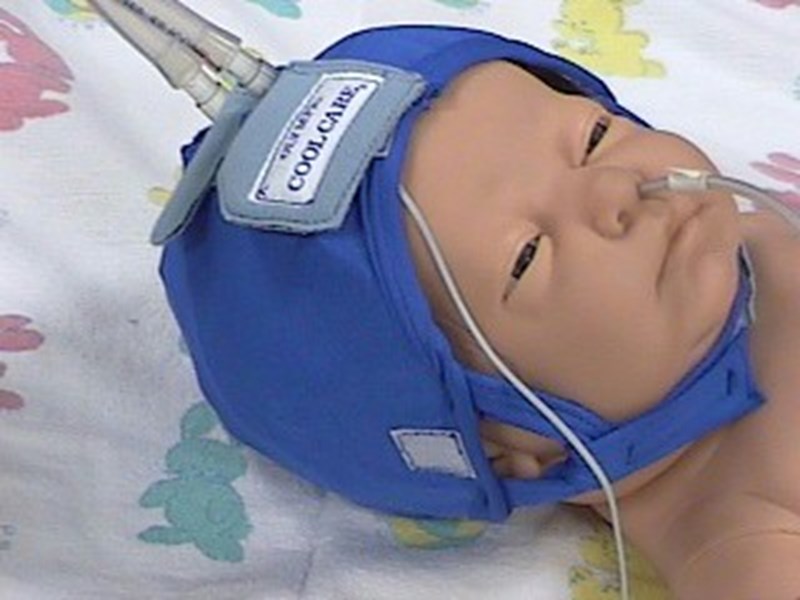 1 Только в 2020 году во всем мире умерло около 5 миллионов детей в возрасте до 5 лет. ; из них 2,4 миллиона умерли в неонатальный период, в первые 28 дней жизни. 2 Глобальный коэффициент неонатальной смертности (NMR) составляет 17 смертей на 1000 живорождений, причем этот показатель непропорционально выше в странах Африки к югу от Сахары (27 смертей на 1000 живорождений). 2 Ведущими причинами неонатальной смертности являются преждевременные роды (35%), интранатальные осложнения (24%) и инфекции (15%). 3 ЦУР 3 включает задачи по снижению ЧСС до 12 смертей на 1000 живорождений и коэффициента смертности детей в возрасте до 5 лет (U5MR) до 25 смертей на 1000 живорождений во всех странах к 2030 году. 1 Прогресс в достижении этих целей была заметно неравномерной по странам и между регионами, и пандемия COVID-19, вероятно, может свести на нет недавние достижения в области выживаемости детей. 2,4 В целом, лишь несколько стран находятся на пути к достижению целей NMR и U5MR к 2030 году.
1 Только в 2020 году во всем мире умерло около 5 миллионов детей в возрасте до 5 лет. ; из них 2,4 миллиона умерли в неонатальный период, в первые 28 дней жизни. 2 Глобальный коэффициент неонатальной смертности (NMR) составляет 17 смертей на 1000 живорождений, причем этот показатель непропорционально выше в странах Африки к югу от Сахары (27 смертей на 1000 живорождений). 2 Ведущими причинами неонатальной смертности являются преждевременные роды (35%), интранатальные осложнения (24%) и инфекции (15%). 3 ЦУР 3 включает задачи по снижению ЧСС до 12 смертей на 1000 живорождений и коэффициента смертности детей в возрасте до 5 лет (U5MR) до 25 смертей на 1000 живорождений во всех странах к 2030 году. 1 Прогресс в достижении этих целей была заметно неравномерной по странам и между регионами, и пандемия COVID-19, вероятно, может свести на нет недавние достижения в области выживаемости детей. 2,4 В целом, лишь несколько стран находятся на пути к достижению целей NMR и U5MR к 2030 году.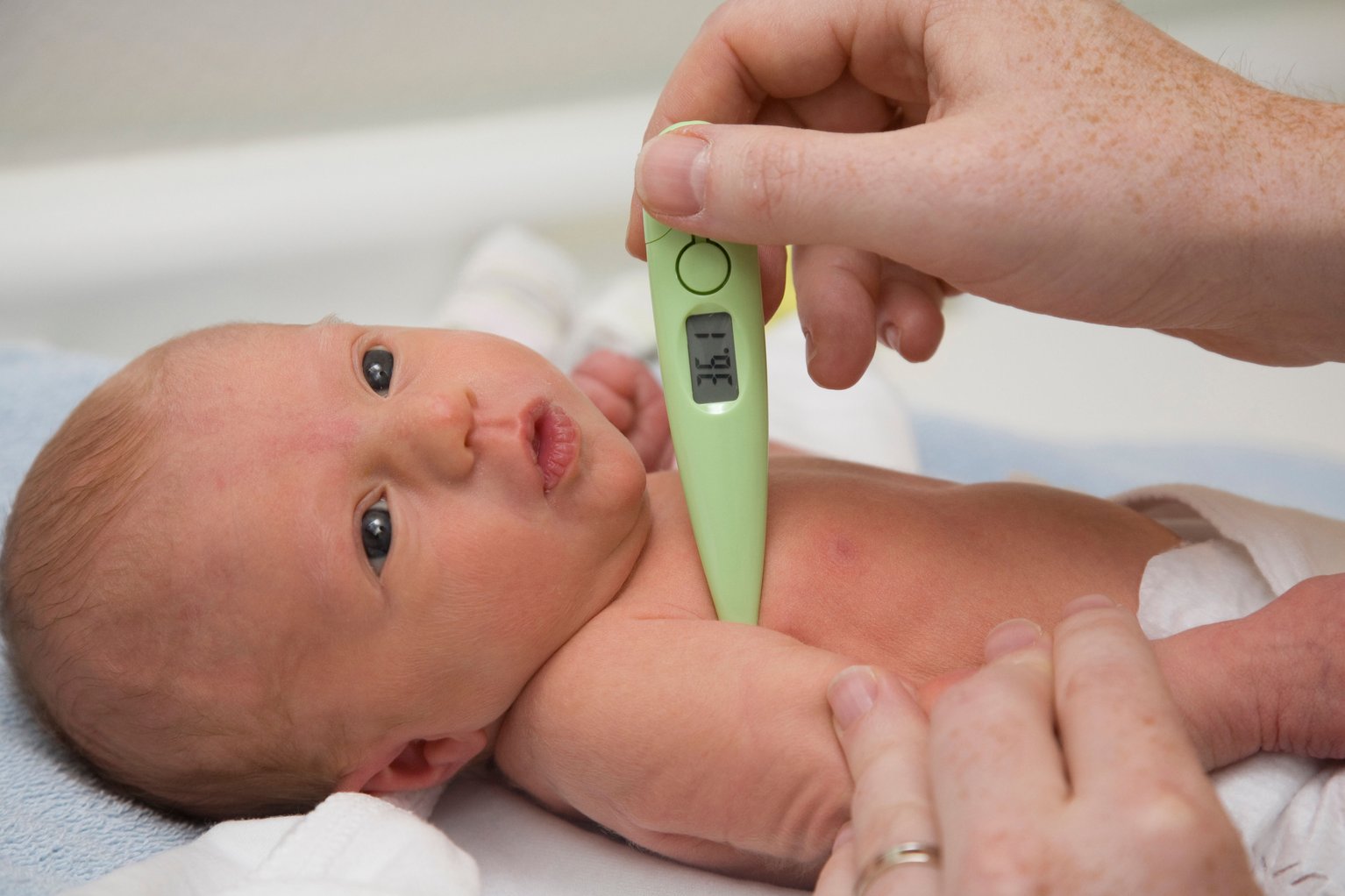 Если нынешние тенденции сохранятся, две трети стран Африки к югу от Сахары не достигнут целей. 5 Ускоренный прогресс в достижении незавершенной повестки дня в области устойчивого развития требует новых парадигм, стратегического мышления и инновационных подходов для снижения детской смертности, особенно в критический неонатальный период.
Если нынешние тенденции сохранятся, две трети стран Африки к югу от Сахары не достигнут целей. 5 Ускоренный прогресс в достижении незавершенной повестки дня в области устойчивого развития требует новых парадигм, стратегического мышления и инновационных подходов для снижения детской смертности, особенно в критический неонатальный период. 11 Младенцы теряют тепло в результате излучения, испарения, теплопроводности и конвекции, и очень важно бороться с этими формами потери энергии, чтобы новорожденные оставались теплыми. 7 Тепловая защита признана ключевым компонентом основного ухода за новорожденными. Эффективные стратегии предотвращения развития неонатальной гипотермии состоят из теплого родильного зала, укутывания и сушки сразу после рождения, телесного контакта и метода кенгуру (KMC), грудного вскармливания, откладывания купания и взвешивания новорожденного, использования соответствующей одежды и постельные принадлежности, содержание новорожденного с матерью, обеспечение теплой транспортировки и реанимации в случае необходимости, а также повышение осведомленности и обучение методам неонатальной гипотермии. 7 Регулярный мониторинг температуры способствует раннему выявлению и лечению гипотермии. Однако регулярный мониторинг температуры в условиях ограниченных ресурсов остается сложной задачей из-за нехватки персонала и переполненности палат.
11 Младенцы теряют тепло в результате излучения, испарения, теплопроводности и конвекции, и очень важно бороться с этими формами потери энергии, чтобы новорожденные оставались теплыми. 7 Тепловая защита признана ключевым компонентом основного ухода за новорожденными. Эффективные стратегии предотвращения развития неонатальной гипотермии состоят из теплого родильного зала, укутывания и сушки сразу после рождения, телесного контакта и метода кенгуру (KMC), грудного вскармливания, откладывания купания и взвешивания новорожденного, использования соответствующей одежды и постельные принадлежности, содержание новорожденного с матерью, обеспечение теплой транспортировки и реанимации в случае необходимости, а также повышение осведомленности и обучение методам неонатальной гипотермии. 7 Регулярный мониторинг температуры способствует раннему выявлению и лечению гипотермии. Однако регулярный мониторинг температуры в условиях ограниченных ресурсов остается сложной задачей из-за нехватки персонала и переполненности палат.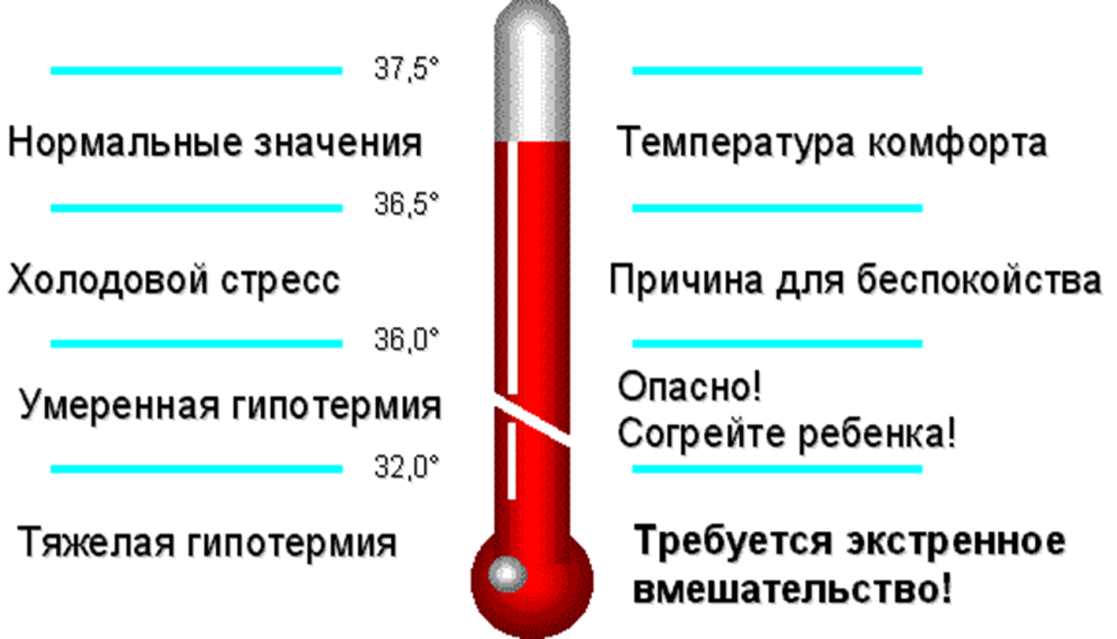 6,11 Недостаток обученного персонала, дорогие ресурсы, плохое предоставление и качество ухода, а также ограниченное обучение матерей уходу за новорожденным еще больше затрудняют профилактику, выявление и лечение гипотермии. 6,10 Следовательно, неонатальная гипотермия плохо выявляется и остается невидимой проблемой общественного здравоохранения.
6,11 Недостаток обученного персонала, дорогие ресурсы, плохое предоставление и качество ухода, а также ограниченное обучение матерей уходу за новорожденным еще больше затрудняют профилактику, выявление и лечение гипотермии. 6,10 Следовательно, неонатальная гипотермия плохо выявляется и остается невидимой проблемой общественного здравоохранения. доставки). 12–17 Недоношенные и маловесные дети подвергаются наибольшему риску гипотермии, поскольку у них меньше бурого жира, меньше подкожного жира и неэффективное метаболическое производство тепла. 8,13
доставки). 12–17 Недоношенные и маловесные дети подвергаются наибольшему риску гипотермии, поскольку у них меньше бурого жира, меньше подкожного жира и неэффективное метаболическое производство тепла. 8,13 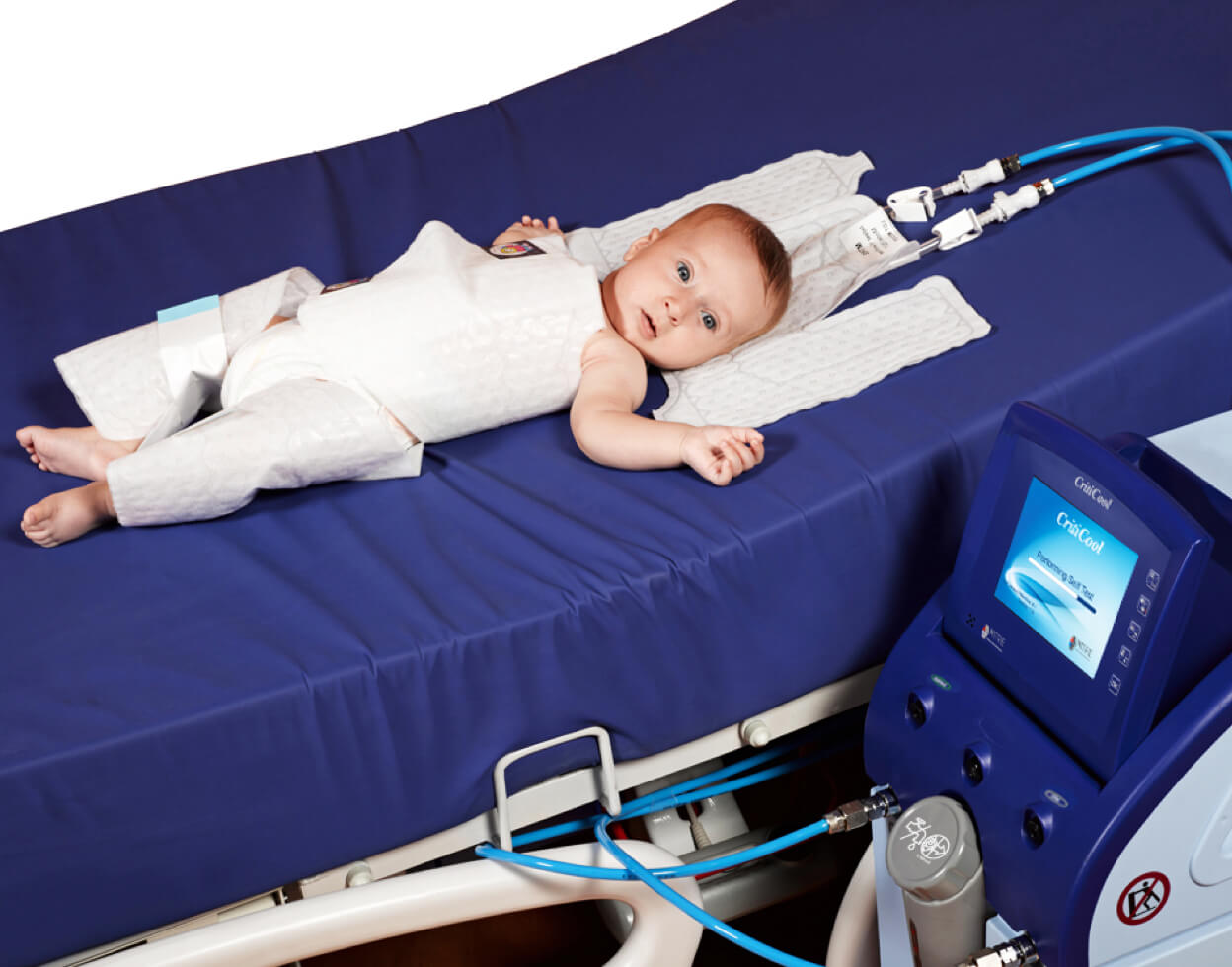 BEMPU® TempWatch состоит из силиконовой ленты с металлической чашкой термистора, которая издает звуковой сигнал и мигает оранжевым, когда температура тела падает ниже 36,5°C (рис. 1). 19 Браслет подходит для новорожденных весом до 3500 граммов. Эффективность BEMPU® TempWatch как инструмента для предупреждения лиц, осуществляющих уход, о неонатальной гипотермии оценивалась в нескольких исследованиях. Чувствительность и специфичность TempWatch при обнаружении гипотермии были 98,6% и 95% соответственно. 20 Новые данные свидетельствуют о том, что устройство улучшает раннее распознавание гипотермии и может увеличить прибавку в весе и способствовать развитию кенгуру. 19–23 Тем не менее, необходима дальнейшая проверка устройства. 23
BEMPU® TempWatch состоит из силиконовой ленты с металлической чашкой термистора, которая издает звуковой сигнал и мигает оранжевым, когда температура тела падает ниже 36,5°C (рис. 1). 19 Браслет подходит для новорожденных весом до 3500 граммов. Эффективность BEMPU® TempWatch как инструмента для предупреждения лиц, осуществляющих уход, о неонатальной гипотермии оценивалась в нескольких исследованиях. Чувствительность и специфичность TempWatch при обнаружении гипотермии были 98,6% и 95% соответственно. 20 Новые данные свидетельствуют о том, что устройство улучшает раннее распознавание гипотермии и может увеличить прибавку в весе и способствовать развитию кенгуру. 19–23 Тем не менее, необходима дальнейшая проверка устройства. 23  Отделение интенсивной терапии новорожденных (ОИТН) клинической больницы Корле-Бу (KBTH) обеспечивает уход за недоношенными и тяжелобольными доношенными детьми и имеет номинальную вместимость 60 коек, подогревающих платформ и инкубаторов, хотя это количество часто превышается. Подразделение получает направления из медицинских учреждений в южной части страны. С 2011 по 2015 год среднее количество госпитализаций составляло 1843 человека в год, а общий уровень смертности — 19 человек..2%. 24 Как правило, младенцев, поступающих в отделение интенсивной терапии новорожденных, сортируют по их весу, при этом младенцы с массой тела менее 2000 граммов содержатся в инкубаторах с минимальной одеждой. Мониторы, прикрепленные к инкубаторам, отображают температуру воздуха в инкубаторе и регулируются по мере необходимости. Клинически стабильные дети с массой тела 2000 г находятся в кроватках, одеты и завернуты. Матерям младенцев разрешается находиться в отделении интенсивной терапии новорожденных в установленное время кормления младенцев для сцеживания грудного молока или непосредственного кормления грудью своих младенцев.
Отделение интенсивной терапии новорожденных (ОИТН) клинической больницы Корле-Бу (KBTH) обеспечивает уход за недоношенными и тяжелобольными доношенными детьми и имеет номинальную вместимость 60 коек, подогревающих платформ и инкубаторов, хотя это количество часто превышается. Подразделение получает направления из медицинских учреждений в южной части страны. С 2011 по 2015 год среднее количество госпитализаций составляло 1843 человека в год, а общий уровень смертности — 19 человек..2%. 24 Как правило, младенцев, поступающих в отделение интенсивной терапии новорожденных, сортируют по их весу, при этом младенцы с массой тела менее 2000 граммов содержатся в инкубаторах с минимальной одеждой. Мониторы, прикрепленные к инкубаторам, отображают температуру воздуха в инкубаторе и регулируются по мере необходимости. Клинически стабильные дети с массой тела 2000 г находятся в кроватках, одеты и завернуты. Матерям младенцев разрешается находиться в отделении интенсивной терапии новорожденных в установленное время кормления младенцев для сцеживания грудного молока или непосредственного кормления грудью своих младенцев. Пристроенная комната KMC вмещает до 6 пар мать-младенец.
Пристроенная комната KMC вмещает до 6 пар мать-младенец.
 Цифровые термометры имеют точность около 0,02 ° C при использовании для измерения из подмышечной области. 25 Всякий раз, когда звучал сигнал тревоги на BEMPU® TempWatch, указывающий на эпизод гипотермии, медсестры, проводившие исследование, измеряли температуру в подмышечной впадине у младенца, снова документировали практику теплового ухода и записывали все предпринятые клинические действия. У каждого младенца в течение 24-часового периода наблюдения было зафиксировано не менее семи температурных показателей. Данные собирались и хранились на планшетах Android с помощью программного обеспечения Open Data Kit (ODK), а затем загружались на защищенный сервер.
Цифровые термометры имеют точность около 0,02 ° C при использовании для измерения из подмышечной области. 25 Всякий раз, когда звучал сигнал тревоги на BEMPU® TempWatch, указывающий на эпизод гипотермии, медсестры, проводившие исследование, измеряли температуру в подмышечной впадине у младенца, снова документировали практику теплового ухода и записывали все предпринятые клинические действия. У каждого младенца в течение 24-часового периода наблюдения было зафиксировано не менее семи температурных показателей. Данные собирались и хранились на планшетах Android с помощью программного обеспечения Open Data Kit (ODK), а затем загружались на защищенный сервер. в момент рождения и в момент регистрации температуры. Одномерные и многомерные линейные регрессии были выполнены для изучения связи между температурой и различными независимыми переменными. В связи с многократными наблюдениями за каждым младенцем мы использовали обобщенные оценочные уравнения (GEE). Одномерные ассоциации с P <0,1 были включены в исходную многомерную модель. Для выбора окончательной многомерной модели использовалась пошаговая процедура с критерием включения 0,05. Уровень статистической значимости был установлен на уровне P <0,05. Изменения температуры, доверительные интервалы и p-значения сообщались для каждой независимой переменной. Все статистические анализы проводились с использованием STATA 17.0 (StataCorp LLC, Колледж-Стейшн, Техас, США).
в момент рождения и в момент регистрации температуры. Одномерные и многомерные линейные регрессии были выполнены для изучения связи между температурой и различными независимыми переменными. В связи с многократными наблюдениями за каждым младенцем мы использовали обобщенные оценочные уравнения (GEE). Одномерные ассоциации с P <0,1 были включены в исходную многомерную модель. Для выбора окончательной многомерной модели использовалась пошаговая процедура с критерием включения 0,05. Уровень статистической значимости был установлен на уровне P <0,05. Изменения температуры, доверительные интервалы и p-значения сообщались для каждой независимой переменной. Все статистические анализы проводились с использованием STATA 17.0 (StataCorp LLC, Колледж-Стейшн, Техас, США). Письменное информированное согласие на участие в исследовании было получено от матерей младенцев на местном языке или английском языке до включения в исследование.
Письменное информированное согласие на участие в исследовании было получено от матерей младенцев на местном языке или английском языке до включения в исследование.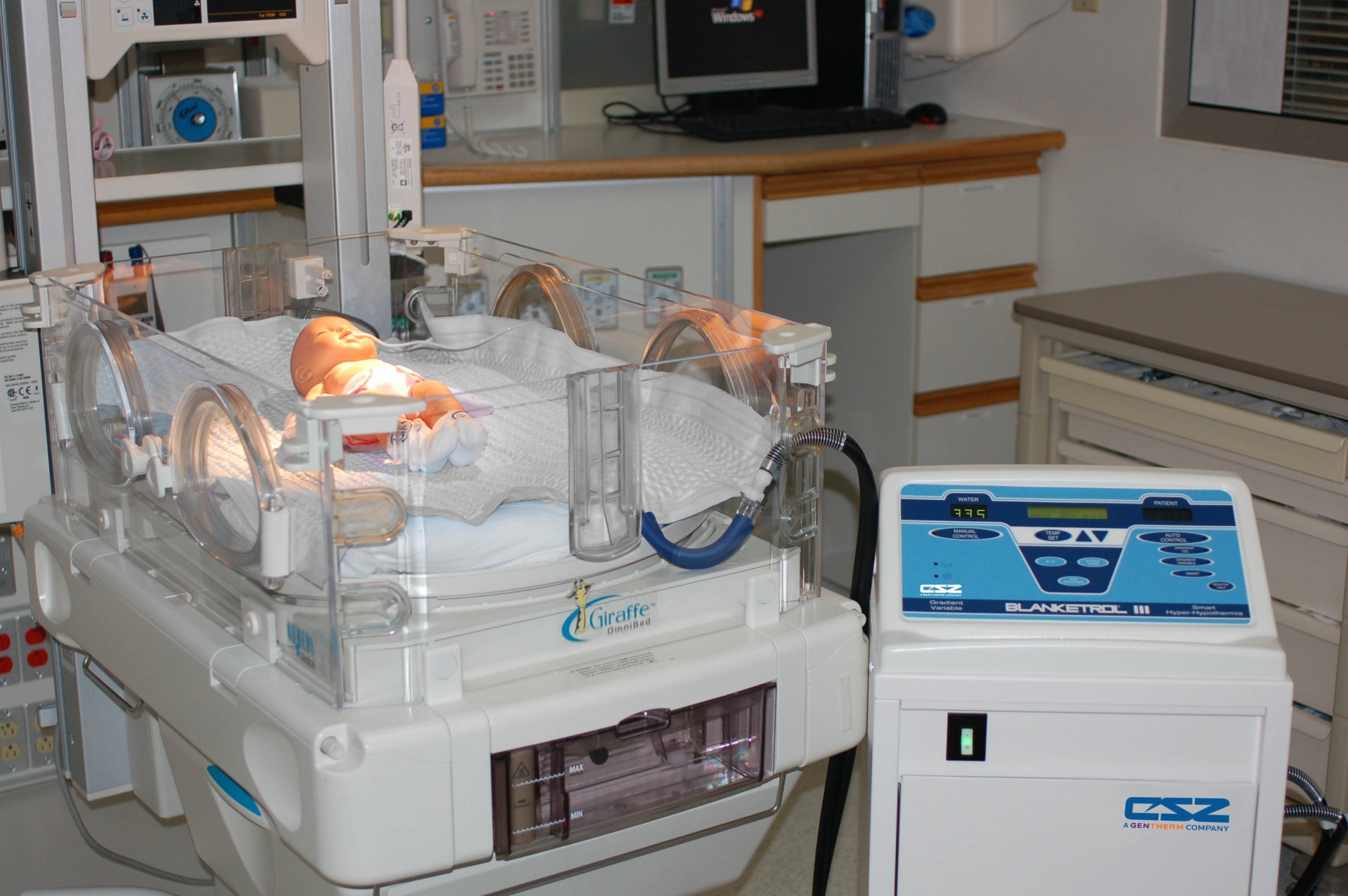 4,5%), были повторнородящими (52,6%) и повторнобеременными (65,3%).
4,5%), были повторнородящими (52,6%) и повторнобеременными (65,3%). 26,5% показателей температуры соответствовали критериям легкой гипотермии (36,0-36,4°С), а 18,0% — критериям умеренной гипотермии (32,0-35,9°С). Ни одно из показаний не соответствовало критериям тяжелой гипотермии (<32,0°C). В целом в этой популяции преобладала легкая и умеренная гипотермия: у 85,8% младенцев хотя бы одно значение температуры было ниже 36,5 °C в течение 24-часового периода наблюдения. Частота гипотермии была выше среди детей с ОНМТ (86,3%) и крайне недоношенных детей (100%).
26,5% показателей температуры соответствовали критериям легкой гипотермии (36,0-36,4°С), а 18,0% — критериям умеренной гипотермии (32,0-35,9°С). Ни одно из показаний не соответствовало критериям тяжелой гипотермии (<32,0°C). В целом в этой популяции преобладала легкая и умеренная гипотермия: у 85,8% младенцев хотя бы одно значение температуры было ниже 36,5 °C в течение 24-часового периода наблюдения. Частота гипотермии была выше среди детей с ОНМТ (86,3%) и крайне недоношенных детей (100%). Не было выявлено значимой связи между температурой и ношением шапки/кепки, носков или перчаток/рукавиц ( P >0,05). После поправки на значимые ковариаты модель многомерной линейной регрессии показала, что по сравнению с детьми, находящимися на исключительно грудном вскармливании, у детей на смешанном вскармливании (смеси и грудного молока) температура была ниже на 1,08°C, а у детей на искусственном вскармливании температура была выше на 0,38°C. . Младенцы с ОНМТ имели более низкую среднюю температуру по сравнению с детьми, не имевшими ОНМТ при рождении (β=-0,14°C), в то время как у крайне недоношенных детей температура была ниже, чем у доношенных детей (β=-0,70°C). Младенцы, имевшие контакт кожа к коже при рождении, были завернуты и помещены в инкубатор, у них была более высокая температура (0,20°C, 0,36°C и 0,67°C соответственно).
Не было выявлено значимой связи между температурой и ношением шапки/кепки, носков или перчаток/рукавиц ( P >0,05). После поправки на значимые ковариаты модель многомерной линейной регрессии показала, что по сравнению с детьми, находящимися на исключительно грудном вскармливании, у детей на смешанном вскармливании (смеси и грудного молока) температура была ниже на 1,08°C, а у детей на искусственном вскармливании температура была выше на 0,38°C. . Младенцы с ОНМТ имели более низкую среднюю температуру по сравнению с детьми, не имевшими ОНМТ при рождении (β=-0,14°C), в то время как у крайне недоношенных детей температура была ниже, чем у доношенных детей (β=-0,70°C). Младенцы, имевшие контакт кожа к коже при рождении, были завернуты и помещены в инкубатор, у них была более высокая температура (0,20°C, 0,36°C и 0,67°C соответственно). Некоторые из результатов исследования имеют значение для теплового ухода за маловесными младенцами в условиях ограниченных ресурсов. Во-первых, у 85,8% новорожденных хотя бы один раз в течение 24-часового периода наблюдения наблюдалась гипотермия. Этот показатель распространенности находится в пределах диапазона, ранее описанного в других условиях (от 8,1% до 9%).4,9%). 13 Однако коэффициент распространенности находится на верхней границе диапазона, скорее всего, потому, что LBW был одним из критериев включения в это исследование. Около половины (49,6%) младенцев в этом исследовании были ОНМТ, и большинство (92,9%) были недоношенными. У 86,3% новорожденных с ОНМТ был эпизод гипотермии в течение 24-часового периода наблюдения; среди глубоконедоношенных новорожденных у всех (100%) был эпизод гипотермии в течение 24-часового периода наблюдения. После поправки на другие ковариаты, включая использование инкубатора, разница в неонатальной температуре между ОНМТ и другими младенцами составила 0,11 °C, а разница между крайне недоношенными и доношенными детьми составила 0,73 °C.
Некоторые из результатов исследования имеют значение для теплового ухода за маловесными младенцами в условиях ограниченных ресурсов. Во-первых, у 85,8% новорожденных хотя бы один раз в течение 24-часового периода наблюдения наблюдалась гипотермия. Этот показатель распространенности находится в пределах диапазона, ранее описанного в других условиях (от 8,1% до 9%).4,9%). 13 Однако коэффициент распространенности находится на верхней границе диапазона, скорее всего, потому, что LBW был одним из критериев включения в это исследование. Около половины (49,6%) младенцев в этом исследовании были ОНМТ, и большинство (92,9%) были недоношенными. У 86,3% новорожденных с ОНМТ был эпизод гипотермии в течение 24-часового периода наблюдения; среди глубоконедоношенных новорожденных у всех (100%) был эпизод гипотермии в течение 24-часового периода наблюдения. После поправки на другие ковариаты, включая использование инкубатора, разница в неонатальной температуре между ОНМТ и другими младенцами составила 0,11 °C, а разница между крайне недоношенными и доношенными детьми составила 0,73 °C. Эти результаты согласуются с предыдущими исследованиями, которые показали более высокую частоту гипотермии среди детей с низкой массой тела и недоношенных детей. 12–17
Эти результаты согласуются с предыдущими исследованиями, которые показали более высокую частоту гипотермии среди детей с низкой массой тела и недоношенных детей. 12–17  27 Уход за матерями методом кенгуру (KMC), который включает ранний, непрерывный и длительный телесный контакт и грудное вскармливание, снижает гипотермию, частоту инфекций и риск смертности, одновременно способствуя увеличению веса и вскармливанию привязанность родитель-ребенок. 28–30 Несмотря на призывы к всеобщему охвату кенгуру для маловесных и недоношенных детей во всем континууме учреждение-сообщество, внедрение и расширение масштабов кенгуру было медленным из-за структурных, экономических, логистических и социальных барьеров. 31 Должен быть достигнут прогресс в расширении МК и вмешательств, дополняющих МК, таких как непрерывный мониторинг температуры.
27 Уход за матерями методом кенгуру (KMC), который включает ранний, непрерывный и длительный телесный контакт и грудное вскармливание, снижает гипотермию, частоту инфекций и риск смертности, одновременно способствуя увеличению веса и вскармливанию привязанность родитель-ребенок. 28–30 Несмотря на призывы к всеобщему охвату кенгуру для маловесных и недоношенных детей во всем континууме учреждение-сообщество, внедрение и расширение масштабов кенгуру было медленным из-за структурных, экономических, логистических и социальных барьеров. 31 Должен быть достигнут прогресс в расширении МК и вмешательств, дополняющих МК, таких как непрерывный мониторинг температуры.
