Рецепторы. Большая российская энциклопедия
БелкиБелки
Реце́пторы (лат. receptor – получатель, приёмник, от recipio – получать, принимать), группа белков, с помощью которых клетки и организм в целом воспринимают действие внешних и внутренних раздражителей. Рецепторы способны изменять свою пространственную конфигурацию в ответ на определённый тип раздражителя, активировать механизмы передачи (трансдукции) сигнала и запускать ответную реакцию клетки, оказывая влияние на её метаболизм и функциональное состояние (пролиферация, секреция и т. д.). В роли раздражителей могут выступать т. н. сигнальные молекулы, или лиганды (в том числе гормоны, медиаторы, факторы роста), и физические факторы (температура, кванты света, механическое воздействие). Различные клетки организма, в зависимости от их функции, имеют свой набор рецепторов. В соответствии с локализацией в клетке различают мембранные, цитоплазматические и ядерные рецепторы. Классификация рецепторов также проводится на основе их структуры, механизмов передачи сигнала и природы лигандов.
Большинство рецепторов представлено встроенными в плазматическую мембрану (интегральными) белками; при этом лиганд присоединяется к рецептору с внешней стороны клетки. Мембранные рецепторы функционируют в виде гомо- или гетеродимеров и олигомеров. Образование гетеродимерных комплексов модулирует лигандную специфичность и расширяет сигнальные возможности рецепторов. Сигналы от рецепторов передаются на внутриклеточные и мембранные эффекторные системы – протеинкиназы и другие ферменты, ионные каналы, транскрипционные факторы, сократительные белки и некоторые другие мишени. Передача сигнала может происходить разными способами: в результате взаимодействия части молекулы рецептора, ориентированной внутрь клетки, с мишенями в своём ближайшем микроокружении; с помощью вторичных посредников (мессенджеров), действующих на относительном удалении от рецептора; путём изменения электрического потенциала плазматической мембраны, благодаря чему сигнал распространяется по всей клеточной поверхности и может передаваться на большие расстояния. В большинстве случаев центральную роль в проведении внешних сигналов играет фосфорилирование соответствующих белков с участием протеинкиназ. Вторичными посредниками служат поступающие в цитоплазму клетки из внешней среды или из внутриклеточных органелл ионы кальция и образующиеся ферментативным путём циклическая аденозиндифосфатрибоза, циклические аденозин- и гуанозинмонофосфаты, никотинатадениндинуклеотидфосфат, продукты расщепления липидов плазматической мембраны – D-миоинозитол-1,4,5-трисфосфат, диацилглицерин, арахидоновая кислота.
В большинстве случаев центральную роль в проведении внешних сигналов играет фосфорилирование соответствующих белков с участием протеинкиназ. Вторичными посредниками служат поступающие в цитоплазму клетки из внешней среды или из внутриклеточных органелл ионы кальция и образующиеся ферментативным путём циклическая аденозиндифосфатрибоза, циклические аденозин- и гуанозинмонофосфаты, никотинатадениндинуклеотидфосфат, продукты расщепления липидов плазматической мембраны – D-миоинозитол-1,4,5-трисфосфат, диацилглицерин, арахидоновая кислота.
Самое большое семейство рецепторных белков образуют т. н. гептаспиральные рецепторы (содержат семь альфа-спиральных трансмембранных доменов, отсюда название). В связывании лигандов участвует N-концевой фрагмент (обычно гликозилирован) и другие части молекулы, расположенные с внешней стороны клеточной мембраны. С-концевой фрагмент и пептидные петли, обращённые внутрь клетки, сопряжены с ГТФ-связывающими G-белками – универсальными посредниками при передаче сигналов от этих рецепторов, адапторными белками и т. н. каркасными белками, которые формируют примембранный «скелет», на котором крепятся компоненты эффекторных систем, участвующих в передаче сигналов от рецептора. У человека гептаспиральные рецепторы кодируются примерно 800 генами (около 3 % от общего числа генов). Эти рецепторы осуществляют восприятие пахучих веществ, феромонов, молекул веществ горького и сладкого вкуса, большинства гормонов и нейромедиаторов, простагландинов, многих других биологически активных соединений внутренней среды организмов, квантов света (родопсины) и т. д.
н. каркасными белками, которые формируют примембранный «скелет», на котором крепятся компоненты эффекторных систем, участвующих в передаче сигналов от рецептора. У человека гептаспиральные рецепторы кодируются примерно 800 генами (около 3 % от общего числа генов). Эти рецепторы осуществляют восприятие пахучих веществ, феромонов, молекул веществ горького и сладкого вкуса, большинства гормонов и нейромедиаторов, простагландинов, многих других биологически активных соединений внутренней среды организмов, квантов света (родопсины) и т. д.
Большая группа рецепторов плазматических мембран обладает собственной протеинкиназной активностью. К их числу относятся рецепторные тирозинкиназы. Их лигандсвязывающий домен расположен на поверхности мембраны, а активный центр обращён внутрь клетки. При активации рецептора происходит димеризация фермента и автофосфорилирование тирозиновых остатков в его С-концевых фрагментах. К остаткам фосфотирозина присоединяются адапторные белки, через которые запускаются процесс фосфорилирования ряда других белков и активация факторов транскрипции соответствующих генов. Тирозинкиназы опосредуют действие инсулина и ряда белковых факторов роста. Рецепторные серин/треонинкиназы активируются морфогенетическими факторами роста, регулирующими эмбриональное развитие. Рецепторы цитокинов, не обладая собственной киназной активностью, взаимодействуют с тирозинкиназами, которые автофосфорилируются при активации рецептора, а далее фосфорилируют соответствующие факторы транскрипции, запуская деление клеток. Рецепторы Т- и В-лимфоцитов, распознающие антигены, присоединяют и активируют цитоплазматические тирозиновые киназы семейства Src family kinases. Рецепторы аминокислот и сахаров у бактерий, этилена у растений состоят из рецепторного фермента гистидинкиназы и т. н. регулятора ответа – цитоплазматического белка, передающего сигнал на эффекторную систему. Мембранные рецепторные гуанилатциклазы выявлены в сосудах, кишечнике, эпителии, фоторецепторных клетках. Их лигандом в сосудах является предсердный натрийуретический гормон, снижающий артериальное давление. Вторичным посредником в этом случае служит циклический гуанозинмонофосфат; он активирует протеинкиназу, которая фосфорилирует клеточные белки, меняя их активность.
Тирозинкиназы опосредуют действие инсулина и ряда белковых факторов роста. Рецепторные серин/треонинкиназы активируются морфогенетическими факторами роста, регулирующими эмбриональное развитие. Рецепторы цитокинов, не обладая собственной киназной активностью, взаимодействуют с тирозинкиназами, которые автофосфорилируются при активации рецептора, а далее фосфорилируют соответствующие факторы транскрипции, запуская деление клеток. Рецепторы Т- и В-лимфоцитов, распознающие антигены, присоединяют и активируют цитоплазматические тирозиновые киназы семейства Src family kinases. Рецепторы аминокислот и сахаров у бактерий, этилена у растений состоят из рецепторного фермента гистидинкиназы и т. н. регулятора ответа – цитоплазматического белка, передающего сигнал на эффекторную систему. Мембранные рецепторные гуанилатциклазы выявлены в сосудах, кишечнике, эпителии, фоторецепторных клетках. Их лигандом в сосудах является предсердный натрийуретический гормон, снижающий артериальное давление. Вторичным посредником в этом случае служит циклический гуанозинмонофосфат; он активирует протеинкиназу, которая фосфорилирует клеточные белки, меняя их активность. Адгезивные рецепторы, осуществляющие взаимодействие клеток между собой и с внеклеточным матриксом, – интегрины, кадгерины и селектины – передают системе цитоскелета информацию о миграции клетки или сцеплении с матриксом.
Адгезивные рецепторы, осуществляющие взаимодействие клеток между собой и с внеклеточным матриксом, – интегрины, кадгерины и селектины – передают системе цитоскелета информацию о миграции клетки или сцеплении с матриксом.
Ионотропные рецепторы (лигандуправляемые ионные каналы) усиливают или тормозят клеточную активность путём изменения электрического потенциала плазматической мембраны. Рецепторы этого типа участвуют в передаче нервных импульсов, сокращении мышечных клеток, секреции гормонов и медиаторов, в реакции фототропизма у растений. К возбуждающим относятся, например, отдельные типы рецепторов ацетилхолина, серотонина, АТФ, терморецепторы. Вызываемая ими деполяризация за счёт входа ионов натрия запускает потенциал действия и индуцирует открывание потенциалуправляемых кальциевых каналов. Активация рецепторов гамма-аминомасляной кислоты и глицина ведёт к открыванию каналов для ионов хлора, которые гиперполяризуют постсинаптическую мембрану. Ионотропные рецепторы представлены преимущественно в электровозбудимых клетках (нейронах, мышечных и секреторных клетках).
Рецепторы, локализованные в цитоплазме или ядерном матриксе, связывают жирорастворимые вещества, свободно проникающие через липидный бислой плазматической мембраны. У животных внутриклеточные рецепторы осуществляют рецепцию газов. Цитоплазматическая гуанилатциклаза служит рецептором оксидов азота и углерода, аденилатциклаза – рецептор аниона. Находящиеся в кровеносных сосудах рецепторы газов принимают участие в регуляции кровообращения. Ядерные рецепторы опосредуют, например, действие на клетки стероидных и тиреоидных гормонов, витамина D3, которые могут проходить через плазматические мембраны за счёт диффузии. После присоединения лиганда ядерные рецепторы приобретают способность связываться с определёнными последовательностями в ДНК, вызывая усиление или подавление транскрипции соответствующих генов.
Традиционно в физиологии рецепторами называются также концевые образования чувствительных нервных волокон, воспринимающие те или иные виды раздражителей (механорецепторы, в том числе фонорецепторы органов слуха; терморецепторы; фоторецепторы; хеморецепторы) и преобразующие их в нервные импульсы. Таким образом, рецепторы являются периферической частью анализаторов. Они могут быть представлены свободными окончаниями афферентных (чувствительных) нейронов, разветвляющимися в тканях (например, болевые рецепторы), или окружены специальными структурами (инкапсулированные рецепторы давления в коже, барорецепторы артериальных сосудов). Наиболее сложно организованы рецепторы слуховой системы млекопитающих (кортиев орган) и сетчатки глаза (колбочки, палочки). Анализ состояния внутренней среды организма осуществляют интероцепторы (интерорецепторы). Раздражения, действующие на организм из внешней среды, воспринимают высокоспециализированные чувствительные образования (экстероцепторы, экстерорецепторы). Работа любого рецептора сенсорных систем основана на изменении конформации рецепторных белков.
Таким образом, рецепторы являются периферической частью анализаторов. Они могут быть представлены свободными окончаниями афферентных (чувствительных) нейронов, разветвляющимися в тканях (например, болевые рецепторы), или окружены специальными структурами (инкапсулированные рецепторы давления в коже, барорецепторы артериальных сосудов). Наиболее сложно организованы рецепторы слуховой системы млекопитающих (кортиев орган) и сетчатки глаза (колбочки, палочки). Анализ состояния внутренней среды организма осуществляют интероцепторы (интерорецепторы). Раздражения, действующие на организм из внешней среды, воспринимают высокоспециализированные чувствительные образования (экстероцепторы, экстерорецепторы). Работа любого рецептора сенсорных систем основана на изменении конформации рецепторных белков.
Нарушения работы рецепторов являются причиной многих нейроэндокринных, сердечно-сосудистых, онкологических, неврологических заболеваний. Лиганды рецепторов и ингибиторы сопряжённых с рецептором сигнальных систем составляют большую часть (не менее 50 %) от применяемых лекарственных средств.
Виды рецепторов
Существуют несколько классификаций рецепторов:
По адекватному раздражителю
Хеморецепторы — воспринимают воздействие растворенных или летучих химических веществ.
Осморецепторы — воспринимают изменения осмотической концентрации жидкости (как правило, внутренней среды).
Механорецепторы — воспринимают механические стимулы (прикосновение, давление, растяжение, колебания воды или воздуха и т. п.)
Фоторецепторы — воспринимают видимый и ультрафиолетовый свет
Терморецепторы — воспринимают понижение (холодовые) или повышение (тепловые) температуры
Болевые рецепторы, стимуляция которых приводит к возникновению боли.
 Такого физического
стимула, как боль, не существует, поэтому
выделение их в отдельную группу по
природе раздражителя в некоторой
степени условно. В действительности,
они представляют собой высокопороговые
сенсоры различных (химических,
термических или механических)
повреждающих факторов. Однако уникальная
особенность ноцицепторов, которя не
позволяет отнести их, например, к
«высокопороговым терморецепторам»,
состоит в том, что многие из них
полимодальны: одно и то же нервное
окончание способно возбуждаться в
ответ на несколько различных повреждающих
стимулов
Такого физического
стимула, как боль, не существует, поэтому
выделение их в отдельную группу по
природе раздражителя в некоторой
степени условно. В действительности,
они представляют собой высокопороговые
сенсоры различных (химических,
термических или механических)
повреждающих факторов. Однако уникальная
особенность ноцицепторов, которя не
позволяет отнести их, например, к
«высокопороговым терморецепторам»,
состоит в том, что многие из них
полимодальны: одно и то же нервное
окончание способно возбуждаться в
ответ на несколько различных повреждающих
стимулов Электрорецепторы — воспринимают изменения электрического поля
Магнитные рецепторы — воспринимают изменения магнитного поля
У
человека имеются первые шесть типов
рецепторов. На хеморецепции основаны
вкус и обоняние, на механорецепции —
осязание, слух и равновесие, а также
ощущения положения тела в пространстве,
на фоторецепции — зрение.
Иногда предлагается выделять группу электромагнитных рецепторов, в которую включают фото-, электро- и магниторецепторы. Магниторецепторы точно не идентифицированы ни у одной группы животных, хотя предположительно ими служат некоторые клетки сетчатки птиц, а возможно, и ряд других клеток[2].
26глаз (лат. oculus) —
сенсорный орган (орган зрительной
системы)
человека и животных, обладающий
способностью воспринимать 
Глаз позвоночных животных представляет собой периферическую частьзрительного анализатора, в котором фоторецепторную функцию выполняютнейроны — фотосенсорные клетки («нейроциты») сетчатой оболочки. Внутреннее строение
1. Задняя камера 2. Зубчатый край 3. Ресничная (аккомодационная) мышца 4. Ресничный (цилиарный) поясок 5. Шлеммов канал 6. Зрачок 7. Передняя камера 8. Роговица 9. Радужная оболочка 10. Кора хрусталика 11. Ядро хрусталика 12. Цилиарный отросток 13. Конъюнктива
14. Нижняя косая мышца 15. Нижняя прямая мышца 16. Медиальная прямая мышца 17. Артерии и вены сетчатки 18. Слепое пятно 19. Твердая мозговая оболочка 20. Центральная артерия сетчатки 21. Центральная вена сетчатки 22. Зрительный нерв 23. Вортикозная вена 24. Влагалище глазного яблока 25. Жёлтое
пятно 26. Центральная
ямка 27. Склера 28. Сосудистая
оболочка глаза 29. Верхняя
прямая мышца 30. Сетчатка
Жёлтое
пятно 26. Центральная
ямка 27. Склера 28. Сосудистая
оболочка глаза 29. Верхняя
прямая мышца 30. СетчаткаГлазное яблоко состоит из оболочек, которые окружают внутреннее ядро глаза, представляющее его прозрачное содержимое — стекловидное тело, хрусталик, водянистая влага в передней и задней камерах.
Ядро глазного яблока окружают три оболочки: наружная, средняя и внутренняя.
Наружная — очень плотная фиброзная оболочка глазного яблока (
Средняя, или сосудистая, оболочка глазного яблока (tunica vasculosa bulbi), играет важную роль в обменных процессах, обеспечивая питание глаза и выведение продуктов обмена.
 Она богата кровеносными
сосудами и пигментом (богатые пигментом
клетки хориоидеи препятствуют
проникновению света через склеру,
устраняя светорассеяние). Она
образована радужкой, ресничным
телом и собственно
сосудистой оболочкой.
В центре радужки имеется круглое
отверстие — зрачок, через которое
лучи света проникают внутрь глазного
яблока и достигают сетчатки (величина
зрачка изменяется в результате
взаимодействия гладких мышечных
волокон — сфинктера и
дилататора, заключённых в радужке и
иннервируемых парасимпатическим и симпатическимнервами).
Радужка содержит различное количество
пигмента, от которого зависит её
окраска — «цвет
глаз».
Она богата кровеносными
сосудами и пигментом (богатые пигментом
клетки хориоидеи препятствуют
проникновению света через склеру,
устраняя светорассеяние). Она
образована радужкой, ресничным
телом и собственно
сосудистой оболочкой.
В центре радужки имеется круглое
отверстие — зрачок, через которое
лучи света проникают внутрь глазного
яблока и достигают сетчатки (величина
зрачка изменяется в результате
взаимодействия гладких мышечных
волокон — сфинктера и
дилататора, заключённых в радужке и
иннервируемых парасимпатическим и симпатическимнервами).
Радужка содержит различное количество
пигмента, от которого зависит её
окраска — «цвет
глаз».Внутренняя, или сетчатая, оболочка глазного яблока (tunica interna bulbi), — сетчатка — рецепторная часть зрительного анализатора, здесь происходит непосредственное восприятие света, биохимические превращения зрительных пигментов, изменение электрических свойств нейронов и передача информации вцентральную нервную систему.

С функциональной точки зрения оболочки глаза и её производные подразделяют на три аппарата: рефракционный (светопреломляющий) и аккомодационный (приспособительный), формирующие оптическую систему глаза, и сенсорный (рецепторный) аппарат.
Типы рецепторов — Неврология — Книжная полка NCBI
Независимо от природы инициирующего сигнала клеточные ответы определяются наличием рецепторов, которые специфически связываются с сигнальными молекулами. Связывание сигнальных молекул вызывает конформационные изменения в рецепторе, которые затем запускают последующий сигнальный каскад. Учитывая, что химические сигналы могут действовать либо на плазматической мембране, либо внутри цитоплазмы (или ядра) клетки-мишени, неудивительно, что рецепторы обнаруживаются с обеих сторон плазматической мембраны.
Рецепторы для непроникающих сигнальных молекул представляют собой трансмембранные белки, которые включают компоненты как снаружи, так и внутри клеточной поверхности. Внеклеточный домен таких рецепторов включает сайт связывания сигнала, в то время как внутриклеточный домен активирует внутриклеточные сигнальные каскады после связывания сигнала. Было идентифицировано большое количество этих рецепторов, которые сгруппированы в три семейства, определяемые механизмом, используемым для преобразования связывания сигнала в клеточный ответ (-).
Внеклеточный домен таких рецепторов включает сайт связывания сигнала, в то время как внутриклеточный домен активирует внутриклеточные сигнальные каскады после связывания сигнала. Было идентифицировано большое количество этих рецепторов, которые сгруппированы в три семейства, определяемые механизмом, используемым для преобразования связывания сигнала в клеточный ответ (-).
Рисунок 8.4
Категории клеточных рецепторов. Мембранно-непроницаемые сигнальные молекулы могут связываться и активировать рецепторы, связанные с каналом (А), рецепторы, связанные с ферментами (В), или рецепторы, связанные с G-белком (С). Проникающие в мембрану сигнальные молекулы активируют внутриклеточные (подробнее…)
Связанные с каналами рецепторы (также называемые лиганд-управляемыми ионными каналами) выполняют функции рецептора и трансдукции как часть одной и той же белковой молекулы. Взаимодействие химического сигнала с местом связывания рецептора вызывает открытие или закрытие поры ионного канала в другой части той же молекулы. Возникающий ионный поток изменяет мембранный потенциал клетки-мишени и в некоторых случаях также может приводить к проникновению Ca 2+ ионов, которые служат вторичным мессенджером сигнала внутри клетки. Хорошими примерами таких рецепторов являются рецепторы нейротрансмиттеров, описанные в главе 7.
Возникающий ионный поток изменяет мембранный потенциал клетки-мишени и в некоторых случаях также может приводить к проникновению Ca 2+ ионов, которые служат вторичным мессенджером сигнала внутри клетки. Хорошими примерами таких рецепторов являются рецепторы нейротрансмиттеров, описанные в главе 7.
Связанные с ферментом рецепторы также имеют внеклеточный сайт связывания химических сигналов. Внутриклеточный домен таких рецепторов представляет собой фермент, каталитическая активность которого регулируется связыванием внеклеточного сигнала. Подавляющее большинство этих рецепторов представляют собой протеинкиназ, часто тирозинкиназ , , которые фосфорилируют внутриклеточные белки-мишени, тем самым изменяя физиологическую функцию клеток-мишеней. Заслуживающие внимания члены этой группы рецепторов включают семейство Trk рецепторов нейротрофинов (см. главу 23) и другие рецепторы факторов роста.
Связанные с G-белком рецепторы регулируют внутриклеточные реакции посредством косвенного механизма, включающего промежуточную трансдуцирующую молекулу, называемую GTP-связывающими белками (или G-белками). Поскольку все эти рецепторы обладают общей структурной особенностью семикратного пересечения плазматической мембраны, их также называют 7-трансмембранными рецепторами (или метаботропными рецепторами; см. главу 7). Были идентифицированы сотни различных рецепторов, связанных с G-белком. Хорошо известные примеры включают β-адренергический рецептор, мускарининовый тип ацетилхолинового рецептора, метаботропные глутаматные рецепторы, рецепторы одорантов в обонятельной системе и многие типы рецепторов пептидных гормонов. Родопсин, светочувствительный 7-трансмембранный белок в фоторецепторах сетчатки, представляет собой другую форму рецептора, связанного с G-белком (см. главу 11).
Поскольку все эти рецепторы обладают общей структурной особенностью семикратного пересечения плазматической мембраны, их также называют 7-трансмембранными рецепторами (или метаботропными рецепторами; см. главу 7). Были идентифицированы сотни различных рецепторов, связанных с G-белком. Хорошо известные примеры включают β-адренергический рецептор, мускарининовый тип ацетилхолинового рецептора, метаботропные глутаматные рецепторы, рецепторы одорантов в обонятельной системе и многие типы рецепторов пептидных гормонов. Родопсин, светочувствительный 7-трансмембранный белок в фоторецепторах сетчатки, представляет собой другую форму рецептора, связанного с G-белком (см. главу 11).
Внутриклеточные рецепторы активируются проникающими в клетку или липофильными сигнальными молекулами (). Многие из этих рецепторов приводят к активации сигнальных каскадов, производящих новую мРНК и белок внутри клетки-мишени. Часто такие рецепторы содержат рецепторный белок, связанный с ингибирующим белковым комплексом. Когда сигнальная молекула связывается с рецептором, ингибирующий комплекс диссоциирует, обнажая ДНК-связывающий домен на рецепторе. Затем эта активированная форма рецептора может перемещаться в ядро и напрямую взаимодействовать с ядерной ДНК, что приводит к изменению транскрипции. Одни внутриклеточные рецепторы расположены преимущественно в цитоплазме, другие — в ядре. В любом случае, как только эти рецепторы активированы, они могут влиять на экспрессию генов, изменяя транскрипцию ДНК.
Когда сигнальная молекула связывается с рецептором, ингибирующий комплекс диссоциирует, обнажая ДНК-связывающий домен на рецепторе. Затем эта активированная форма рецептора может перемещаться в ядро и напрямую взаимодействовать с ядерной ДНК, что приводит к изменению транскрипции. Одни внутриклеточные рецепторы расположены преимущественно в цитоплазме, другие — в ядре. В любом случае, как только эти рецепторы активированы, они могут влиять на экспрессию генов, изменяя транскрипцию ДНК.
Физиология, клеточный рецептор — StatPearls
Введение
Клеточные рецепторы представляют собой белки внутри клетки или на ее поверхности, принимающие сигнал. В нормальной физиологии это химический сигнал, при котором белок-лиганд связывается с белковым рецептором. Лиганд представляет собой химический мессенджер, высвобождаемый одной клеткой для подачи сигнала либо самой себе, либо другой клетке. Связывание приводит к клеточному эффекту, который проявляется в виде любого количества изменений в этой клетке, включая изменение транскрипции или трансляции генов или изменение морфологии клеток. Как правило, один лиганд будет иметь один рецептор, с которым он может связываться и вызывать клеточный ответ. Существует несколько различных типов клеточной передачи сигналов, все из которых зависят от разных лигандов и клеточных рецепторов.
Как правило, один лиганд будет иметь один рецептор, с которым он может связываться и вызывать клеточный ответ. Существует несколько различных типов клеточной передачи сигналов, все из которых зависят от разных лигандов и клеточных рецепторов.
Основные категории клеточной передачи сигналов включают аутокринный, сигнал через щелевой контакт, паракринный и эндокринный. Аутокринная передача сигналов — это когда клетка высвобождает сигнал, который затем связывается с одним из ее рецепторов, чтобы изменить его функционирование. Передача сигналов через щелевые контакты происходит, когда небольшие сигнальные молекулы перемещаются непосредственно через соседние прикрепленные клетки. Паракринная передача сигналов — это связь между соседними клетками. Эндокринная сигнализация — это когда клеточные сигналы поступают к клеточным рецепторам-мишеням в другой части тела через кровоток. Каждый тип передачи сигналов требует лиганда и рецептора. Клеточные рецепторы можно разделить на внутренние рецепторы, рецепторы клеточной поверхности, рецепторы ионных каналов, рецепторы, связанные с G-белком (GPCR), и рецепторы, связанные с ферментами.
Сотовый уровень
Типы лигандов
Лиганды — это сигнальные молекулы, используемые организмом для связи различных клеток с другими клетками. Надпочечники могут выделять гормон, такой как кортизол, который взаимодействует с большим количеством различных клеток различных органов, оказывая значительное влияние, или один ингибирующий нейрон может выделять нейротрансмиттер, такой как ГАМК, для оказания непосредственного воздействия на другую клетку. Эффект лиганда зависит как от самого лиганда, так и от рецептора, на который он нацелен. Например, небольшие и гидрофобные лиганды, такие как стероиды, такие как кортизол, часто нацелены на внутренние рецепторы, поскольку они способны проходить через плазматическую мембрану без посторонней помощи.
Внутренние рецепторы
Эти рецепторы также известны как внутриклеточные или цитоплазматические. Они обнаруживаются в цитоплазме клетки и часто становятся мишенью для гидрофобных лигандов, которые могут пересекать липидный бислой мембраны плазматических клеток животных. Часто эти рецепторы модифицируют синтез мРНК и, таким образом, синтез белка внутри клетки. Они достигают этого за счет того, что комплекс лиганд-рецептор может перемещаться в ядро и связывать ДНК в регуляторном участке гена, чего рецептор и лиганд сами по себе не могут сделать. Тестостерон, эстроген, кортизол и альдостерон являются примерами стероидных гормонов, которые являются гидрофобными и проникают через плазматическую мембрану к внутренним рецепторам. Внутренние рецепторы часто работают без вторичных мессенджеров для передачи сигнала до синтеза мРНК, и это влияет на синтез белка, процесс, уникальный для внутренних рецепторов, поскольку другие типы работают через клеточный каскад, который приводит к изменению синтеза белка.
Рецепторы клеточной поверхности
Эти рецепторы также известны как трансмембранные рецепторы. Это белки, которые находятся на поверхности клеток и охватывают плазматическую мембрану. Они связываются с лигандами, которые сами по себе не могут пройти через плазматическую мембрану. Это часто гидрофильные лиганды или слишком большие, чтобы пройти через них. Эти рецепторы не связываются с ДНК для изменения транскрипции и трансляции генов, а выполняют трансдукцию сигнала; внеклеточный сигнал запускает внутриклеточный сигнал, который обычно направляется в ядро, чтобы повлиять на функционирование клетки. Часто рецептор клеточной поверхности будет специфичным для этого типа клеток, так что лиганд может влиять только на функционирование своих клеток-мишеней. Компоненты рецептора клеточной поверхности могут расщепляться на внешний лиганд-связывающий домен, гидрофобную область, которая охватывает мембрану, и внутриклеточный домен, который отвечает за запуск каскада вторичных мессенджеров.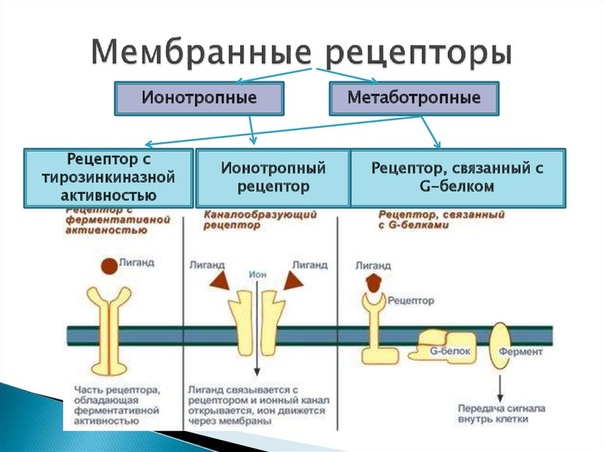 Рецепторы клеточной поверхности бывают трех основных типов: рецепторы ионных каналов, GPCR и рецепторы, связанные с ферментами.
Рецепторы клеточной поверхности бывают трех основных типов: рецепторы ионных каналов, GPCR и рецепторы, связанные с ферментами.
Рецепторы ионных каналов
Когда лиганд связывается с рецептором ионного канала, открывается канал через плазматическую мембрану, через который проходят определенные ионы. Этот процесс требует специализированной трансмембранной области рецептора. Связывание лиганда создает изменение формы рецептора, что позволяет проходить определенным ионам, обычно натрию, магнию, кальцию или водороду. Химически закрытые ионные каналы находятся на дендритах и телах нейронов.
GPCR
GPCR представляют собой подтип рецепторов клеточной поверхности, которые действуют через G-белок, запуская каскад вторичных мессенджеров, модулируя клеточную функцию. Рецептор имеет сайт связывания лиганда снаружи плазматической мембраны и имеет трансмембранную часть, которая может связываться с G-белком во внутриклеточном пространстве. G-белок представляет собой гетеротримерный белок с тремя субъединицами: альфа, бета и гамма. Бета- и гамма-субъединицы прикреплены к мембране липидным якорем. Когда лиганд не связан с рецептором, альфа-субъединица и GDP связаны с трансмембранным рецептором, а также с бета- и гамма-субъединицами. Когда лиганд связывается с рецептором, конформационное изменение активирует G-белок, и молекула GTP заменяет молекулу GDP на альфа-субъединице. G-белок диссоциирует с бета- и гамма-субъединицами, оставшимися прикрепленными своим якорем, а активированная альфа-субъединица, теперь связанная с молекулой GTP, освобождается от внутриклеточной стенки плазматической мембраны. И бета-гамма-димер, и альфа-ГТФ могут способствовать распространению сигнального каскада. Некоторые распространенные ферменты и вторичные мессенджеры, активируемые этим каскадом, включают аденилатциклазу, циклический АМФ, диацилглицерин, инозитол-1,4,5-трифосфат и фосфолипазу С. GPCR могут быть как активирующими, так и ингибирующими. GPCR участвуют во многих функциях многоклеточного организма, включая, помимо прочего, рост, передачу эндокринных сигналов, чувствительность и свертывание крови.
Бета- и гамма-субъединицы прикреплены к мембране липидным якорем. Когда лиганд не связан с рецептором, альфа-субъединица и GDP связаны с трансмембранным рецептором, а также с бета- и гамма-субъединицами. Когда лиганд связывается с рецептором, конформационное изменение активирует G-белок, и молекула GTP заменяет молекулу GDP на альфа-субъединице. G-белок диссоциирует с бета- и гамма-субъединицами, оставшимися прикрепленными своим якорем, а активированная альфа-субъединица, теперь связанная с молекулой GTP, освобождается от внутриклеточной стенки плазматической мембраны. И бета-гамма-димер, и альфа-ГТФ могут способствовать распространению сигнального каскада. Некоторые распространенные ферменты и вторичные мессенджеры, активируемые этим каскадом, включают аденилатциклазу, циклический АМФ, диацилглицерин, инозитол-1,4,5-трифосфат и фосфолипазу С. GPCR могут быть как активирующими, так и ингибирующими. GPCR участвуют во многих функциях многоклеточного организма, включая, помимо прочего, рост, передачу эндокринных сигналов, чувствительность и свертывание крови.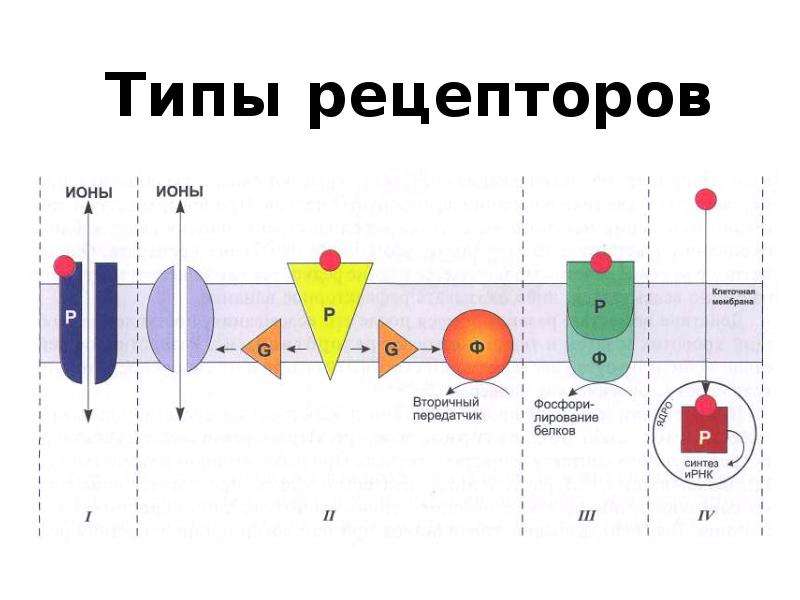
Рецепторы, связанные с ферментами
Этот подтип трансмембранных рецепторов имеет каталитический сайт в цитоплазматическом домене. Часто, когда лиганд связывается с этими рецепторами, они димеризуются, что активирует каталитический сайт рецептора и приводит к ферментативной активности. Существует несколько типов рецепторов, связанных с ферментами; наиболее распространенным типом является рецепторная тирозинкиназа. Другие примеры включают рецепторную серин/треонинкиназу, рецепторную гуанилилциклазу и рецепторную тирозинфосфатазу. Рецепторные тирозиновые и рецепторные сериновые и треонинкиназы димеризуются, что вызывает аутофосфорилирование в тирозиновых, сериновых или треониновых участках соответственно. Это фосфорилирование активирует ферментативную активность рецептора. Многие сигналы роста, такие как эпидермальный фактор роста и тромбоцитарный фактор роста, работают с рецепторной тирозинкиназой.
Развитие
Процесс превращения отдельной клетки в сложный многоклеточный организм требует тщательного регулирования клеточной активности, включая дифференцировку, миграцию и пролиферацию. Все эти действия должны происходить в нужное время и в нужном месте. Этот высокий уровень координации требует обширной, скоординированной и быстрой сотовой связи. Существует несколько ключевых сигнальных путей, идентифицированных в исследованиях на людях и животных, необходимых для правильного развития, включая FGF, hedgehog, Wnt, TGF бета и notch. Один лиганд может связываться с несколькими разными рецепторами на разных клетках, вызывая различные последующие эффекты. Например, в пути Wnt лиганд может связываться с множественными рецепторными комплексами и запускать несколько нижестоящих сигнальных каскадов, что приводит к разнообразным клеточным ответам. Это один из примеров того, как клеточные рецепторы могут превращать один и тот же сигнал в несколько разных эффектов. Благодаря сложному взаимодействию лиганда и рецептора отдельная клетка развивается в сложный многоклеточный организм в нужное время по отношению к другим клеточным процессам.
Все эти действия должны происходить в нужное время и в нужном месте. Этот высокий уровень координации требует обширной, скоординированной и быстрой сотовой связи. Существует несколько ключевых сигнальных путей, идентифицированных в исследованиях на людях и животных, необходимых для правильного развития, включая FGF, hedgehog, Wnt, TGF бета и notch. Один лиганд может связываться с несколькими разными рецепторами на разных клетках, вызывая различные последующие эффекты. Например, в пути Wnt лиганд может связываться с множественными рецепторными комплексами и запускать несколько нижестоящих сигнальных каскадов, что приводит к разнообразным клеточным ответам. Это один из примеров того, как клеточные рецепторы могут превращать один и тот же сигнал в несколько разных эффектов. Благодаря сложному взаимодействию лиганда и рецептора отдельная клетка развивается в сложный многоклеточный организм в нужное время по отношению к другим клеточным процессам.
Вовлеченные системы органов
Каждая система органов в организме нуждается в клеточной связи и, следовательно, в клеточных рецепторах, включая межклеточные взаимодействия, такие как макрофаги, активирующие плазматические клетки иммунной системы, и высвобождение ацетилхолина в нервно-мышечном соединении нервной системы. Эта активность также включает взаимодействия в масштабах всего тела, такие как высвобождение АКТГ гипоталамусом, вызывающее высвобождение надпочечниками кортизола, который затем влияет почти на все системы органов. В конечном счете, способность любого организма становиться многоклеточным зависит от способности использовать клеточные рецепторы для коммуникации.
Эта активность также включает взаимодействия в масштабах всего тела, такие как высвобождение АКТГ гипоталамусом, вызывающее высвобождение надпочечниками кортизола, который затем влияет почти на все системы органов. В конечном счете, способность любого организма становиться многоклеточным зависит от способности использовать клеточные рецепторы для коммуникации.
Патофизиология
Существует два основных пути участия клеточных рецепторов в патофизиологии человека: микроорганизмы, связывающие клеточные рецепторы человека для выживания или вызывающие заболевание, и дисфункция клеточных рецепторов, приводящая к нарушению нормальных физиологических процессов, что приводит к заболеванию.
Вирусы должны связываться с рецепторами на клеточной поверхности клетки-хозяина, чтобы получить к ним доступ. Таким образом, вирусы захватили рецепторы клеток человека для своего использования. Например, поверхностный белок ВИЧ GP-120 должен связываться с рецептором CCR5, чтобы попасть в макрофаги человека. [2] Люди, гомозиготные по делеции рецептора CCR5, устойчивы к заражению вирусами ВИЧ, которым для заражения нужен этот рецептор. Кроме того, ведутся исследования, нацеленные на рецептор CCR5 как на способ блокирования ВИЧ-инфекции.[3]
[2] Люди, гомозиготные по делеции рецептора CCR5, устойчивы к заражению вирусами ВИЧ, которым для заражения нужен этот рецептор. Кроме того, ведутся исследования, нацеленные на рецептор CCR5 как на способ блокирования ВИЧ-инфекции.[3]
Вирус гриппа поражает эпителиальные клетки верхних и нижних дыхательных путей. Вирусные клетки имеют на своей поверхности белок, называемый гемагглютинином, который связывается с сиаловой кислотой. Сиаловая кислота представляет собой сахар, находящийся на поверхности клеток. Благодаря тому, что вирус связывает сиаловую кислоту, сахар действует как клеточный рецептор гриппа, что необходимо вирусу для заражения клетки.
Этот список не является исчерпывающим, а просто суммирует некоторые состояния, вызванные дефектом клеточного рецептора:
Псевдогипопаратиреоз относится к гетерогенной группе заболеваний, определяемых нечувствительностью органов-мишеней к паратгормону (ПТГ). Это состояние связано с любой дисфункцией сигнального пути ПТГ. Одной из конкретных причин псевдогипопаратиреоза является миссенс-мутация в последовательности гена ПТГ, которая приводит к снижению связывания ПТГ с рецептором. Когда сигнал не может связываться со своим рецептором, ПТГ не может воздействовать на различные органы-мишени, особенно на почки и кости, чтобы регулировать уровни кальция и фосфора в организме.
Одной из конкретных причин псевдогипопаратиреоза является миссенс-мутация в последовательности гена ПТГ, которая приводит к снижению связывания ПТГ с рецептором. Когда сигнал не может связываться со своим рецептором, ПТГ не может воздействовать на различные органы-мишени, особенно на почки и кости, чтобы регулировать уровни кальция и фосфора в организме.
Синдром МакКьюна-Олбрайта представляет собой редкое заболевание, проявляющееся триадой: периферическим преждевременным половым созреванием, пятнами цвета «кофе с молоком» и фиброзной дисплазией кости. У детей с синдромом МакКьюна-Олбрайта имеется соматическая мутация альфа-субъединицы стимулирующего G-белка, которая активирует аденилатциклазу. Мутация в этом белке приводит к постоянной стимуляции его сигнального каскада независимо от связывания с рецептором.[6]
Критерием клинического диагноза семейной гиперхолестеринемии Американской кардиологической ассоциации является уровень ЛПНП выше 190 мг/дл и либо родственник первой степени родства с уровнем ЛПНП выше 190 мг/дл, либо известная преждевременная ишемическая болезнь сердца. Примерно у 80% пациентов с подтвержденной СГ имеется мутация в одном из трех генов, связанных с катаболизмом ЛПНП, опосредованным рецептором ЛПНП. Из 80% известных мутаций от 85 до 90% мутаций связаны с рецептором ЛПНП. Наиболее распространенной этиологией СГ является мутация апо В/Е клеточного рецептора ЛПНП. В норме частицы ЛПНП связываются с рецептором ЛПНП на поверхности клеток печени. Когда эти частицы ЛПНП связаны, они интернализуются и катаболизируются, удаляя их из крови. Исследователи выявили более 1600 различных мутаций в рецепторе ЛПНП, что привело к четырем классам аллелей на основе результирующего фенотипа мутантного рецептора.[6] Класс I — белок не синтезируется. Класс II — это когда внутриклеточный транспорт рецепторов от ER к аппарату Гольджи нарушен. Класс III — это когда рецептор проникает на поверхность клетки, но не может связываться с ЛПНП, класс IV — это когда ЛПНП связывается нормально, но рецепторы не группируются в покрытых ямках, и частицы ЛПНП не становятся адекватно интернализованными.
Примерно у 80% пациентов с подтвержденной СГ имеется мутация в одном из трех генов, связанных с катаболизмом ЛПНП, опосредованным рецептором ЛПНП. Из 80% известных мутаций от 85 до 90% мутаций связаны с рецептором ЛПНП. Наиболее распространенной этиологией СГ является мутация апо В/Е клеточного рецептора ЛПНП. В норме частицы ЛПНП связываются с рецептором ЛПНП на поверхности клеток печени. Когда эти частицы ЛПНП связаны, они интернализуются и катаболизируются, удаляя их из крови. Исследователи выявили более 1600 различных мутаций в рецепторе ЛПНП, что привело к четырем классам аллелей на основе результирующего фенотипа мутантного рецептора.[6] Класс I — белок не синтезируется. Класс II — это когда внутриклеточный транспорт рецепторов от ER к аппарату Гольджи нарушен. Класс III — это когда рецептор проникает на поверхность клетки, но не может связываться с ЛПНП, класс IV — это когда ЛПНП связывается нормально, но рецепторы не группируются в покрытых ямках, и частицы ЛПНП не становятся адекватно интернализованными. Независимо от класса, если у кого-то нет должным образом функционирующего рецептора ЛПНП, он не может должным образом очистить кровь от ЛПНП. Результатом является ранний атеросклероз и сопутствующая патология.
Независимо от класса, если у кого-то нет должным образом функционирующего рецептора ЛПНП, он не может должным образом очистить кровь от ЛПНП. Результатом является ранний атеросклероз и сопутствующая патология.
Миастения гравис — это заболевание, которое часто проявляется на втором и третьем десятилетиях жизни с преобладанием женского пола или на шестом-восьмом десятилетии жизни с преобладанием мужчин. Наиболее частым признаком миастении является колеблющаяся мышечная слабость. Заболевание возникает из-за аутоантител против ацетилхолинового рецептора.[7] Эти антитела действуют на нервно-мышечное соединение и блокируют связывание ацетилхолина с его клеточным рецептором. Кроме того, связывание аутоантител вызывает перекрестное связывание и интернализацию рецепторов. Когда ацетилхолин не может связываться с большинством своих клеточных рецепторов в нервно-мышечном синапсе, мышца не может сокращаться так, как должна.
Синдром нечувствительности к андрогенам — это состояние, влияющее на половое развитие как до рождения, так и в период полового созревания. Когда плод генетически мужского пола, с X- и Y-хромосомой, плод должен развиваться как мужчина и претерпевать мужские изменения во время полового созревания. Во время развития у плода разовьются внутренние мужские органы из-за гена SRY на Y-хромосоме, но без передачи сигналов андрогена внешний фенотип пациента будет женским. Это состояние у пациентов с синдромом нечувствительности к андрогенам, поскольку у них есть мутация потери функции в гене, кодирующем рецептор андрогена.[8] Без этого рецептора уровень андрогенов будет нормальным или высоким, но не повлияет на развитие.
Когда плод генетически мужского пола, с X- и Y-хромосомой, плод должен развиваться как мужчина и претерпевать мужские изменения во время полового созревания. Во время развития у плода разовьются внутренние мужские органы из-за гена SRY на Y-хромосоме, но без передачи сигналов андрогена внешний фенотип пациента будет женским. Это состояние у пациентов с синдромом нечувствительности к андрогенам, поскольку у них есть мутация потери функции в гене, кодирующем рецептор андрогена.[8] Без этого рецептора уровень андрогенов будет нормальным или высоким, но не повлияет на развитие.
Ахондроплазия является аутосомно-доминантным заболеванием и наиболее распространенной костной дисплазией у людей. Пациенты с ахондроплазией имеют мутацию усиления функции в гене FGFR3, что приводит к постоянно активированному рецептору FGFR3.[9] Этот рецептор не нуждается в связывании своего лиганда, чтобы активироваться. В результате ингибируется пролиферация хондроцитов и нарушается формирование эндохондральной кости, что приводит к ограничению роста и укорочению кости, среди других скелетных аномалий. [10]
[10]
Клиническое значение
Бактериальный сепсис и вызванный им септический шок являются результатом перепроизводства воспалительных сигналов. Это перепроизводство воспалительных сигналов является результатом взаимодействия иммунной системы с компонентами бактериальной стенки. В этот процесс особенно вовлечены липополисахариды, пептидогликаны и другие вещества. Когда эти компоненты бактериальной стенки связываются с рецепторами комплемента и Fc на поверхности мононуклеарных клеток, макрофаги становятся метаболически активными и продуцируют бактерицидные агенты, а также секретируют провоспалительные цитокины, такие как TNF-альфа.
Пациенты с псевдогипопаратиреозом будут иметь гипокальциемию, гиперфосфатемию и повышенный уровень ПТГ, так как паращитовидная железа пытается вырабатывать больше гормонов для устранения дисбаланса. У пациентов с псевдогипопаратиреозом нарушения электролитного баланса могут проявляться тетанией, судорогами, сердечными аритмиями, отеком диска зрительного нерва и психическими симптомами.
У пациентов с синдромом МакКьюна-Олбрайта больше всего страдают эндокринные функции, что приводит к преждевременному половому созреванию, тиреотоксикозу, гигантизму, акромегалии, синдрому Кушинга или гипофосфатемическому рахиту, в зависимости от того, где произошла мутация. Мутации также могут возникать в печени или сердце, приводя к холестазу и гепатиту или сердечным аритмиям.
У пациентов с миастенией часто первым заметным симптомом является диплопия или птоз из-за слабости глазных мышц или мышц век. При тяжелых формах заболевания также могут поражаться бульбарные мышцы, конечности и дыхательные мышцы. Аналогичное состояние Ламберта-Итона, когда аутоантитела нацелены на пресинаптические кальциевые каналы, что приводит к неспособности нейрона высвобождать ацетилхолин в НМС [7]. Оба этих состояния обусловлены неспособностью клеток прикреплять ацетилхолин к их клеточным рецепторам.
Синдром нечувствительности к андрогенам существует в диапазоне от частичного до полного, в зависимости от уровня функционирования рецептора андрогена. При полной нечувствительности к андрогенам у здорового ребенка женского пола обнаруживаются паховые образования, содержащие яички. Пациентов также часто выявляют в период полового созревания, когда у них отсутствуют менструации. При тестировании у пациентов будут аномально высокие уровни тестостерона, ЛГ и ФСГ из-за отказа петли отрицательной обратной связи в гипоталамо-гипофизарно-гонадной оси.
При полной нечувствительности к андрогенам у здорового ребенка женского пола обнаруживаются паховые образования, содержащие яички. Пациентов также часто выявляют в период полового созревания, когда у них отсутствуют менструации. При тестировании у пациентов будут аномально высокие уровни тестостерона, ЛГ и ФСГ из-за отказа петли отрицательной обратной связи в гипоталамо-гипофизарно-гонадной оси.
Мутация при ахондроплазии, вызывающая конститутивно активный рецептор FGF3, приводит к ингибированию пролиферации хондроцитов и образованию эндохондральной кости, что приводит к ограничению роста и укорочению костей, среди других скелетных аномалий.[10]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Jones B. Терапевтический потенциал агонизма, обусловленного рецептором GLP-1. Бр Дж. Фармакол. 2022 фев; 179(4):492-510.
 [Бесплатная статья PMC: PMC8820210] [PubMed: 33880754]
[Бесплатная статья PMC: PMC8820210] [PubMed: 33880754]- 2.
Dragic T, Litwin V, Allaway GP, Martin SR, Huang Y, Nagashima KA, Cayanan C, Maddon PJ, Koup RA, Moore JP, Пакстон В.А. Проникновение ВИЧ-1 в клетки CD4+ опосредовано хемокиновым рецептором CC-CKR-5. Природа. 1996 20 июня; 381 (6584): 667-73. [PubMed: 8649512]
- 3.
Ким М.Б., Гислер К.Е., Тахирович Ю.А., Труакс В.М., Лиотта Д.К., Уилсон Л.Дж. Антагонисты рецептора CCR5 на стадии доклинических и клинических исследований фазы II для лечения ВИЧ. Мнение эксперта по расследованию наркотиков. 2016 декабря; 25 (12): 1377-1392. [Бесплатная статья PMC: PMC5776690] [PubMed: 27791451]
- 4.
Стенсель-Баеренвальд Дж. Э., Рейсс К., Райтер Д. М., Штеле Т., Дермоди Т. С. Золотая середина: определение взаимодействия вируса и сиаловой кислоты. Nat Rev Microbiol. 2014 ноябрь;12(11):739-49. [Бесплатная статья PMC: PMC4791167] [PubMed: 25263223]
- 5.

Lee S, Mannstadt M, Guo J, Kim SM, Yi HS, Khatri A, Dean T, Okazaki M, Gardella TJ, Juppner H. Гомозиготная мутация [Cys25]PTH(1-84), нарушающая активацию рецептора PTH/PTHrP, определяет новую форму гипопаратиреоза. Джей Боун Шахтер Рез. 2015 Окт;30(10):1803-13. [Бесплатная статья PMC: PMC4580526] [PubMed: 25891861]
- 6.
Вайнштейн Л.С., Шенкер А., Гейман П.В., Мерино М.Дж., Фридман Э., Шпигель А.М. Активирующие мутации стимулирующего G-белка при синдроме МакКьюна-Олбрайта. N Engl J Med. 1991 12 декабря; 325 (24): 1688-95. [PubMed: 1944469]
- 7.
Хуанг К., Луо Ю.Б., Ян Х. Аутоиммунные каналопатии нервно-мышечного соединения. Фронт Нейрол. 2019;10:516. [Бесплатная статья PMC: PMC6533877] [PubMed: 31156543]
- 8.
Макфол М.Дж., Марчелли М., Зоппи С., Гриффин Д.Э., Уилсон Д.Д. Генетическая основа эндокринных заболеваний. 4. Спектр мутаций в гене рецептора андрогенов, обуславливающих резистентность к андрогенам.


 Такого физического
стимула, как боль, не существует, поэтому
выделение их в отдельную группу по
природе раздражителя в некоторой
степени условно. В действительности,
они представляют собой высокопороговые
сенсоры различных (химических,
термических или механических)
повреждающих факторов. Однако уникальная
особенность ноцицепторов, которя не
позволяет отнести их, например, к
«высокопороговым терморецепторам»,
состоит в том, что многие из них
полимодальны: одно и то же нервное
окончание способно возбуждаться в
ответ на несколько различных повреждающих
стимулов
Такого физического
стимула, как боль, не существует, поэтому
выделение их в отдельную группу по
природе раздражителя в некоторой
степени условно. В действительности,
они представляют собой высокопороговые
сенсоры различных (химических,
термических или механических)
повреждающих факторов. Однако уникальная
особенность ноцицепторов, которя не
позволяет отнести их, например, к
«высокопороговым терморецепторам»,
состоит в том, что многие из них
полимодальны: одно и то же нервное
окончание способно возбуждаться в
ответ на несколько различных повреждающих
стимулов  Она богата кровеносными
сосудами и пигментом (богатые пигментом
клетки хориоидеи препятствуют
проникновению света через склеру,
устраняя светорассеяние). Она
образована радужкой, ресничным
телом и собственно
сосудистой оболочкой.
В центре радужки имеется круглое
отверстие — зрачок, через которое
лучи света проникают внутрь глазного
яблока и достигают сетчатки (величина
зрачка изменяется в результате
взаимодействия гладких мышечных
волокон — сфинктера и
дилататора, заключённых в радужке и
иннервируемых парасимпатическим и симпатическимнервами).
Радужка содержит различное количество
пигмента, от которого зависит её
окраска — «цвет
глаз».
Она богата кровеносными
сосудами и пигментом (богатые пигментом
клетки хориоидеи препятствуют
проникновению света через склеру,
устраняя светорассеяние). Она
образована радужкой, ресничным
телом и собственно
сосудистой оболочкой.
В центре радужки имеется круглое
отверстие — зрачок, через которое
лучи света проникают внутрь глазного
яблока и достигают сетчатки (величина
зрачка изменяется в результате
взаимодействия гладких мышечных
волокон — сфинктера и
дилататора, заключённых в радужке и
иннервируемых парасимпатическим и симпатическимнервами).
Радужка содержит различное количество
пигмента, от которого зависит её
окраска — «цвет
глаз».
 [Бесплатная статья PMC: PMC8820210] [PubMed: 33880754]
[Бесплатная статья PMC: PMC8820210] [PubMed: 33880754]
