Регистр лекарственных средств России РЛС Пациент 2003.
Листать назад Оглавление Листать вперёд
Строение автономной нервной системы, управляющей нашими органами независимо от сознания, ее функции. Участие в приспособительных реакциях организма. Механизм передачи нервного импульса (строение синапса). Ацетилхолин и норадреналин – основные посредники этой системы и их эффекты.
Почему мы не можем по своему желанию остановить собственное сердце или прекратить процесс переваривания пищи в желудке, почему внезапный испуг заставляет сильнее биться сердце? Существует отдельная часть нервной системы человека, которая управляет многими непроизвольными функциями нашего организма. Она называется вегетативной нервной системой. Это автономная нервная система, активность которой не контролируется нашим сознанием. Под контролем этой системы находится активность различных желез, сокращение гладких мышц, работа почек, сокращение сердца и многие другие функции.
Вегетативная нервная система поддерживает на заданном природой уровне кровяное давление, потоотделение, температуру тела, обменные процессы, деятельность внутренних органов, кровеносных и лимфатических сосудов. Вместе с эндокринной системой, о которой мы будем рассказывать в следующей главе, она регулирует постоянство состава крови, лимфы, тканевой жидкости (внутренней среды) в организме, управляет обменом веществ и осуществляет взаимодействие отдельных органов в системах органов (дыхания, кровообращения, пищеварения, выделения и размножения).
Строение вегетативной нервной системы.
Вегетативная нервная система состоит из симпатического и парасимпатического отделов. | |||
Функции их, как правило, противоположны (рисунок 1.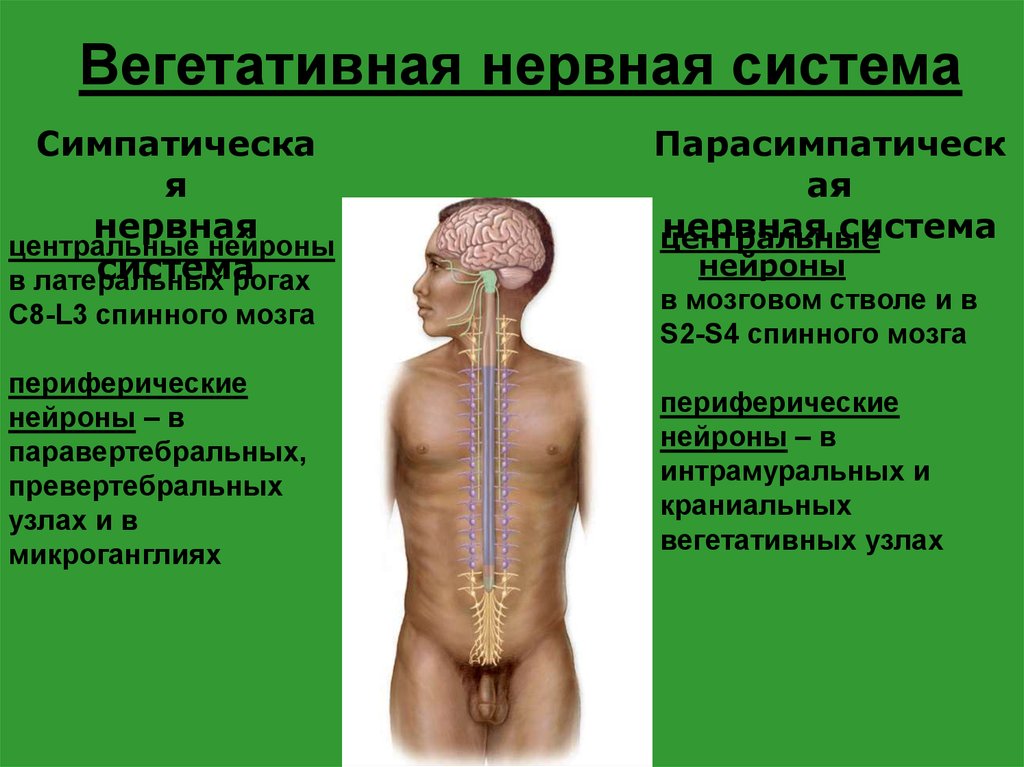 5.17). Как видно из рисунка 1.5.17, если нервы симпатического отдела стимулируют какую-то реакцию, то нервы парасимпатического ее подавляют. Эти процессы разнонаправленного воздействия друг на друга в конечном итоге взаимно уравновешивают друг друга, в результате функция поддерживается на соответствующем уровне. Именно на возбуждение или торможение одного из таких противоположных по своей направленности влияний часто направлено действие лекарств.
5.17). Как видно из рисунка 1.5.17, если нервы симпатического отдела стимулируют какую-то реакцию, то нервы парасимпатического ее подавляют. Эти процессы разнонаправленного воздействия друг на друга в конечном итоге взаимно уравновешивают друг друга, в результате функция поддерживается на соответствующем уровне. Именно на возбуждение или торможение одного из таких противоположных по своей направленности влияний часто направлено действие лекарств.
Возбуждение симпатических нервов вызывает расширение сосудов головного мозга, кожи, периферических сосудов; расширение зрачка; снижение выделительной функции слюнных желез и усиление – потовых; расширение бронхов; ускорение и усиление сердечных сокращений; сокращение мышц, поднимающих волосы; ослабление моторики желудка и кишечника; усиление секреции гормонов надпочечников; расслабление мочевого пузыря; оказывает возбуждающее действие на половые органы, вызывает сокращение матки. По парасимпатическим нервным волокнам отдаются “приказы”, обратные по своей направленности: например, сосудам и зрачку – сузиться, мускулатуре мочевого пузыря – сократиться и так далее.
Вегетативная нервная система очень чувствительна к эмоциональному воздействию. Печаль, гнев, тревога, страх, апатия, половое возбуждение – эти состояния вызывают изменения функций органов, находящихся под контролем вегетативной нервной системы. Например, внезапный испуг заставляет сильнее биться сердце, дыхание становится более частым и глубоким, в кровь из печени выбрасывается глюкоза, прекращается выделение пищеварительного сока, появляется сухость во рту. Организм готовится к быстрой реакции на опасность и, если требуется, к самозащите. Так при длительном и сильном эмоциональном напряжении и возбуждении развиваются тяжелые заболевания, такие как:
гипертензия, коронарная болезнь сердца, язвенная болезнь желудка и многие другие.Представьте себе прогулку по холмистой местности. Пока дорога проходит по ее равнинной части, вы идете не спеша, дыхание ровное, и сердце бьется спокойно. При этом каждая клетка организма всегда помнит генетически запрограммированный оптимальный режим своего функционирования и далее стремится поддерживать его как эталонный. Мы уже упоминали в разделе 1.4.1, что свойство живого организма осуществлять деятельность, направленную на поддержание постоянства внутренней среды, называется гомеостазом.
Мы уже упоминали в разделе 1.4.1, что свойство живого организма осуществлять деятельность, направленную на поддержание постоянства внутренней среды, называется гомеостазом.
Затем дорога пошла в гору и, как только это произошло, ваше тело стало выполнять дополнительную работу по преодолению силы земного притяжения. На выполнение этой работы всем участвующим в ней клеткам организма потребовалась дополнительная энергия, поступающая за счет увеличения скорости сгорания энергоемких веществ, которые клетка получает из крови.
В момент, когда клетка стала сжигать этих веществ больше, чем приносит кровь при данной скорости кровотока, она сообщает вегетативной нервной системе о нарушении своего постоянного состава и отклонении от эталонного энергетического состояния. Центральные отделы вегетативной нервной системы при этом формируют управляющее воздействие, приводящее к комплексу изменений для восстановления энергетического голодания: учащению дыхания и сокращений сердца, ускорению распада белков, жиров и углеводов и так далее (рисунок 1.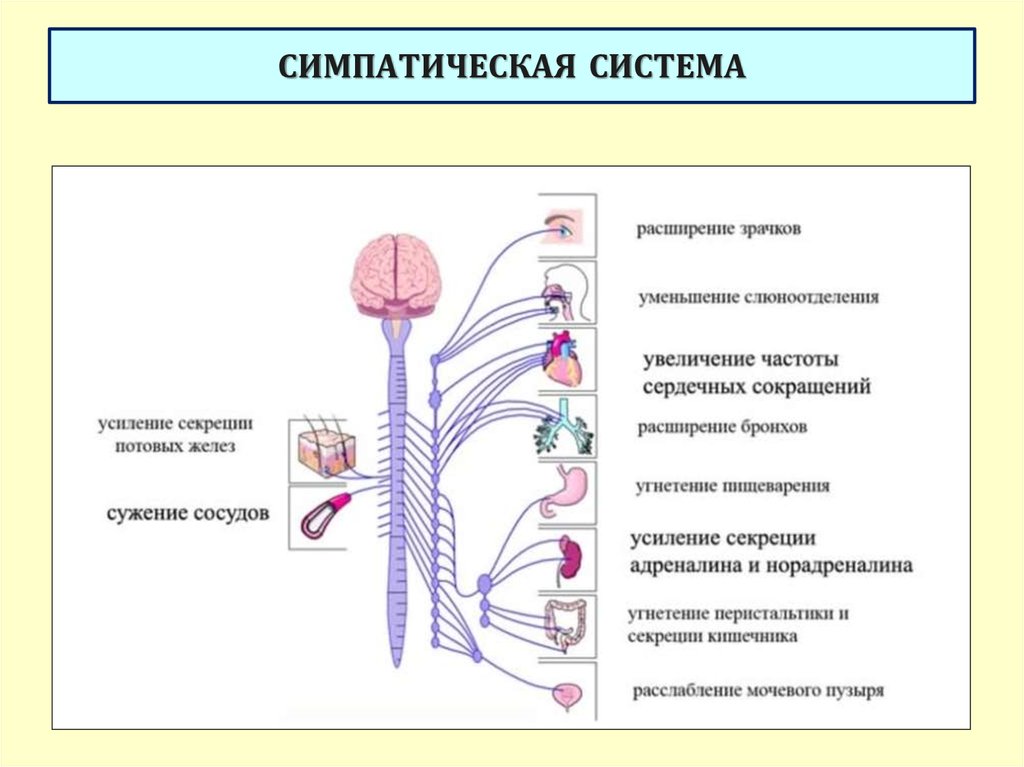 5.18).
5.18).
Рисунок 1.5.18. Функциональная модель описания вегетативной нервной системы
В результате, за счет увеличения количества поступающего в организм кислорода и скорости кровотока участвующая в работе клетка переходит на новый режим, при котором она отдает больше энергии в условиях повышения физической активности, но и потребляет ее больше ровно настолько, насколько необходимо для поддержания энергетического баланса, обеспечивающего клетке комфортное состояние. Таким образом, можно сделать вывод:
Поддержание постоянства внутренней среды клетки (гомеостаз) осуществляется за счет отрицательной обратной связи вегетативной нервной системы. | |||
И, хотя она действует автономно, то есть выключение сознания не приводит к прекращению ее работы (вы продолжаете дышать, и сердце бьется ровно), она реагирует на малейшие изменения в работе центральной нервной системы.
Для тех, кто хочет детальнее изучить работу вегетативной нервной системы, мы даем ее описание более подробно.
Как мы уже говорили выше, вегетативная нервная система представлена в центральных отделах симпатическими и парасимпатическими ядрами, расположенными в головном и спинном мозге, а на периферии – нервными волокнами и узлами (ганглиями).
Нервные волокна, составляющие ветки и веточки этой системы, расходятся по всему телу, сопровождаемые сетью кровеносных сосудов. Общая длина их составляет около 150 000 км.
В нашем теле все внутренние ткани и органы, “подчиненные” вегетативной нервной системе, снабжены нервами (иннервированы), которые, как датчики, собирают информацию о состоянии организма и передают ее в соответствующие центры, а от них доносят до периферии корректирующие воздействия.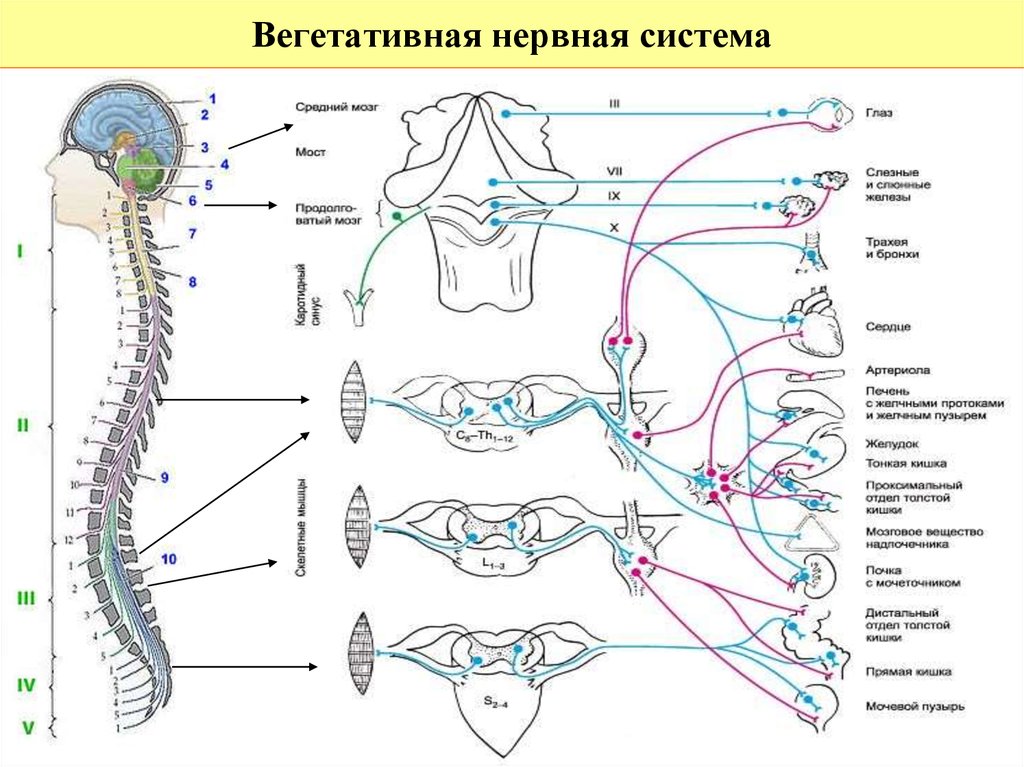
Так же как и центральная нервная система, вегетативная система имеет чувствительные (афферентные) окончания (входы), обеспечивающие возникновение ощущений, и исполнительные (двигательные, или эфферентные) окончания, которые передают из центра модифицирующие воздействия к исполнительному органу. Физиологически этот процесс выражается в чередовании процессов возбуждения и торможения, в ходе которых происходит передача нервных импульсов, возникающих в клетках нервной системы (
Переход нервного импульса с одного нейрона на другой или с нейронов на клетки исполнительных (эффекторных) органов осуществляется в местах контакта клеточных мембран, называемых синапсами (рисунок 1.5.19). Передача информации осуществляется специальными химическими веществами-посредниками (медиаторами), выделяемыми из нервных окончаний в синаптическую щель. В нервной системе эти вещества называют нейромедиаторами.
В нервной системе эти вещества называют нейромедиаторами.
Основными нейромедиаторами в вегетативной нервной системе являются ацетилхолин и норадреналин. | |||
В состоянии покоя эти медиаторы, вырабатываемые в нервных окончаниях, находятся в особых пузырьках. Попробуем коротко рассмотреть работу этих медиаторов на рисунке 1.5.20. Условно (так как он занимает считанные доли секунды) весь процесс передачи информации можно разбить на четыре этапа. Как только по пресинаптическому окончанию поступает импульс, на внутренней стороне клеточной мембраны за счет входа ионов натрия происходит образование положительного заряда, и пузырьки с медиатором начинают приближаться к пресинаптической мембране (этап I на рисунке 1.5.20). На втором этапе осуществляется выход медиатора в синаптическую щель из пузырьков в месте их контакта с пресинаптической мембраной.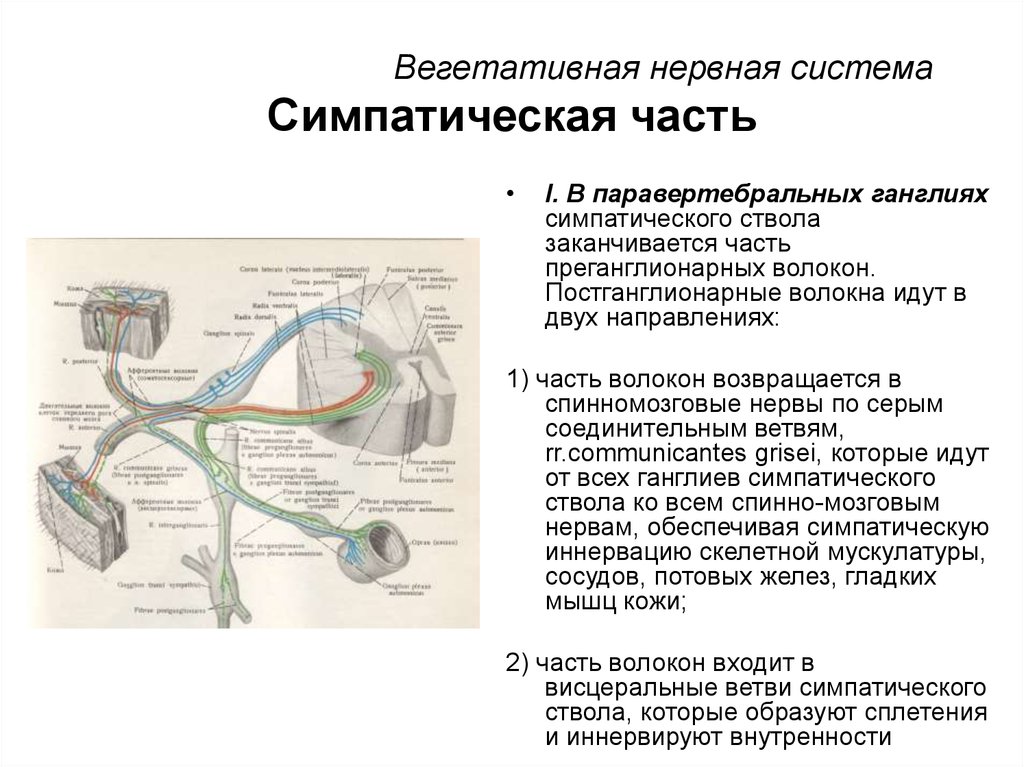 После выделения из нервных окончаний (этап II) нейромедиатор проникает через синаптическую щель путем диффузии
После выделения из нервных окончаний (этап II) нейромедиатор проникает через синаптическую щель путем диффузии
Рисунок 1. 5.20. Функционирование синапса:
5.20. Функционирование синапса:
I — поступление нервного импульса; II — выделение медиатора в синаптическую щель; III — взаимодействие с рецепторами постсинаптической мембраны; IV — «судьба» медиатора в Синаптической щели — возвращение синапса в состояние покоя
1- обратный захват медиатора; 2 — разрушение медиатора ферментом; 3- возбуждение пресинаптических рецепторов
Как мы уже говорили, в вегетативной нервной системе передача информации осуществляется, главным образом, с помощью нейромедиаторов – ацетилхолина и норадреналина. Поэтому пути передачи и синапсы называют холинергическими (медиатор – ацетилхолин) или адренергическими (медиатор – норадреналин). Аналогично этому рецепторы, с которыми связывается ацетилхолин, называют холинорецепторами, а рецепторы норадреналина – адренорецепторами (смотри схему на рисунке 1.5.21). На адренорецепторы влияет также гормон, выделяемый надпочечниками, – адреналин.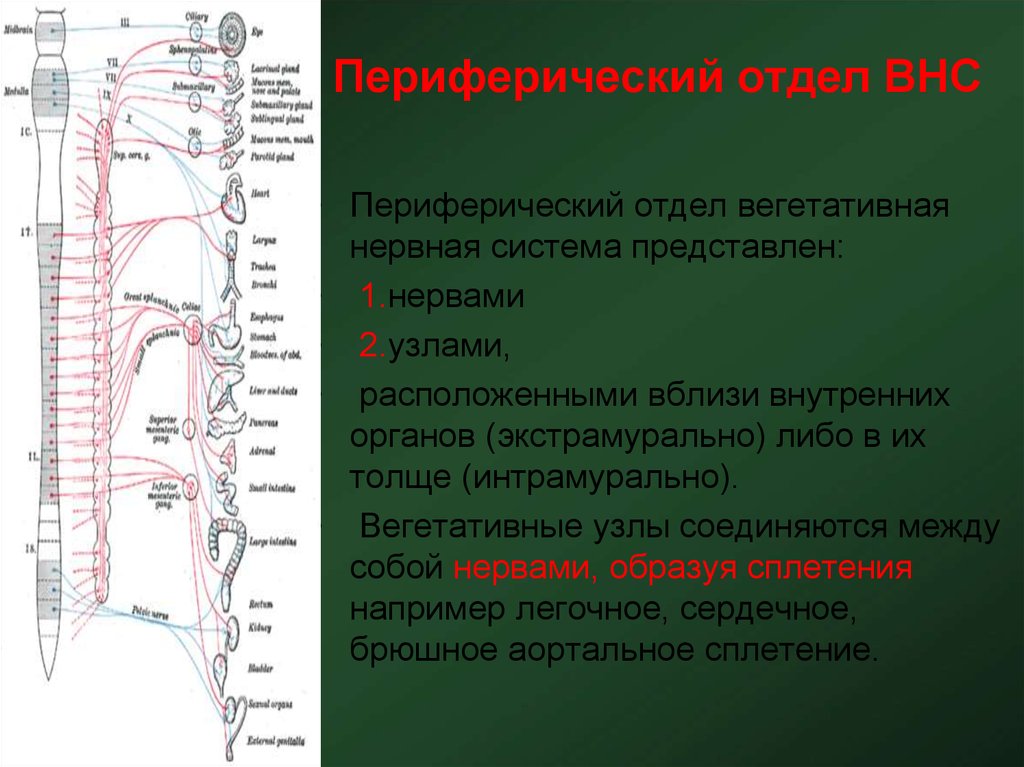
Рисунок 1.5.21. Общая схема передачи информации по звеньям вегетативной нервной системы
Холино- и адренорецепторы неоднородны и различаются чувствительностью к некоторым химическим веществам. Так, среди холинорецепторов выделяют мускаринчувствительные (м-холинорецепторы) и никотинчувствительные (н-холинорецепторы) – по названиям естественных алкалоидов, которые оказывают избирательное действие на соответствующие холинорецепторы. Мускариновые холинорецепторы, в свою очередь, могут быть м1-, м2— и м3-типа в зависимости от того, в каких органах или тканях они преобладают.
Адренорецепторы, исходя из различной чувствительности их к химическим соединениям, подразделяют на альфа- и бета-адренорецепторы, которые тоже в зависимости от локализации имеют несколько разновидностей.
Сеть нервных волокон пронизывает все человеческое тело, таким образом, холино- и адренорецепторы расположены по всему телу. Нервный импульс, распространяющийся по всей нервной сети или ее пучку, воспринимается как сигнал к действию теми клетками, которые имеют соответствующие рецепторы.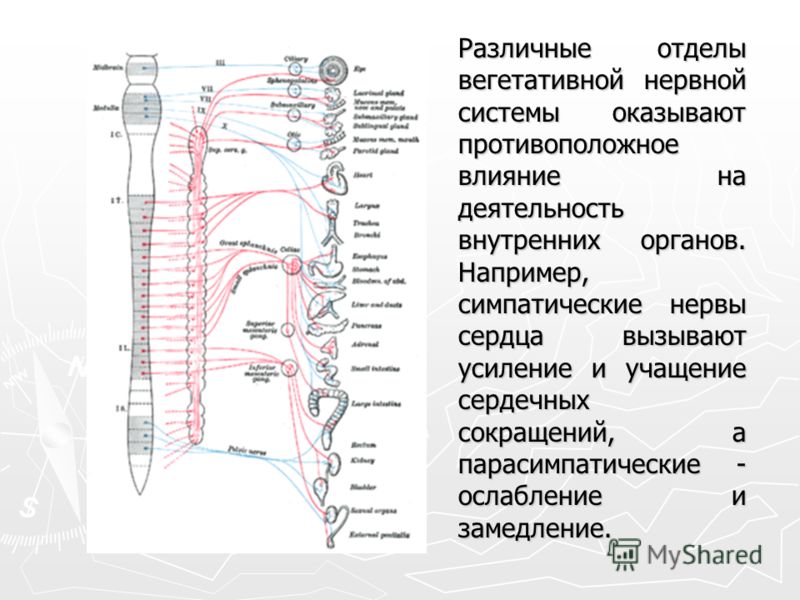 И, хотя холинорецепторы локализуются в большей степени в мышцах внутренних органов (желудочно-кишечного тракта, мочеполовой системы, глаз, сердца, бронхиол и других органов), а адренорецепторы – в сердце, сосудах, бронхах, печени, почках и в жировых клетках, обнаружить их можно практически в каждом органе. Воздействия, при реализации которых они служат посредниками, очень разнообразны.
И, хотя холинорецепторы локализуются в большей степени в мышцах внутренних органов (желудочно-кишечного тракта, мочеполовой системы, глаз, сердца, бронхиол и других органов), а адренорецепторы – в сердце, сосудах, бронхах, печени, почках и в жировых клетках, обнаружить их можно практически в каждом органе. Воздействия, при реализации которых они служат посредниками, очень разнообразны.
Препараты, влияющие на различные типы рецепторов, будут представлены в главе 3.2.
Листать назад Оглавление Листать вперёд
Страница не найдена
Размер:
AAA
Цвет: C C C
Изображения Вкл. Выкл.
Обычная версия сайта
RUENBY
Гомельский государственный
медицинский университет
- Университет
- Университет
- История
- Руководство
- Устав и Символика
- Воспитательная деятельность
- Организация образовательного процесса
- Международное сотрудничество
- Система менеджмента качества
- Советы
- Факультеты
- Кафедры
- Подразделения
- Первичная профсоюзная организация работников
- Издания университета
- Гордость университета
- Выпускник-2021
- Первичная организация «Белорусский союз женщин»
- Одно окно
- ГомГМУ в международных рейтингах
- Структура университета
- Абитуриентам
- Приёмная комиссия
- Целевая подготовка
- Заключение, расторжение «целевого» договора
- Льготы для молодых специалистов
- Архив проходных баллов
- Карта и маршрут проезда
- Порядок приёма на 2022 год
- Специальности
- Контрольные цифры приёма в 2022 году
- Стоимость обучения
- Информация о ходе приёма документов
- Приём документов и время работы приёмной комиссии
- Порядок приёма граждан РФ, Кыргызстана, Таджикистана, Казахстана
- Pепетиционное тестирование
- Горячая линия по вопросам вступительной кампании
- Студентам
- Первокурснику
- Расписание занятий
- Расписание экзаменов
- Информация для студентов
- Студенческий клуб
- Спортивный клуб
- Общежитие
- Нормативные документы
- Практика
- Стоимость обучения
- Безопасность жизнедеятельности
- БРСМ
- Профком студентов
- Учебный центр практической подготовки и симуляционного обучения
- Многофункциональная карточка студента
- Анкетирование студентов
- Выпускникам
- Интернатура и клиническая ординатура
- Докторантура
- Аспирантура
- Магистратура
- Распределение
- Врачам и специалистам
- Профессорский консультативный центр
- Факультет повышения квалификации и переподготовки
- Иностранным гражданам
- Факультет иностранных студентов
- Стоимость обучения
- Регистрация и визы
- Полезная информация
- Правила приёма
- Информация о возможностях и условиях приема в 2022 году
- Официальные представители ГомГМУ по набору студентов
- Страхование иностранных граждан
- Приём на Подготовительное отделение иностранных граждан
- Прием иностранных граждан для обучения на английском языке / Training of foreign students in English
- Повышение квалификации и переподготовка для иностранных граждан
- Научная деятельность
- Направления научной деятельности
- Научно-педагогические школы
- Студенчеcкое научное общество
- Инновационные технологии в ГомГМУ
- Научно-исследовательская часть
- Научно-исследовательская лаборатория
- Конкурсы, гранты, стипендии
- Работа комитета по этике
- Научные мероприятия
- В помощь исследователю
- Диссертационный совет
- «Горизонт Европа»
- Патенты
- Инструкции на метод
- Совет молодых ученых
- Госпрограмма (ЧАЭС)
- Главная
Биология Вегетативная нервная система
Материалы к уроку
Конспект урока
Вегетативная нервная система
|
Вегетативная нервная система регулирует кровообращение, дыхание, пищеварение, обмен веществ, выделение, деятельность эндокринных желез, то есть обеспечивает трофические функции организма и поддержание состава внутренней среды. В различных ситуациях внутренние органы нашего организма работают с разной интенсивностью. Например, когда человек бежит, начинают усиленно работать сердце, лёгкие и потовые железы, снабжая организм необходимой энергией и защищая от перегрева. Во время сна, наоборот, наш организм переходит в «энергосберегающий» режим. Сердце и лёгкие работают медленно, размерено, а вот пищеварительная система работает в полную силу, запасая энергию на будущее. Всё это возможно благодаря работе вегетативной нервной системы. Анатомически и функционально вегетативная система подразделяется на симпатическую и парасимпатическую. Экспериментально доказано, что симпатическая нервная система усиливает обмен веществ, повышает возбудимость большинства тканей, мобилизует силы организма на активную деятельность, особенно в стрессовых ситуациях. Парасимпатическая нервная система способствует восстановлению израсходованных запасов энергии, регулирует жизнедеятельность организма во время сна. Основной морфологической единицей вегетативной нервной системы, как и соматической, является нейрон. В вегетативной нервной системе тоже выделяют центральную и периферическую части. Центральную часть образуют тела нейронов, лежащих в спинном и головном мозге. Эти скопления нервных клеток получили название вегетативных ядер. Отходящие от ядер волокна лежат за пределами центральной нервной системы, и нервные сплетения в стенках внутренних органов образуют периферическую часть вегетативной нервной системы. Центры симпатического отдела находятся в боковых рогах серого вещества грудного и поясничного отделов спинного мозга. Волокна их нейронов, выходя за пределы спинного мозга, образуют околопозвоночные узлы симпатического отдела. Эти узлы проходят вдоль всего позвоночного столба, образуя два симпатических ствола — левый и правый. Нервные волокна, идущие от этих стволов, иннервируют все без исключения органы тела человека, в то время как область иннервации парасимпатических волокон более ограничена. Центры парасимпатической нервной системы находятся в мозговом стволе и в крестцовом отделе спинного мозга. Нервные волокна, отходящие от этих центров, регулируют аккомодацию глаза, деятельность основных внутренних органов, являются «запускающими» для выделения слюны, слезной и других жидкостей тела. Большинство внутренних органов получают двойную вегетативную иннервацию, так как к ним подходят как симпатические, так и парасимпатические нервные волокна, которые функционируют в тесном взаимодействии, но производят на органы противоположный эффект. Влияние вегетативной нервной системы на некоторые внутренние органы показано в таблице. (Чтение таблицы № 1) Вся деятельность вегетативной нервной системы построена по рефлекторному принципу. Строение рефлекторных дуг вегетативного отдела мало отличается от строения рефлекторных дуг соматической части нервной системы. Самая простая вегетативная рефлекторная дуга представлена тремя нейронами. Первое звено — это чувствительный нейрон, берущий начало в органах и тканях, и направляющий собранную информацию к соответствующим ядрам в спинной или головной мозг. Второе звено несёт импульсы из центральной нервной системы к рабочему органу. Этот путь представлен двумя нейронами, один из которых можно назвать вставочным, так как он находится между чувствительным звеном рефлекторной дуги и двигательным нейроном. Тела третьих нейронов лежат в периферических узлах вегетативной нервной системы. Отростки этих нейронов направляются к органам и тканям в составе вегетативных или смешанных нервов. Заканчиваются нервные волокна на гладких мышцах, железах и в других тканях. Вегетативные рефлексы часто наблюдают врачи для суждения о функциональном состоянии вегетативной нервной системы. Например, в клинике исследуют рефлекторные изменения сосудов при механическом раздражении кожи (проведение по коже карандашом). |
Таблица № 1
Влияние симпатического и парасимпатического отдела
|
Орган |
Действие симпатических нервов |
Действие парасимпатических органов |
|
Сердце |
Усиление и учащение сердечных сокращений |
Ослабление и замедление сердечных сокращений |
|
Артерии |
Сужение артерий и повышение кровяного давления |
Расширение артерий и понижение кровяного давления |
|
Пищеварительный тракт |
Замедление перистальтики, уменьшение активности |
Ускорение перистальтики, повышение активности |
|
Мочевой пузырь |
Расслабление пузыря |
Сокращение пузыря |
|
Мускулатура бронхов |
Расширение бронхов, облегчение дыхания |
Сокращение бронхов |
|
Мышечные волокна радужной оболочки |
Расширение зрачка |
Сужение зрачка |
|
Мышцы, поднимающие волосы |
Поднятие волос |
Прилегание волос |
|
Потовые железы |
Усиление секреции |
Ослабление секреции |
|
Слюнные железы |
Угнетают слюноотделение |
Усиливают слюноотделение |
Остались вопросы по теме? Наши репетиторы готовы помочь!
Подготовим к ЕГЭ, ОГЭ и другим экзаменам
Найдём слабые места по предмету и разберём ошибки
Повысим успеваемость по школьным предметам
Поможем подготовиться к поступлению в любой ВУЗ
Выбрать репетитора
Статья «Вегетативная дистония у детей»
Все органы и системы организма находятся под регулирующим воздействием нервной системы, состоящим из центрального отдела (головной мозг) и вегетативного отдела. Вегетативная нервная система при взаимодействии с корой головного мозга и эндокринной системой (щитовидная железа, гипофиз, надпочечники) принимает непосредственное участие в адаптации организма, регулирует реакции на любые стрессорные воздействия. Вегетативная нервная система состоит из 2 отделов: симпатический и парасимпатический. Симпатический отдел включаются в ситуациях, требующих напряженной психической и физической деятельности. Парасимпатический отдел проявляет свою основную функцию вне периода наряженной активности организма, преимущественно в период «отдыха».
Вегетативная нервная система при взаимодействии с корой головного мозга и эндокринной системой (щитовидная железа, гипофиз, надпочечники) принимает непосредственное участие в адаптации организма, регулирует реакции на любые стрессорные воздействия. Вегетативная нервная система состоит из 2 отделов: симпатический и парасимпатический. Симпатический отдел включаются в ситуациях, требующих напряженной психической и физической деятельности. Парасимпатический отдел проявляет свою основную функцию вне периода наряженной активности организма, преимущественно в период «отдыха».
«Синдром вегетативной дистонии» — это состояние, которое характеризуется нарушениями вегетативной (нервной) регуляции работы внутренних органов: сердечно-сосудистой системы, желудочно-кишечного тракта, органов дыхания, желез внутренней секреции. Изменения со стороны всех этих систем носят функциональный, т.е. обратимый характер и не представляют угрозы для жизни и здоровья ребенка. Причиной развития вегетативной дистонии являются наследственно — конституциональные факторы.
Дети с дистонией могут предъявлять самые разнообразные жалобы
Самые частые из них — головные боли, боли в области сердца и живота. Как правило, такие дети плохо переносят транспорт, душные помещения, могут быть головокружения и даже кратковременные потери сознания (обмороки). Нередко отмечается нестабильное артериальное давление, повышенная утомляемость, беспокойный сон, перемена настроения. Часто бывают внезапные ощущения проколов в левой половине грудной клетки, особенно на вдохе, сопровождающиеся чувством затрудненного дыхания, сердцебиения, бледностью.
Со стороны органов дыхания могут отмечаться приступы внезапной одышки, без видимых причин появляются глубокие «вздохи», так называемый «дыхательный невроз», приступы невротического, спазматического кашля.
При дистонии могут появляться боли и неприятные ощущения в области мышц ног, чувства онемения, преимущественно по вечерам, перед засыпанием — симптом «беспокойных ног».
Существует 2 варианта вегетативной дистонии:
- по ваготоническому типу
- по симпатикотоническому типу
При ваготоническом типе дети жалуются на частые головные боли, связанные с понижением артериального давления, боли в области сердца, редкий пульс, обморочные состояния в душных помещениях, чрезмерную потливость, зябкость, длительные сохранения субфебрильной (до 37.5) температуры после перенесенных инфекций. Часто бывают немотивированные боли в животе, тошнота, метеоризм. Такие дети быстро устают, у них повышенная тревожность, сонливость, утомляемость, склонность к депрессиям.
При симпатикотоническом типе дистонии у детей наоборот отмечаются сердцебиения, ускоренный пульс, склонность к повышенному давлению.
Верхние пределы артериального давления у детей:
- 7-9 лет 125/75
- 10-13 лет 130/80
- 14-17 лет 135/85
У таких детей часто бывают проявления «термоневроза» — повышение температуры тела на фоне стресса, колебания в течение суток, субфебрильная температура при отсутствии признаков заболевания. Такие дети обычно худые, несмотря на нормальный аппетит.
Такие дети обычно худые, несмотря на нормальный аппетит.
Рекомендации для родителей
В основе лечения вегетативной дистонии лежат немедикаментозные методы лечения.
Они включают в себя: правильную организацию труда и отдыха, соблюдение распорядка дня, занятия физической культурой, рациональное питание, водолечение и бальнеотерапию, физиотерапию, психотерапию. Необходимо устранить гиподинамию, так как физическая активность повышает тонус сердечно-сосудистой системы, улучшает обменные процессы и микроциркуляцию.
Прогулки на свежем воздухе должны быть не менее 2 часов в день. Освобождение от занятий физкультуры в школе не требуется.
Рекомендуемые занятия спортом: плавание, коньки, лыжи, игровые виды спорта, велосипед, легкая атлетика.
Не рекомендуется: бокс, все виды борьбы, тяжелая атлетика.
Ночной сон должен составлять не менее 8-10 часов, так как сон является основным регулятором циркадных биоритмов организма. Занятия за компьютером должны составлять не более 40 — 60 минут в день в зависимости от возраста ребенка.
Занятия за компьютером должны составлять не более 40 — 60 минут в день в зависимости от возраста ребенка.
Питание детей должно быть рациональным, с достаточным количеством минеральных веществ и витаминов. Нужно избегать избытка мучных продуктов, копченостей, животных жиров. При склонности к повышению АД необходимо ограничение соли, жидкости, высококалорийных продуктов. При ваготонической дистонии можно включать в рацион кофе, шоколад, крепкий чай, солености.
Очень эффективны водные процедуры:
- плавание
- лечебные ванны (солено — хвойные, кислородные, жемчужные)
- души (циркулярный, контрастный, подводный, душ Шарко, игольчатый)
В лечении дистонии широко используются физиотерапия и массаж. Занятия с психологом помогают детям снять излишнее напряжение, скоррегировать отношения с окружающими, снизить уровень тревоги.
А ты симпатическая
Автономная нервная система — важнейший «дирижер» организма, который в паре с эндокринной системой регулирует все телесные функции, не зависящие от сознательного контроля. Она была описана 130 лет назад, и казалось, что к настоящему времени изучена практически досконально, по меньшей мере анатомически и физиологически. Однако сейчас франко-британский научный коллектив пришел к небезосновательному выводу, что в классическом представлении об этой системе присутствует фундаментальная ошибка: граница между ее симпатическим и парасимпатическим отделами была проведена неправильно.
Она была описана 130 лет назад, и казалось, что к настоящему времени изучена практически досконально, по меньшей мере анатомически и физиологически. Однако сейчас франко-британский научный коллектив пришел к небезосновательному выводу, что в классическом представлении об этой системе присутствует фундаментальная ошибка: граница между ее симпатическим и парасимпатическим отделами была проведена неправильно.
Инь и ян автономной нервной системы
Автономная, или вегетативная, нервная система подразделяется на два отдела с практически противоположными эффектами: симпатический, который отвечает за реакцию на стресс («борьба или бегство»), и парасимпатический, который поддерживает гомеостаз («отдых и пищеварение»). Эти отделы различаются по развитию в ходе формирования организма, анатомическому строению и биохимии.
Сигналы автономной системы идут от соответствующих ядер ЦНС
(головного и спинного мозга) по нервным волокнам к нейронам периферических
ганглиев (нервных узлов), которые, в свою очередь, передают эти сигналы к
внутренним органам.
При этом ганглии симпатической системы расположены сегментарно рядом с позвоночником, то есть ее преганглионарные нервные волокна короткие, а постганглионарные длинные. Нервные узлы парасимпатической системы анатомически связаны с органами, которые они иннервируют, то есть ее преганглионарные волокна идут по длинным нервам из ЦНС, а постганглионарные коротки.
Во всех преганглионарных и парасимпатических постганглионарных волокнах нейромедиатором служит ацетилхолин, а в симпатических постганглионарных — норадреналин.
Особый отдел автономной нервной системы представляет собой нервная система кишечника: помимо вышеперечисленных структур, в ней присутствуют еще сенсорные и вставочные нейроны, из-за чего некоторые специалисты предлагают выделить ее в собственный отдел вегетатики. Но речь сейчас не о ней.
В процессе развития симпатические ганглии образуются в
результате прямой миграции клеток нервного гребня из нервной трубки
(предшественницы ЦНС). Формирование парасимпатических ганглиев зависит от роста
преганглионарных нервных волокон, которые доставляют клетки-предшественницы
нейронов к месту будущего узла. Такая разница в образовании ганглиев связана с
экспрессией разных факторов транскрипции в будущих симпатических и
парасимпатических нейронах.
Такая разница в образовании ганглиев связана с
экспрессией разных факторов транскрипции в будущих симпатических и
парасимпатических нейронах.
Интуиция подвела
Со времен классического труда британского физиолога Уолтера Гаскелла (Walter Gaskell) считалось, что парасимпатическую иннервацию осуществляют длинные черепные нервы (глазодвигательный, лицевой, языкоглоточный и — основной — блуждающий), берущие начало в ядрах среднего и промежуточного мозга и регулирующие работу глаз, слизистой оболочки носа, желез и внутренних органов до нижних отделов толстой кишки, а также крестцовые чревные нервы, которые начинаются в ядрах боковых рогов крестцового отдела спинного мозга и регулируют работу тазовых органов.
Поводом для этого стали некоторые особенности крестцовых
нервов. Анатомически они менее разветвлены, чем симпатические нервы грудного и
поясничного отделов, их ганглии расположены дальше от позвоночника, и они
иннервируют внутренние органы, до которых не доходят ветви блуждающего нерва.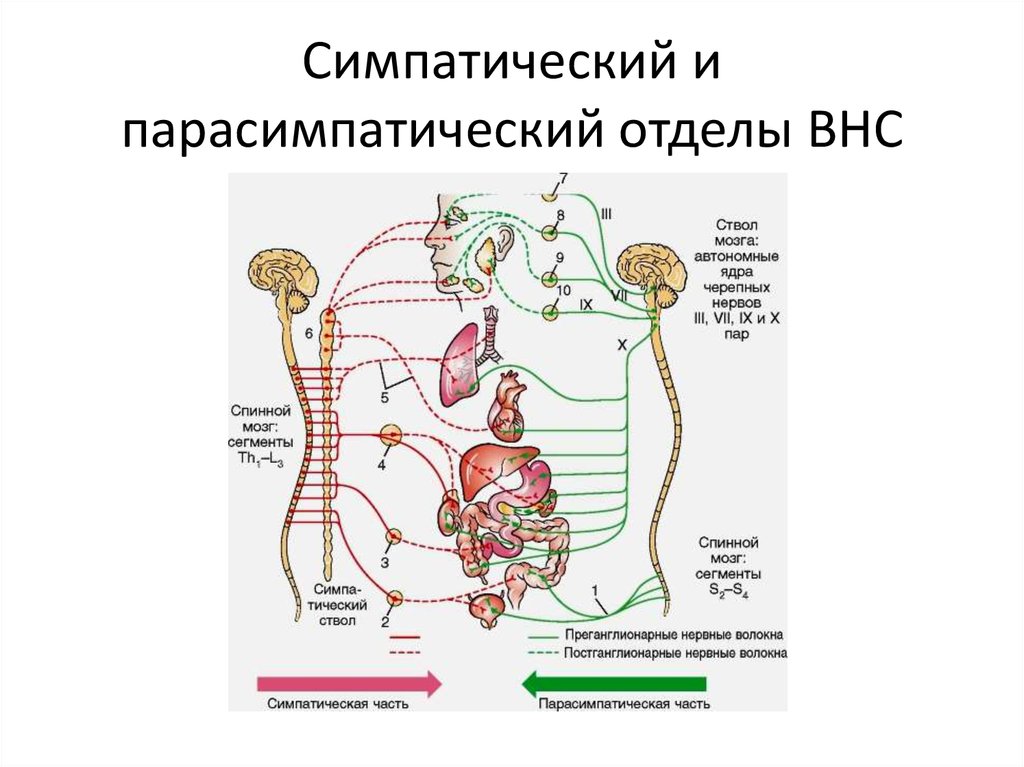 Физиологически крестцовые нервы действуют на некоторые органы противоположно грудным
и поясничным. И, наконец, фармакологически иннервируемые ими органы
чувствительны к блокаторам постганглионарных рецепторов к ацетилхолину.
Физиологически крестцовые нервы действуют на некоторые органы противоположно грудным
и поясничным. И, наконец, фармакологически иннервируемые ими органы
чувствительны к блокаторам постганглионарных рецепторов к ацетилхолину.
Классическое представление об устройстве симпатической (красный цвет) и парасимпатической (синий цвет) нервных систем
Anatomy of the Human Body, Henry Gray, 1918 / Wikimedia Commons
Поделиться
Правомерность отнесения крестцовых чревных нервов к парасимпатической системе уже ставили под сомнение, поскольку волокна черепных нервов отходят от ЦНС дорсально (со стороны спины), а крестцовых чревных — вентрально (со стороны груди и живота), как и симпатические волокна. Это, в свою очередь, указывает на разные источники их развития в эмбриональном периоде. Однако к переписыванию учебников это не привело.
Вся парасимпатика — от головы
Спустя 130 лет после выхода статьи Гаскелла сотрудники
Парижского исследовательского университета естественных и гуманитарных наук и
Лондонского университетского колледжа убедительно подтвердили подобные сомнения,
исследовав развитие пре- и постганглионарных нейронов у мышей.
Они выяснили, что, в отличие от клеток-предшественниц парасимпатических нейронов, которые экспрессируют факторы транскрипции Sox10, Phox2b, Tbx20, Tbx2 и Tbx3, будущие тазовые ганглионарные клетки экспрессируют Sox10 и FoxP1, как и симпатические нейроны. Более того, формирование тазовых ганглиев оказалось независимым от преганглионарных нервных волокон и происходило даже в их отсутствие, что для парасимпатических ганглиев нехарактерно. Образование этих нервных узлов в присутствии преганглионарных крестцовых волокон и без них показано на видео вверху и внизу соответственно.
На 14 день эмбрионального развития в нейронах ядер блуждающих
нервов происходил синтез везикулярного переносчика ацетилхолина (VAChT) и
отсутствовала синтаза оксида азота (NOS), а в спинномозговых ядрах грудных,
поясничных и крестцовых нервов — наоборот.
Также ученые показали, что нейроны тазовых ганглиев экспрессируют факторы транскрипции Isl1, Gata3 и Hand1, как и клетки симпатических ганглиев, и не вырабатывают факторы Hmx2 и Hmx3, служащие маркерами парасимпатических ганглионарных нейронов.
Новое представление об устройстве симпатической (красный цвет) и парасимпатической (синий цвет) нервных систем
I. Espinosa-Medina et al., Science, 2016
Поделиться
Полученные результаты красноречиво свидетельствуют о том, что крестцовые чревные нервы и тазовые ганглии относятся к симпатической нервной системе. Таким образом, вся парасимпатическая иннервация исходит только от черепных нервов, и тазовые органы ее лишены.
Лечить по-новому
Подобные выводы в корне меняют взгляды на эволюцию,
развитие, анатомию и физиологию автономной нервной системы и тазовых органов. Это,
в свою очередь, должно изменить понимание развития заболеваний нижнего отдела спинного мозга, крестцовых нервов и
тазовых органов, а следовательно, и подходы к их лечению, как имеющиеся, так и перспективные.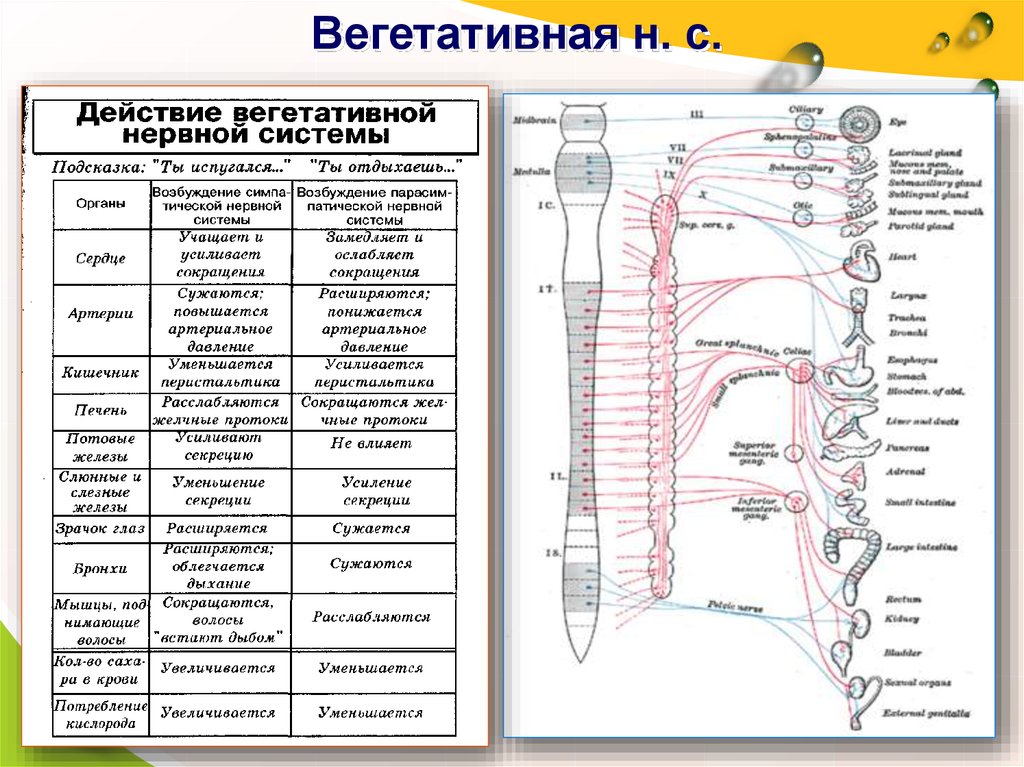
Как пишет автор сопутствующей статьи Игорь Адамейко из Каролинского института в Стокгольме и Венского медицинского университета, полученные данные имеют большое значение для развивающейся сферы биомедицины — электроцевтики, или биоэлектронной медицины. Ее целью является лечение широкого спектра хронических заболеваний с помощью миниатюрных автономных устройств с микропроцессорами («нервной пыли»), имплантируемых непосредственно в нервы. Эти устройства модифицируют нервные импульсы так, чтобы нормализовать нарушенные функции пораженных органов. Подобное вмешательство схоже с успешно применяемой электростимуляцией мозга, но действует на уровне отдельных нервов или нервных волокон. Для успеха подобного лечения необходимо четко понимать, является интересующий нерв симпатическим или парасимпатическим.
Биоэлектронный чип на нервном волокне в представлении художника
GSK
Поделиться
Разработками в области электроцевтики занимается новый проект Galvani
Bioelectronics, созданный Verily Life Sciences (дочкой компании Alphabet,
которой принадлежит Google) и британским фармгигантом GlaxoSmithKline. На
протяжении первых семи лет работы партнеры намерены вложить в этот проект 540
миллионов фунтов стерлингов.
На
протяжении первых семи лет работы партнеры намерены вложить в этот проект 540
миллионов фунтов стерлингов.
Помимо электроцевтики, пересмотр иннервации тазовых органов имеет значение для развивающейся клеточной медицины, отмечает Адамейко. В случае восстановления поврежденных крестцовых нервов и тазовых ганглиев с помощью стволовых клеток врачам и ученым необходимо понимать, какие клетки-предшественницы использовать и как направлять их дифференцировку.
Олег Лищук
ВЕГЕТАТИВНАЯ НЕРВНАЯ СИСТЕМА • Большая российская энциклопедия
Авторы: О. Л. Виноградова, О. С. Тарасова
ВЕГЕТАТИ́ВНАЯ НЕ́РВНАЯ СИСТЕ́МА, часть нервной системы позвоночных животных и человека, которая регулирует деятельность органов кровообращения, пищеварения, дыхания, выделения, размножения, обмен веществ и рост организма; играет ведущую роль в поддержании гомеостаза и в приспособительных реакциях организма. Термин «В. н.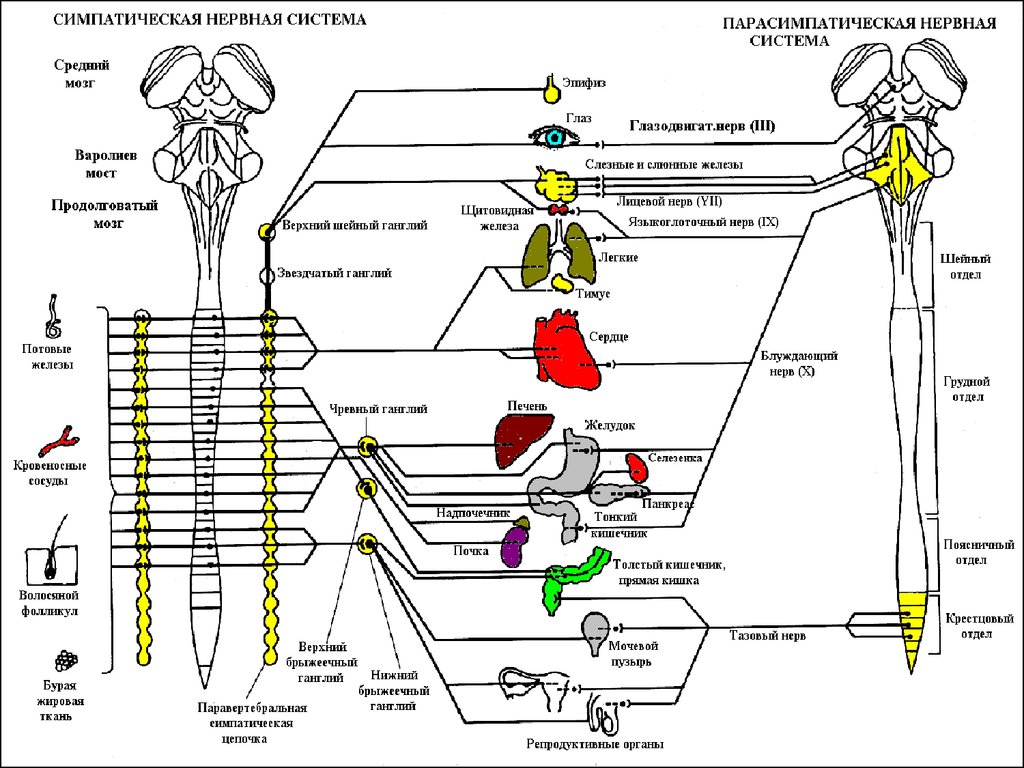 с.» ввёл в 1800 М. Биша, исходя из того, что эта часть нервной системы регулирует процессы, свойственные не только животным, но и др. организмам. Поскольку функции В. н. с. не могут быть произвольно вызваны или сознательно прекращены, англ. физиолог Дж. Ленгли назвал её автономной.
с.» ввёл в 1800 М. Биша, исходя из того, что эта часть нервной системы регулирует процессы, свойственные не только животным, но и др. организмам. Поскольку функции В. н. с. не могут быть произвольно вызваны или сознательно прекращены, англ. физиолог Дж. Ленгли назвал её автономной.
Схема строения и связей вегетативной нервной системы человека: I – шейный отдел спинного мозга, II – грудной, III – поясничный, IV – крестцовый. Синим обозначена парасимпатичес…
Анатомически и функционально В. н. с. делится на симпатическую нервную систему (СНС), парасимпатическую нервную систему (ПНС) и метасимпатическую нервную систему (МНС). В СНС и ПНС эфферентные пути, исходящие от центральной нервной системы (ЦНС), состоят из двух последовательно связанных нейронов. Клеточные тела первых нейронов СНС лежат в грудном и поясничном отделах спинного мозга, а ПНС – в среднем и продолговатом мозге и в крестцовом отделе спинного мозга. Вторые нейроны (расположены вне ЦНС) образуют ганглии вблизи позвоночника, по пути к органам (в СНС), недалеко от иннервируемого органа или непосредственно в нём (в ПНС). Влияние ПНС на работу мн. органов (сердца, почек и др.) обеспечивается гл. обр. через блуждающий нерв. Для нервных волокон В. н. с. характерна малая скорость проведения сигналов по сравнению с ЦНС. В ганглиях СНС и ПНС передатчиком сигналов служит ацетилхолин; он же выделяется из постганглионарных волокон ПНС. В СНС эту роль играет норадреналин (редко – ацетилхолин). Вместе с норадреналином и ацетилхолином могут использоваться др. медиаторы.
Вторые нейроны (расположены вне ЦНС) образуют ганглии вблизи позвоночника, по пути к органам (в СНС), недалеко от иннервируемого органа или непосредственно в нём (в ПНС). Влияние ПНС на работу мн. органов (сердца, почек и др.) обеспечивается гл. обр. через блуждающий нерв. Для нервных волокон В. н. с. характерна малая скорость проведения сигналов по сравнению с ЦНС. В ганглиях СНС и ПНС передатчиком сигналов служит ацетилхолин; он же выделяется из постганглионарных волокон ПНС. В СНС эту роль играет норадреналин (редко – ацетилхолин). Вместе с норадреналином и ацетилхолином могут использоваться др. медиаторы.
Влияние СНС и ПНС на органы часто противоположно. Так, активация СНС приводит к расширению бронхов, увеличению силы и частоты сокращений сердца, расширению зрачков, угнетению перистальтики желудочно-кишечного тракта и секреции пищеварит. соков, расслаблению мочевого пузыря, а активация ПНС вызывает обратный эффект. СНС и ПНС присуща тоническая (поддерживающаяся) активность: напр., увеличение частоты сокращений сердца может достигаться активацией СНС или торможением ПНС. Эффекты могут иметь одинаковую направленность, но различаться особенностями проявления: напр., ПНС вызывает обильную секрецию жидкой слюны, а СНС – умеренную секрецию вязкой. В отношении ряда функций эффекты двух отделов могут суммироваться; так, ПНС стимулирует эрекцию, а СНС – эякуляцию. Некоторые функции регулируются только ПНС (напр., работа слёзных желёз) или СНС (расщепление гликогена и жиров, увеличение работоспособности скелетной мускулатуры, работа потовых желёз). Во многих органах (кроме головного мозга, языка, пищеварительных желёз, половых органов) тонус сосудов также поддерживается только СНС.
соков, расслаблению мочевого пузыря, а активация ПНС вызывает обратный эффект. СНС и ПНС присуща тоническая (поддерживающаяся) активность: напр., увеличение частоты сокращений сердца может достигаться активацией СНС или торможением ПНС. Эффекты могут иметь одинаковую направленность, но различаться особенностями проявления: напр., ПНС вызывает обильную секрецию жидкой слюны, а СНС – умеренную секрецию вязкой. В отношении ряда функций эффекты двух отделов могут суммироваться; так, ПНС стимулирует эрекцию, а СНС – эякуляцию. Некоторые функции регулируются только ПНС (напр., работа слёзных желёз) или СНС (расщепление гликогена и жиров, увеличение работоспособности скелетной мускулатуры, работа потовых желёз). Во многих органах (кроме головного мозга, языка, пищеварительных желёз, половых органов) тонус сосудов также поддерживается только СНС.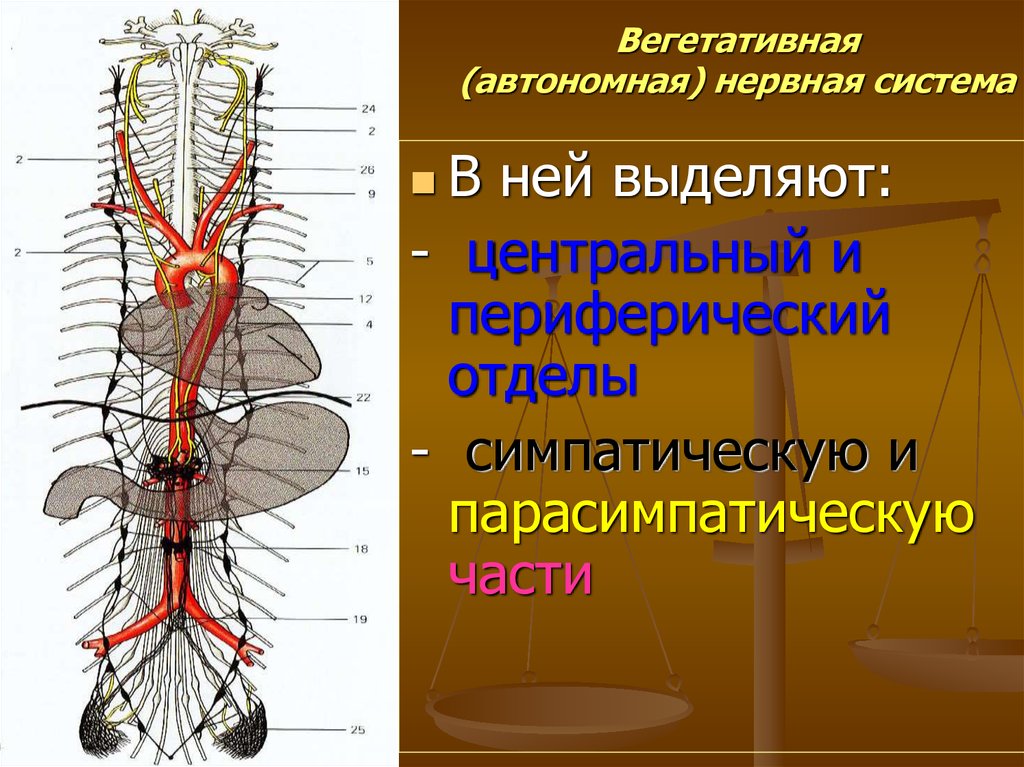 В целом, ПНС отвечает за восстановление затраченных организмом ресурсов, а СНС обеспечивает его адаптацию к экстремальным условиям.
В целом, ПНС отвечает за восстановление затраченных организмом ресурсов, а СНС обеспечивает его адаптацию к экстремальным условиям.
МНС (термин введён А. Д. Ноздрачёвым) иннервирует внутренние органы, наделённые собственной моторной активностью: желудок и кишечник (ауэрбаховское сплетение, мейснерово сплетение), мочевой пузырь, сердце и др. Она имеет собственные чувствительные и вставочные нейроны и чрезвычайно разнообразна по набору медиаторов. После повреждения МНС органы утрачивают способность к координированным ритмич. сокращениям.
Работа МНС автономна, но регулируется СНС и ПНС. Деятельность СНС и ПНС управляется нервными центрами (дыхательным, сердечно-сосудистым, слюноотделительным и др.), которые расположены в продолговатом мозге. На этом уровне работа центров может изменяться рефлекторно и независимо от других. Такие рефлексы находятся под контролем гипоталамуса. Сигналы, поступающие от коры больших полушарий головного мозга, также изменяют активность В. н. с., что обеспечивает целостную реакцию организма на раздражители.
Такие рефлексы находятся под контролем гипоталамуса. Сигналы, поступающие от коры больших полушарий головного мозга, также изменяют активность В. н. с., что обеспечивает целостную реакцию организма на раздражители.
Части нервной системы, обеспечивающие координацию работы внутренних органов у беспозвоночных, называются висцеральными. Их элементы обнаруживаются у низших червей как образования, связанные с кишечной трубкой, а начиная с немертин и кольчатых червей формируются самостоятельные ганглии. У членистоногих достаточно чётко выявляется система ганглиев и нервных стволов, идущих к сердцу, мышцам желудка, но лишь у насекомых обособляются головной и хвостовой отделы, иногда сравниваемые с ПНС позвоночных, и туловищный отдел, сопоставимый с СНС.
Анатомия, вегетативная нервная система — StatPearls
Книжная полка NCBI. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2022 янв.
StatPearls [Интернет].
Показать подробности
Критерий поиска
Джошуа А. Ваксенбаум; Вамси Редди; Мэтью Варакалло.
Информация об авторе
Последнее обновление: 29 июля 2021 г.
Введение
Вегетативная нервная система представляет собой компонент периферической нервной системы, который регулирует непроизвольные физиологические процессы, включая частоту сердечных сокращений, артериальное давление, дыхание, пищеварение и половое возбуждение. Он состоит из трех анатомически различных отделов: симпатического, парасимпатического и энтерального отделов.
Симпатическая нервная система (СНС) и парасимпатическая нервная система (ПНС) содержат как афферентные, так и эфферентные волокна, которые обеспечивают сенсорный вход и двигательный выход, соответственно, в центральную нервную систему (ЦНС). Как правило, двигательные пути СНС и ПНС состоят из серии из двух нейронов: преганглионарного нейрона с телом клетки в ЦНС и постганглионарного нейрона с телом клетки на периферии, иннервирующих ткани-мишени. Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Как правило, двигательные пути СНС и ПНС состоят из серии из двух нейронов: преганглионарного нейрона с телом клетки в ЦНС и постганглионарного нейрона с телом клетки на периферии, иннервирующих ткани-мишени. Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Активация СНС приводит к состоянию общей повышенной активности и внимания: реакция «бей или беги». При этом повышается артериальное давление и частота сердечных сокращений, происходит гликогенолиз, прекращается перистальтика желудочно-кишечного тракта и т.д.[5] СНС иннервирует почти все живые ткани в организме. ПНС способствует процессам «отдыха и переваривания»; снижается частота сердечных сокращений и артериальное давление, возобновляется перистальтика желудочно-кишечного тракта / пищеварение и т.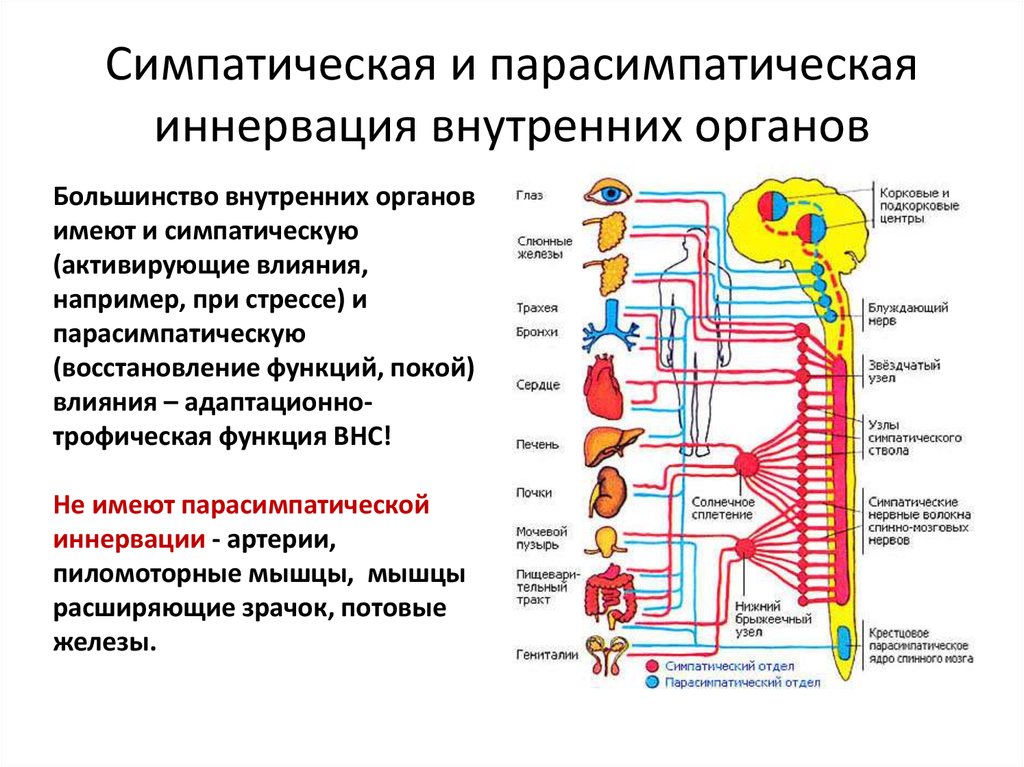 д. [5] [6] ПНС иннервирует только голову, внутренние органы и наружные гениталии, в значительной степени вакантна в большей части костно-мышечной системы и кожи, что делает ее значительно меньше, чем СНС.[7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
д. [5] [6] ПНС иннервирует только голову, внутренние органы и наружные гениталии, в значительной степени вакантна в большей части костно-мышечной системы и кожи, что делает ее значительно меньше, чем СНС.[7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
Пресинаптические нейроны как СНС, так и ПНС используют ацетилхолин (АХ) в качестве нейротрансмиттера. Постсинаптические симпатические нейроны обычно продуцируют норадреналин (НЭ) в качестве своего эффекторного передатчика для воздействия на ткани-мишени, в то время как постсинаптические парасимпатические нейроны повсеместно используют АХ. Известно, что энтеральные нейроны используют несколько основных нейротрансмиттеров, таких как АХ, закись азота и серотонин, и это лишь некоторые из них.[8]
Структура и функция
Симпатическая нервная система
Симпатические нейроны имеют клеточные тела, расположенные в промежуточных латеральных столбах или латеральных рогах спинного мозга. Пресинаптические волокна выходят из спинного мозга через передние корешки и входят в передние ветви спинномозговых нервов T1-L2 и в симпатические стволы через белые соединительные ветви. Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Пресинаптические волокна выходят из спинного мозга через передние корешки и входят в передние ветви спинномозговых нервов T1-L2 и в симпатические стволы через белые соединительные ветви. Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Паравертебральные ганглии существуют в виде узелков по всему симпатическому стволу, прилегающему к позвоночнику, где происходит синапс пре- и постганглионарных нейронов. Хотя количество может варьироваться в зависимости от человека, как правило, существует три шейных, 12 грудных, четыре поясничных и пять крестцовых ганглиев.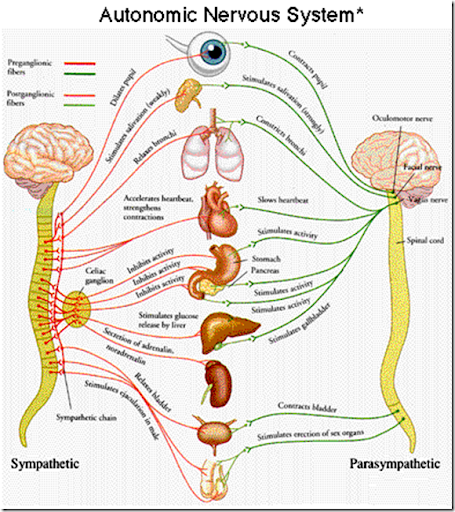 Из них только шейные имеют названия верхних, средних и нижних шейных ганглиев. Нижний шейный ганглий может сливаться с первым грудным ганглием, образуя звездчатый ганглий.
Из них только шейные имеют названия верхних, средних и нижних шейных ганглиев. Нижний шейный ганглий может сливаться с первым грудным ганглием, образуя звездчатый ганглий.
Все нервы, расположенные дистальнее паравертебральных ганглиев, являются внутренностными нервами. Они передают афферентные и эфферентные волокна между ЦНС и внутренними органами. Сердечно-легочные внутренностные нервы несут постсинаптические волокна, направляющиеся в грудную полость.
Нервы, которые будут иннервировать органы брюшной полости и таза, проходят через паравертебральные нервы без образования синапсов, становясь внутрибрюшными тазовыми нервами. Эти нервы включают большой, малый, наименьший и поясничный внутренностные нервы. Пресинаптические нервы, наконец, образуют синапсы в превертебральных ганглиях, которые находятся ближе к органу-мишени. Предвертебральные ганглии входят в состав нервных сплетений, окружающих ветви аорты. К ним относятся чревный, аортокоренальный, а также верхний и нижний брыжеечные ганглии. Чревный ганглий получает вход от большого внутренностного нерва, аортокоренальный от малого и наименьшего внутренностного нерва, а верхний и нижний брыжеечные от наименьшего и поясничного внутренностного нервов. Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.
Чревный ганглий получает вход от большого внутренностного нерва, аортокоренальный от малого и наименьшего внутренностного нерва, а верхний и нижний брыжеечные от наименьшего и поясничного внутренностного нервов. Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке. [13]
[13]
Общее правило двух нейронов для цепей СНС и ПНС имеет несколько заметных исключений. Симпатические и парасимпатические постганглионарные нейроны, которые образуют синапсы с ЭНС, функционально являются частью цепочки из трех или более нейронов. Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Постганглионарные симпатические нейроны высвобождают НЭ, который действует на адренергические рецепторы в ткани-мишени. Подтип рецептора, альфа-1, альфа-2, бета-1, бета-2 или бета-3, и ткани, в которых они экспрессируются, влияют на сродство НЭ к рецептору.[15] Для получения дополнительной информации см. статьи StatPearls, посвященные адренергическим рецепторам, по следующим ссылкам.[16][17][18]
Как уже говорилось, СНС позволяет организму справляться со стрессорами посредством реакции «бей или беги». Эта реакция в первую очередь регулирует кровеносные сосуды. Сосуды тонически иннервированы, и в большинстве случаев усиление симпатических сигналов приводит к вазоконстрикции и, противоположной вазодилатации. Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.
Эта реакция в первую очередь регулирует кровеносные сосуды. Сосуды тонически иннервированы, и в большинстве случаев усиление симпатических сигналов приводит к вазоконстрикции и, противоположной вазодилатации. Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями. [20]
[20]
СНС постоянно активна, даже в нестрессовых ситуациях. В дополнение к вышеупомянутой тонической стимуляции кровеносных сосудов, СНС активна во время нормального дыхательного цикла. Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Кроме того, СНС регулирует иммунитет посредством иннервации иммунных органов, таких как селезенка, тимус и лимфатические узлы.[15][22] Это влияние может усиливать или подавлять воспаление.[23] Клетки адаптивной иммунной системы в основном экспрессируют рецепторы бета-2, тогда как клетки врожденной иммунной системы экспрессируют их, а также адренергические рецепторы альфа-1 и альфа-2. Макрофаги активируются стимуляцией альфа-2 и подавляются активацией бета-2-адренергических рецепторов.
Большинство постганглионарных симпатических нейронов являются норадренергическими и также выделяют один или несколько пептидов, таких как нейропептид Y или соматостатин.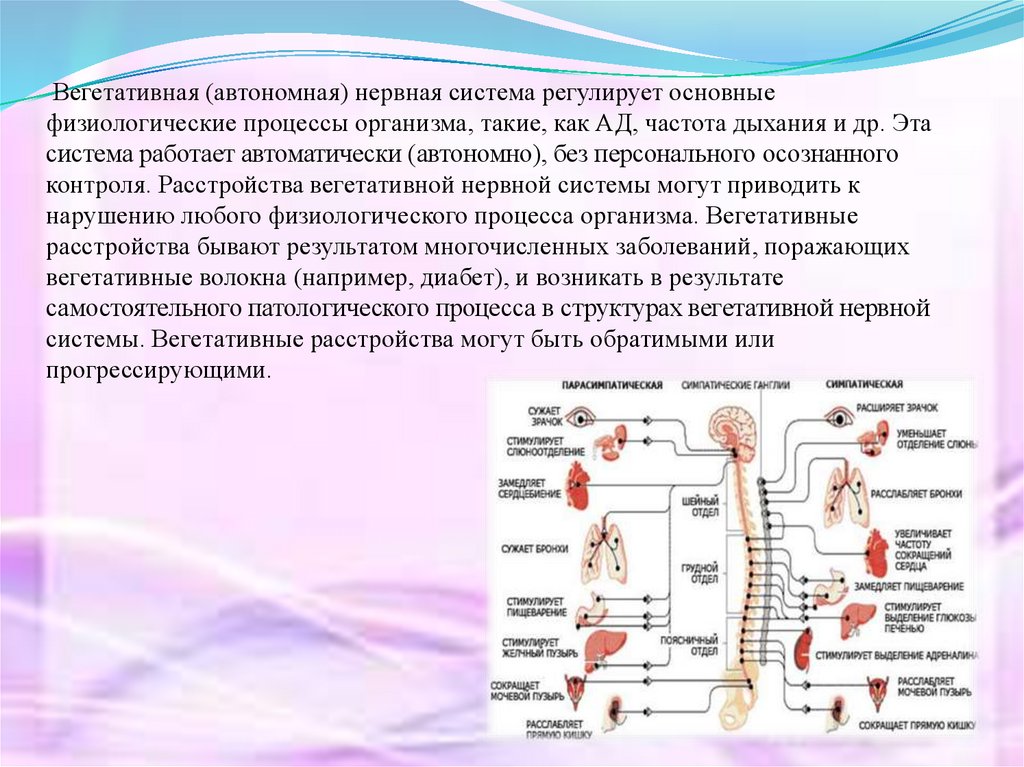 Нейроны NE/нейропептида Y иннервируют кровеносные сосуды сердца, тем самым регулируя кровоток [25], в то время как нейроны NE/соматостатина чревного и верхнего брыжеечного ганглиев иннервируют подслизистые ганглии кишечника и участвуют в контроле моторики желудочно-кишечного тракта. Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Нейроны NE/нейропептида Y иннервируют кровеносные сосуды сердца, тем самым регулируя кровоток [25], в то время как нейроны NE/соматостатина чревного и верхнего брыжеечного ганглиев иннервируют подслизистые ганглии кишечника и участвуют в контроле моторики желудочно-кишечного тракта. Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Пептиды также связаны с холинергическими симпатическими постганглионарными нейронами. Эти нейроны чаще всего иннервируют потовые железы и прекапиллярные сосуды сопротивления в скелетных мышцах и продуцируют вазоактивный интестинальный полипептид вместе с АХ. Пептид, родственный гену кальцитонина, обладающий мощным сосудорасширяющим действием, также был обнаружен в паравертебральных симпатических нейронах.
Парасимпатическая нервная система
Парасимпатические волокна выходят из ЦНС через черепно-мозговые нервы (ЧН) III, VII, IX и X, а также через нервные корешки S2-4.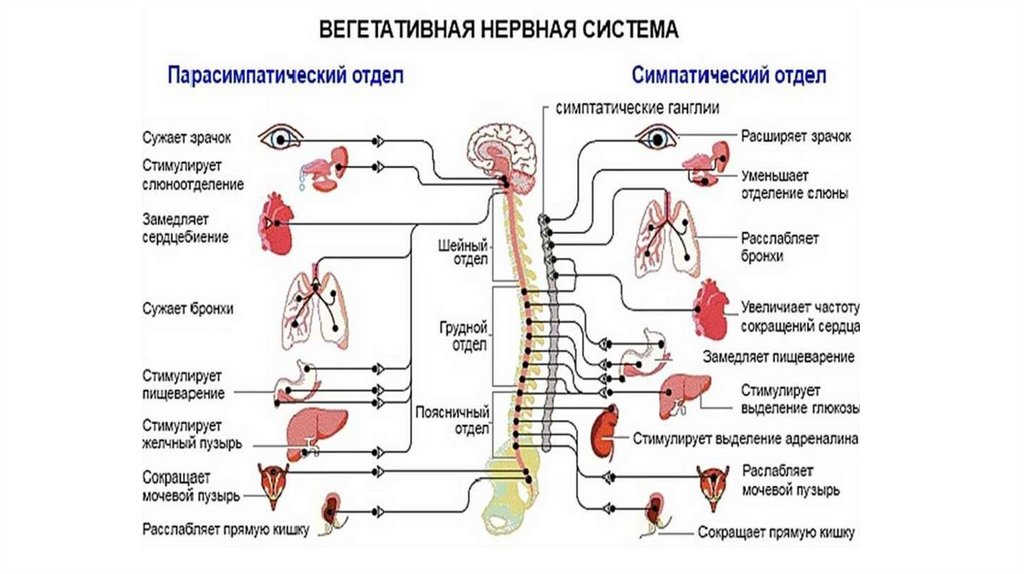 Есть четыре пары парасимпатических ганглиев, и все они расположены в голове. CN III через цилиарный ганглий иннервирует радужную оболочку и ресничные мышцы глаза. CN VII иннервирует слезные, носовые, небные и глоточные железы через крылонебный ганглий, а также подъязычную и поднижнечелюстную железы через поднижнечелюстной ганглий. CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
Есть четыре пары парасимпатических ганглиев, и все они расположены в голове. CN III через цилиарный ганглий иннервирует радужную оболочку и ресничные мышцы глаза. CN VII иннервирует слезные, носовые, небные и глоточные железы через крылонебный ганглий, а также подъязычную и поднижнечелюстную железы через поднижнечелюстной ганглий. CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
Дорсальное ядро: обеспечивает парасимпатический выход к внутренним органам
Спинальное ядро тройничного нерва: получает информацию о прикосновении, боли и температуре наружного уха, слизистой оболочки гортани и части твердой мозговой оболочки
Кроме того, блуждающий нерв проводит сенсорную информацию от барорецепторов каротидного синуса и дуги аорты к мозговому веществу. [32]
[32]
Как упоминалось во введении, блуждающий нерв отвечает за процессы «отдыха и переваривания». Блуждающий нерв способствует сердечной релаксации в нескольких аспектах функции. Он снижает сократительную способность предсердий и в меньшей степени желудочков. Прежде всего, он снижает скорость проведения через атриовентрикулярный узел. Именно благодаря этому механизму массаж каротидного синуса ограничивает повторный вход при синдроме Вольфа-Паркинсона-Уайта.[2] Другая ключевая функция ПНС связана с пищеварением. Парасимпатические волокна, идущие к голове, способствуют слюноотделению, а те, которые соединяются с ЭНС, приводят к усилению перистальтической и секреторной активности.[4][33] Блуждающий нерв также оказывает значительное влияние на дыхательный цикл. В непатологическом состоянии парасимпатические нервы возбуждаются во время выдоха, сокращая и напрягая дыхательные пути, чтобы предотвратить коллапс. Эта функция связана с ПНС в возникновении послеоперационного острого респираторного дистресс-синдрома. [2][21]
[2][21]
Из-за широкой природы блуждающего нерва он был описан как идеальная «система раннего предупреждения» для чужеродных захватчиков, а также для наблюдения за восстановлением организма. До 80% волокон блуждающего нерва являются чувствительными и иннервируют почти все основные органы. Было обнаружено, что парасимпатические ганглии экспрессируют рецепторы интерлейкина-1, ключевого цитокина в воспалительном иммунном ответе.[34] Это, в свою очередь, активирует гипоталамо-гипофизарно-надпочечниковую ось и СНС, что приводит к высвобождению глюкокортикоидов и НЭ соответственно.[2] Исследования коррелируют ингибирование действия блуждающего нерва посредством ваготомии и холинергических ингибиторов со значительно сниженными, если не полностью устраненными, аллергическими, астматическими и воспалительными реакциями.[7]
Постганглионарные парасимпатические нейроны высвобождают АХ, который действует на мускариновые и никотиновые рецепторы, каждый из которых имеет различные субъединицы: M1, M2 и M3, а также N1 и N2, где «M» и «N» обозначают мускарин и никотин соответственно. [5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
[5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
Кишечная нервная система (ENS)
ЭНС состоит из двух ганглиозных сплетений: мышечно-кишечного (Ауэрбаха) и подслизистого (Мейснера). Межмышечное сплетение находится между продольной и круговой гладкой мускулатурой желудочно-кишечного тракта, а подслизистое сплетение находится в подслизистой оболочке. ЭНС самодостаточна, функционирует за счет локальной рефлекторной активности, но часто получает информацию от СНС и ПНС и обеспечивает обратную связь с ними. ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
Подслизистое сплетение регулирует движение воды и электролитов через стенку кишечника, в то время как мышечно-кишечное сплетение координирует сократительную способность циркулярных и продольных мышечных клеток кишечника для обеспечения перистальтики.[39]
Подвижность в ЭНС обеспечивается рефлекторной цепью, включающей круговые и продольные мышцы. Никотиновые синапсы между интернейронами опосредуют рефлекторные цепи.[39] Когда цепь активируется присутствием болюса, возбуждающие нейроны в круговой мышце и тормозные нейроны в продольной мышце возбуждаются, создавая узкий участок кишечника проксимальнее болюса; это известно как пропульсивный сегмент. Одновременно возбуждающие нейроны в продольных мышцах и тормозные нейроны в круговых мышцах возбуждают «воспринимающий сегмент» кишечника, в котором будет продолжаться болюс. Этот процесс повторяется с каждым последующим отделом кишечника.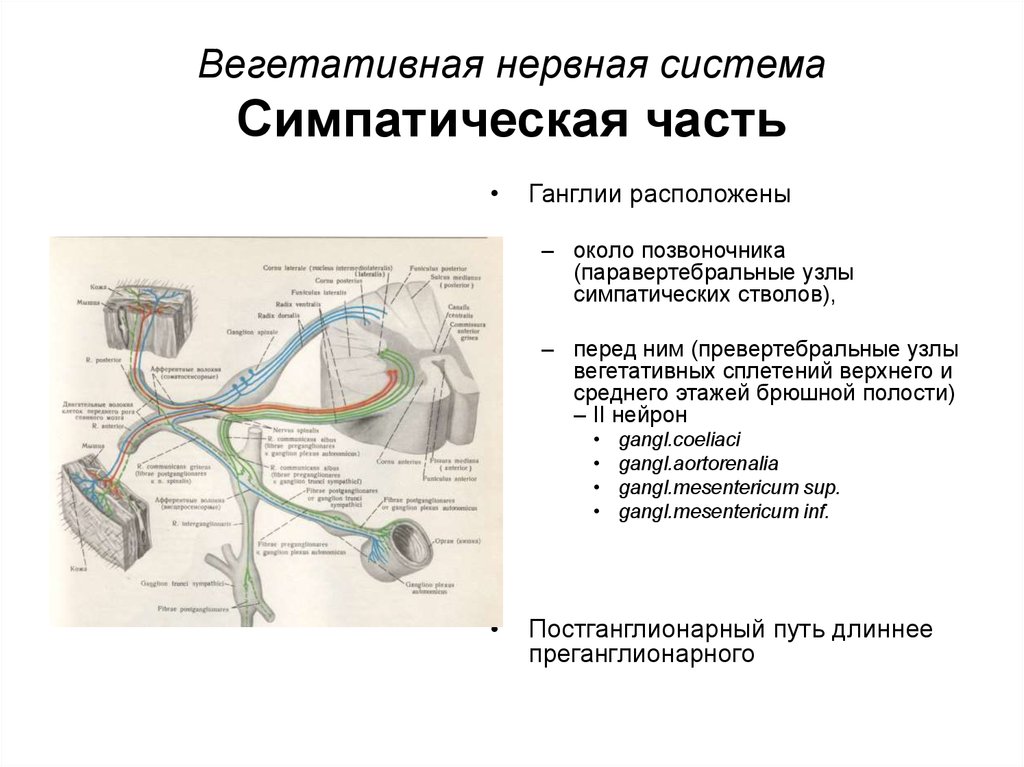 [40]
[40]
ENS имеет некоторые сходства с CNS. Как и в ЦНС, кишечные нейроны могут быть биполярными, псевдоуниполярными и мультиполярными, между которыми осуществляется нейромодуляция посредством возбуждающей и тормозной связи.[1] Точно так же нейроны ЭНС используют более 30 нейротрансмиттеров, которые аналогичны нейротрансмиттерам ЦНС, причем наиболее распространенными являются холинергические и нитрергические передатчики.
Хотя большая часть этого обсуждения была сосредоточена на эфферентных функциях ВНС, афферентные волокна отвечают за многочисленные рефлекторные действия, которые регулируют все, от частоты сердечных сокращений до иммунной системы. Обратная связь от ВНС обычно обрабатывается на подсознательном уровне для создания рефлекторных действий в висцеральных или соматических частях тела. Сознательное ощущение во внутренних органах часто интерпретируется как разлитая боль или спазмы, которые могут коррелировать с чувством голода, полноты или тошноты. Эти ощущения чаще всего возникают в результате внезапного растяжения/сокращения, химических раздражителей или патологических состояний, таких как ишемия. [41]
[41]
Эмбриология
Периферическая нервная система происходит из клеток нервного гребня. Нервный гребень аксиально делится на краниальные, блуждающие, туловищные и пояснично-крестцовые клетки нервного гребня. Клетки ствола нервного гребня вносят вклад в дорсальные корешки спинного мозга и симпатические ганглии. Парасимпатическая иннервация сердца формируется из блуждающего нервного гребня. Было показано, что большая часть парасимпатической нервной системы, включая все ганглии головы, возникает из глиальных клеток, а не из клеток нервного гребня.[42][43]
ЭНС происходит из блуждающего нервного гребня с клетками, которые мигрируют рострально-каудально через кишечную стенку, образуя сеть глии и нейронов различных подтипов. Клетки ЭНС завершают свою миграцию к 4-7 неделям развития и экспрессируют все разновидности нейротрансмиттеров ЭНС к 24-й неделе беременности. Однако моторика зрелого кишечника не реализуется, по крайней мере, до поздних сроков беременности или вскоре после рождения.
Хирургические аспекты
Синдром Горнера — это мягкое, редкое состояние, часто проявляющееся односторонним птозом, суженным, но реактивным зрачком и лицевым ангидрозом, вторичным по отношению к повреждению симпатического нерва в окулосимпатическом пути.[46] Это повреждение может иметь центральную причину, такую как инфаркт латерального продолговатого мозга, или периферическую, такую как повреждение, вторичное по отношению к торакальной хирургии или частичной/тотальной резекции щитовидной железы.[46][47] Более централизованные поражения, как правило, коррелируют с комплексом симптомов, включающим синдром Горнера.[46] Для получения дополнительной информации см. соответствующие статьи StatPearls здесь.[48][49]]
Гипергидроз — распространенное заболевание, характеризующееся повышенной потливостью, преимущественно лица, ладоней, подошв и/или подмышечных впадин. Хотя причина первичного гипергидроза до конца не выяснена, его связывают с повышенной холинергической стимуляцией. Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Клиническое значение
Из-за экстенсивного характера вегетативной нервной системы на нее может влиять широкий спектр состояний. Некоторые из них включают[53][54][55]
Унаследованные
Приобретен
Диабет-сахарный0003
Инфекции: ботулизм, болезнь Шагаса, ВИЧ, проказа, болезнь Лайма, столбняка
Аутоиммунный: Гийен-Барре, Ламберт-Этотонский миастеник-синдром 900.
 0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами ЛевиНеоплазия: опухоли головного мозга, паранеопластические синдромы
Аналогичным образом вегетативная невропатия может проявляться почти в любой системе. Ортостатическая гипотензия является наиболее распространенной вегетативной дизавтономией, но могут присутствовать и многие другие, менее изученные симптомы [53] 9.0003
Сердечно-сосудистые
Желудочно-кишечные
Дисфагия
Запоры
7 Тошнота, рвота, полноту брюшной полости
Genitourinary
PUPDDER ATONONY
9967
PUPLDER ATONONY
PUPLDER ATONONY
79967PUPLDER ATONONY
7067PUPLDER
9.
PUPLDER
.0003
Decreased pupil size
Sexual
Erectile dysfunction
Retrograde ejaculation
Sudomotor
Anhidrosis
Gustatory sweating
Вазомоторный
Похолодание конечностей (из-за потери вазомоторных реакций)
Отек (из-за потери вазомоторного тонуса и повышения проницаемости сосудов)
Наиболее распространенными симптомами ортостатической гипотензии являются головокружение, туннельное зрение и дискомфорт в голове, шее или груди. Она может проявляться одновременно с артериальной гипертензией в положении лежа из-за повышенного периферического сопротивления, что вызывает натрийурез, усугубляющий ортостатическую гипотензию. Существует множество других, более мягких стимулов, которые могут либо снижать артериальное давление (стоя, еда, Вальсальва, обезвоживание, физические упражнения, гипервентиляция и т.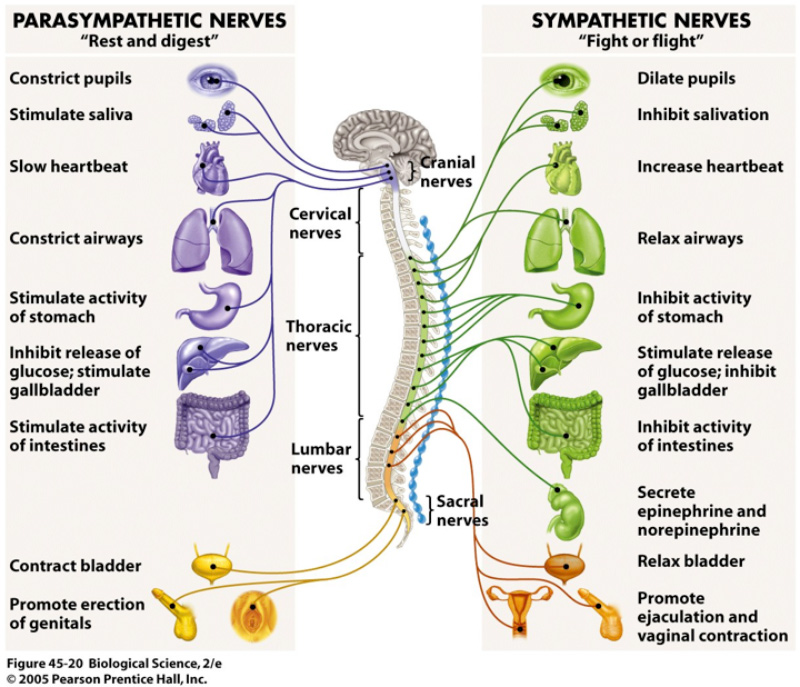 д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
Оценку ортостатической гипотензии обычно проводят с помощью ортостатического тестирования путем повторного измерения артериального давления и частоты сердечных сокращений в положении лежа и стоя, а также с помощью теста с наклонным столом. Однако преимущество этого последнего теста минимально по сравнению с ортостатическим тестом, при этом основным преимуществом является безопасность и удобство для пациента.
Пациенты с дизавтономией склонны к гипотонии во время анестезии[56]. Эту проблему можно надлежащим образом решить с помощью низких доз фенилэфрина, агониста альфа-1. Точно так же гипертонию в положении лежа можно контролировать с помощью трансдермальных или внутривенных нитратов. [53, 57, 58].
Известно, что симпатическая нервная система играет роль в ноцицепции. Есть предположения, что ВНС оказывает регуляторно-тормозное влияние на боль, утрата которого создает цепь положительной обратной связи, приводящую к гипервозбудимости ноцицептивных нервных волокон. Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Большинство состояний, связанных с ЭНС, имеют врожденное происхождение и проявляются в раннем детстве.[44] Энтеральные нейроны расслабляют гладкую мускулатуру кишечника. Их отсутствие приводит к тоническому сокращению кишечника, что приводит к непроходимости кишечника. К предъявляемым жалобам часто относятся гастроэзофагеальный рефлюкс, диспептические синдромы, запоры, хронические боли в животе, синдром раздраженного кишечника.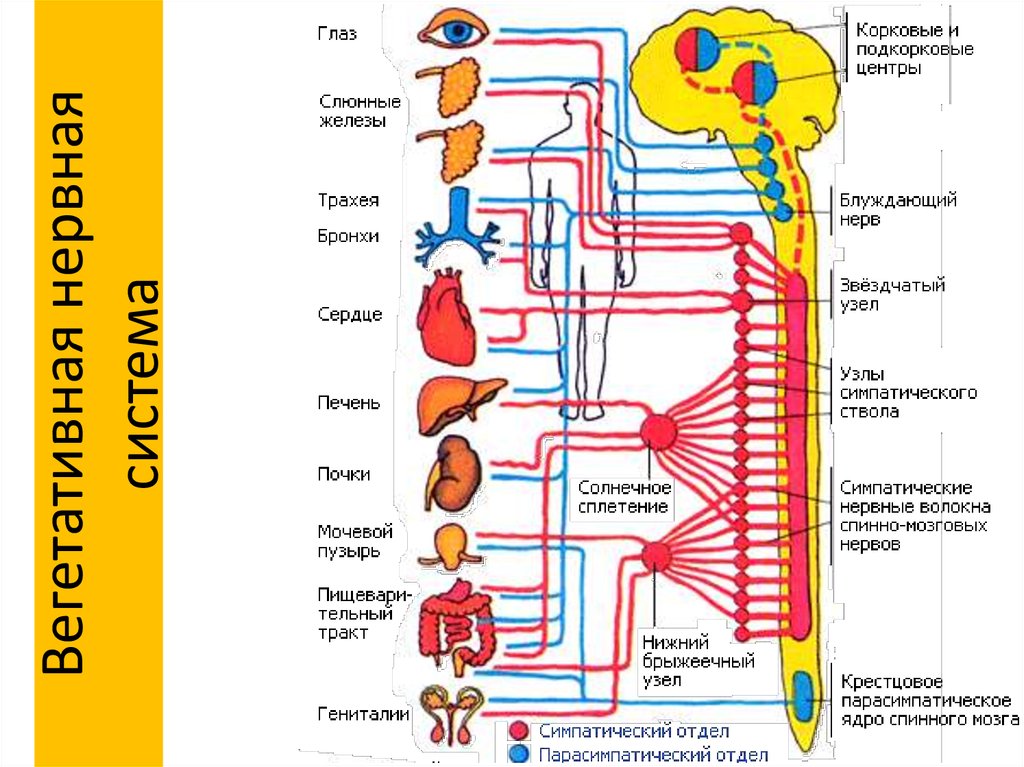 Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Схема вегетативной нервной системы. Предоставлено Генри Греем (1918 г.): Анатомия человеческого тела
Ссылки
- 1.

Стернини С. Организация периферической нервной системы: вегетативные и сенсорные ганглии. J Investig Dermatol Symp Proc. 1997 авг.; 2(1):1–7. [PubMed: 9487007]
- 2.
Каремакер Дж.М. Введение в вегетативную нервную функцию. Физиол Изм. 2017 Май; 38 (5): R89-R118. [PubMed: 28304283]
- 3.
Lake JI, Heuckeroth RO. Развитие энтеральной нервной системы: миграция, дифференцировка и заболевание. Am J Physiol Gastrointest Liver Physiol. 01 июля 2013 г.; 305(1):G1-24. [Бесплатная статья PMC: PMC3725693] [PubMed: 23639815]
- 4.
Siéssere S, Vitti M, Sousa LG, Semprini M, Iyomasa MM, Regalo SC. Анатомическая вариация краниальных парасимпатических ганглиев. Браз Орал Рез. 2008 г., апрель-июнь; 22(2):101-5. [В паблике: 18622477]
- 5.
Купман Ф.А., Стооф С.П., Штрауб Р.Х., Ван Маанен М.А., Верворделдонк М.Дж., Так Р.П. Восстановление баланса вегетативной нервной системы как инновационный подход к лечению ревматоидного артрита.
 Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]
Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]- 6.
Kenney MJ, Ganta CK. Взаимодействие вегетативной нервной системы и иммунной системы. сост. физиол. 2014 июль;4(3):1177-200. [Бесплатная статья PMC: PMC4374437] [PubMed: 24944034]
- 7.
Скотт Г.Д., Фрайер А.Д. Роль парасимпатических нервов и мускариновых рецепторов при аллергии и астме. Хим Иммунол Аллергия. 2012;98:48-69. [Бесплатная статья PMC: PMC4039300] [PubMed: 22767057]
- 8.
McConalogue K, Furness JB. Нейротрансмиттеры желудочно-кишечного тракта. Baillieres Clin Endocrinol Metab. 1994 г., январь; 8 (1): 51–76. [PubMed: 7
3]
- 9.
Шихан Д., Пик Дж. Соединительные ветви у макак-резусов. Дж Анат. 1943 января; 77 (часть 2): 125–39. [PMC бесплатная статья: PMC1252749] [PubMed: 17104919]
- 10.
Лукас М., Клаассен З., Мербс В., Таббс Р.С., Гелецкий Дж.
 , Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]
, Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]- 11.
Ян Х.Дж., Гил Ю.К., Ли В.Дж., Ким Т.Дж., Ли Х.И. Анатомия грудных внутренностных нервов для хирургической резекции. Клин Анат. 2008 март; 21(2):171-7. [PubMed: 18288763]
- 12.
Беверидж Т.С., Джонсон М., Пауэр А, Пауэр Н.Е., Оллман Б.Л. Анатомия нервов и ганглиев аортального сплетения у мужчин. Дж Анат. 2015 Январь; 226 (1): 93-103. [Бесплатная статья PMC: PMC4313893] [PubMed: 25382240]
- 13.
Ehrhardt JD, Weber C, Lopez-Ojeda W. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Анатомия, грудная клетка, большие внутренностные нервы. [PubMed: 29763202]
- 14.
Бриндли Р.Л., Бауэр М.Б., Блейкли Р.Д., Карри КПМ. Серотонин и переносчики серотонина в мозговом веществе надпочечников: потенциальный узел для модуляции симпатической реакции на стресс.
 ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]
ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]- 15.
Нэнси Д.М., Сандерс В.М. Вегетативная иннервация и регуляция иммунной системы (1987-2007 гг.). Мозг Behav Immun. 2007 авг; 21 (6): 736-45. [Бесплатная статья PMC: PMC1986730] [PubMed: 17467231]
- 16.
Alhayek S, Preuss CV. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Рецепторы бета-1. [PubMed: 30422499]
- 17.
Фарзам К., Кидрон А., Лахкар А.Д. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 18 июля 2021 г. Адренергические препараты. [PubMed: 30480963]
- 18.
Халид М.М., Галуска М.А., Гамильтон Р.Дж. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 26 июля 2021 г. Токсичность бета-блокаторов. [В паблике: 28846217]
- 19.
Хойш Г., Темер В. [Значение симпатической нервной системы для коронарного кровообращения].
 З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]
З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]- 20.
Варгас Пелаес А.Ф., Гао З., Ахмад Т.А., Лойенбергер Ю.А., Проктор Д.Н., Маман С.Р., Мюллер М.Д. Влияние адреномиметиков на коронарный кровоток: лабораторное исследование на здоровых добровольцах. Physiol Rep. 2016 May;4(10) [бесплатная статья PMC: PMC4886172] [PubMed: 27225628]
- 21.
Chen IC, Kuo J, Ko WJ, Shih HC, Kuo CD. Повышенное сопротивление потоку и снижение скорости потока у пациентов с острым респираторным дистресс-синдромом: роль вегетативной нервной модуляции. J Chin Med Assoc. 2016 Январь; 79(1):17-24. [PubMed: 26589196]
- 22.
Штернберг Э.М. Нейронная регуляция врожденного иммунитета: скоординированный неспецифический ответ хозяина на патогены. Нат Рев Иммунол. 2006 апр; 6 (4): 318-28. [Бесплатная статья PMC: PMC1783839] [PubMed: 16557263]
- 23.
Еленков И.Ю., Уайлдер Р.Л., Хрусос Г.П., Визи Э.С. Симпатический нерв — интегративный интерфейс между двумя надсистемами: мозгом и иммунной системой.
 Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]
Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]- 24.
Bellinger DL, Millar BA, Perez S, Carter J, Wood C, ThyagaRajan S, Molinaro C, Lubahn C, Lorton D. Симпатическая модуляция иммунитета: отношение к болезни. Клеточный Иммунол. 2008 март-апрель; 252(1-2):27-56. [Бесплатная статья PMC: PMC3551630] [PubMed: 18308299]
- 25.
Лундберг Дж. М., Хёкфельт Т. Множественное сосуществование пептидов и классических передатчиков в периферических вегетативных и сенсорных нейронах — функциональные и фармакологические последствия. Прог Мозг Res. 1986;68:241-62. [PubMed: 2882554]
- 26.
Лундберг Дж.М., Хёкфельт Т., Шульцберг М., Увнес-Валленстен К., Келер С., Саид С.И. Возникновение иммунореактивности, подобной вазоактивному кишечному полипептиду (ВИП), в некоторых холинергических нейронах кошки: данные комбинированной иммуногистохимии и окрашивания ацетилхолинэстеразой. Неврология. 1979;4(11):1539-59. [PubMed: 3
]- 27.

Landis SC, Fredieu JR. Сосуществование пептида, родственного гену кальцитонина, и вазоактивного интестинального пептида в холинергической симпатической иннервации потовых желез крыс. Мозг Res. 1986 г., 02 июля; 377 (1): 177–81. [PubMed: 3524749]
- 28.
Lindh B, Lundberg JM, Hökfelt T, Elfvin LG, Fahrenkrug J, Fischer J. Сосуществование CGRP- и VIP-подобных иммунореактивностей в популяции нейронов звездчатых ганглиев кошек . Acta Physiol Scand. 1987 ноября; 131 (3): 475-6. [PubMed: 3321916]
- 29.
Brain SD, Williams TJ, Tippins JR, Morris HR, MacIntyre I. Пептид, родственный гену кальцитонина, является мощным сосудорасширяющим средством. Природа. 1985 г., 3–9 января; 313 (5997): 54–6. [PubMed: 3
4]- 30.
Berthoud HR, Neuhuber WL. Функциональная и химическая анатомия афферентной системы блуждающего нерва. Автон Нейроски. 2000 г., 20 декабря; 85 (1–3): 1–17. [PubMed: 11189015]
- 31.

Павлов В.А., Ван Х., Чура С.Дж., Фридман С.Г., Трейси К.Дж. Холинергический противовоспалительный путь: недостающее звено в нейроиммуномодуляции. Мол Мед. 2003 май-август 9(5-8):125-34. [Бесплатная статья PMC: PMC1430829] [PubMed: 14571320]
- 32.
Цучихаси К., Ёсихиро Т., Айкава Т., Нио К., Такаёси К., Ёкояма Т., Фуката М., Арита С., Арияма Х., Симидзу Й. Yoshida Y, Torisu T, Esaki M, Odashiro K, Kusaba H, Akashi K, Baba E. Метастатический рак пищевода, представляющий собой шок от повреждения блуждающего нерва, имитирующего барорецепторный рефлекс: клинический случай. Медицина (Балтимор). 2017 Декабрь;96(49):e8987. [Бесплатная статья PMC: PMC5728886] [PubMed: 271]
- 33.
Вуд JD. Применение классификационных схем к энтеральной нервной системе. J Auton Nerv Syst. 1994 г., июнь; 48 (1): 17–29. [PubMed: 8027516]
- 34.
Thayer JF, Sternberg EM. Невральные аспекты иммуномодуляции: фокус на блуждающий нерв.
 Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]
Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]- 35.
Лундберг Дж. М., Хёкфельт Т., Ангард А., Увнес-Валленстен К., Бримиджоин С., Бродин Э., Фаренкруг Дж. Периферийное распределение аксона: транспорт и некоторые аспекты возможного функционирования. Adv Biochem Psychopharmacol. 1980;22:25-36. [PubMed: 6156578]
- 36.
Leblanc GG, Trimmer BA, Landis SC. Нейропептид Y-подобная иммунореактивность в черепных парасимпатических нейронах крыс: сосуществование с вазоактивным кишечным пептидом и холин-ацетилтрансферазой. Proc Natl Acad Sci USA. 1987 May; 84(10):3511-5. [Бесплатная статья PMC: PMC304901] [PubMed: 3554241]
- 37.
Carlson AB, Kraus GP. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 23 августа 2021 г. Физиология, холинергические рецепторы. [В паблике: 30252390]
- 38.
Миллион М, Ларош М. Стресс, секс и кишечная нервная система.
 Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]
Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]- 39.
Хансен МБ. Энтеральная нервная система I: организация и классификация. Фармакол Токсикол. 2003 март; 92(3):105-13. [PubMed: 12753424]
- 40.
Вуд JD. Энтеральная нервная система: нейропатическая моторика желудочно-кишечного тракта. Dig Dis Sci. 2016 июль; 61 (7): 1803-16. [В паблике: 27142673]
- 41.
Сарна SK. Подвижность толстой кишки: от скамейки к постели. Морган и Клейпул Лайф Сайенсиз; Сан-Рафаэль (Калифорния): 2010. [PubMed: 21452445]
- 42.
Батлер С.Дж., Броннер М.Э. От классики к современности: анализ происхождения и судьбы периферической нервной системы и спинного мозга. Дев биол. 2015 15 февраля; 398 (2): 135-46. [Бесплатная статья PMC: PMC4845735] [PubMed: 25446276]
- 43.
Дьячук В., Фурлан А., Шахиди М.К., Джовенко М., Каукуа Н.
 , Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]
, Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]- 44.
Gariepy CE. Нарушения моторики кишечника и развитие энтеральной нервной системы. Педиатр рез. 2001 г., май; 49(5):605-13. [PubMed: 11328941]
- 45.
Сасселли В., Пахнис В., Бернс А.Дж. Энтеральная нервная система. Дев биол. 01 июня 2012 г .; 366 (1): 64–73. [PubMed: 222
]- 46.
Канагалингам С., Миллер Н.Р. Синдром Горнера: клинические перспективы. Глазной мозг. 2015;7:35-46. [Бесплатная статья PMC: PMC5398733] [PubMed: 28539793]
- 47.
Diamantis E, Farmaki P, Savvanis S, Athanasiadis G, Troupis T, Damaskos C. Повреждение симпатического нерва при раке щитовидной железы. Acta Medica (Градец Кралове).
 2017;60(4):135-139. [PubMed: 29716678]
2017;60(4):135-139. [PubMed: 29716678]- 48.
Хан З., Боллу ПК. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 4 мая 2021 г. Синдром Хорнера. [PubMed: 29763176]
- 49.
Lykstad J, Reddy V, Hanna A. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, путь расширения зрачков. [В паблике: 30571042]
- 50.
Делорт С., Марчи Э., Корреа М.А. Оксибутинин как альтернативное лечение гипергидроза. Бюстгальтеры Дерматол. 2017 март-апрель;92(2):217-220. [Бесплатная статья PMC: PMC5429108] [PubMed: 28538882]
- 51.
del Boz J. Системное лечение гипергидроза. Actas Дермосифилиогр. 2015 май; 106(4):271-7. [PubMed: 25638324]
- 52.
Haam SJ, Park SY, Paik HC, Lee DY. Реконструкция симпатического нерва при компенсаторном гипергидрозе после симпатической операции по поводу первичного гипергидроза.
 J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]
J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]- 53.
Mustafa HI, Fessel JP, Barwise J, Shannon JR, Raj SR, Diedrich A, Biaggioni I, Robertson D. Dysautonomia: периоперационные последствия. Анестезиология. 2012 Январь; 116 (1): 205-15. [Бесплатная статья PMC: PMC3296831] [PubMed: 22143168]
- 54.
McLeod JG. Исследование периферической нейропатии. J Neurol Нейрохирург Психиатрия. 1995 март; 58(3):274-83. [Бесплатная статья PMC: PMC1073360] [PubMed: 7897405]
- 55.
Ludwig PE, Reddy V, Varacallo M. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, центральная нервная система (ЦНС) [PubMed: 28723039]
- 56.
Санчес-Мансо Дж. К., Гуджарати Р., Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 октября 2021 г. Вегетативная дисфункция. [PubMed: 28613638]
- 57.

Беван Д.Р. Синдром Шай-Дрейгера. Обзор и описание анестезиологического обеспечения. Анестезия. 1979 октября; 34 (9): 866-73. [PubMed: 532923]
- 58.
Stirt JA, Frantz RA, Gunz EF, Conolly ME. Анестезия, катехоламины и гемодинамика при вегетативной дисфункции. Анест Анальг. 1982 г., август; 61 (8): 701-4. [PubMed: 7201274]
- 59.
Gunduz OH, Kenis-Coskun O. Блокада ганглиев как лечение боли: текущие перспективы. Джей Боль Рез. 2017;10:2815-2826. [Бесплатная статья PMC: PMC5734237] [PubMed: 2
02]
- 60.
Джон Р.С., Диксон Б., Шиенбаум Р. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 31 июля 2021 г. Блокада чревного сплетения. [PubMed: 30285364]
- 61.
Пираччини Э., Мунакоми С., Чанг К.В. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 августа 2021 г. Блоки звездчатого ганглия. [PubMed: 29939575]
- 62.

Александр К.Э., Де Хесус О, Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 30 августа 2021 г. Симпатическая блокада поясничного отдела. [В паблике: 28613759]
Copyright © 2022, StatPearls Publishing LLC.
Эта книга распространяется в соответствии с международной лицензией Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает использование, дублирование, адаптацию, распространение и воспроизведение на любом носителе или формате, при условии, что вы укажете автора(ов) оригинала и источник, будет дана ссылка на лицензию Creative Commons и указаны любые внесенные изменения.
ID книжной полки: NBK539845PMID: 30969667
Анатомия, вегетативная нервная система — StatPearls
Книжная полка NCBI. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2022 янв.
StatPearls [Интернет].
Показать подробности
Критерий поиска
Джошуа А. Ваксенбаум; Вамси Редди; Мэтью Варакалло.
Информация об авторе
Последнее обновление: 29 июля 2021 г.
Введение
Вегетативная нервная система — это компонент периферической нервной системы, который регулирует непроизвольные физиологические процессы, включая частоту сердечных сокращений, кровяное давление, дыхание, пищеварение и половое возбуждение. Он состоит из трех анатомически различных отделов: симпатического, парасимпатического и энтерального отделов.
Симпатическая нервная система (СНС) и парасимпатическая нервная система (ПНС) содержат как афферентные, так и эфферентные волокна, которые обеспечивают сенсорный вход и двигательный выход, соответственно, в центральную нервную систему (ЦНС). Как правило, двигательные пути СНС и ПНС состоят из серии из двух нейронов: преганглионарного нейрона с телом клетки в ЦНС и постганглионарного нейрона с телом клетки на периферии, иннервирующих ткани-мишени. Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Активация СНС приводит к состоянию общей повышенной активности и внимания: реакция «бей или беги». При этом повышается артериальное давление и частота сердечных сокращений, происходит гликогенолиз, прекращается перистальтика желудочно-кишечного тракта и т.д.[5] СНС иннервирует почти все живые ткани в организме. ПНС способствует процессам «отдыха и переваривания»; снижается частота сердечных сокращений и артериальное давление, возобновляется перистальтика желудочно-кишечного тракта / пищеварение и т. д. [5] [6] ПНС иннервирует только голову, внутренние органы и наружные гениталии, в значительной степени вакантна в большей части костно-мышечной системы и кожи, что делает ее значительно меньше, чем СНС. [7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
[7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
Пресинаптические нейроны как СНС, так и ПНС используют ацетилхолин (АХ) в качестве нейротрансмиттера. Постсинаптические симпатические нейроны обычно продуцируют норадреналин (НЭ) в качестве своего эффекторного передатчика для воздействия на ткани-мишени, в то время как постсинаптические парасимпатические нейроны повсеместно используют АХ. Известно, что энтеральные нейроны используют несколько основных нейротрансмиттеров, таких как АХ, закись азота и серотонин, и это лишь некоторые из них.[8]
Структура и функция
Симпатическая нервная система
Симпатические нейроны имеют клеточные тела, расположенные в промежуточных латеральных столбах или латеральных рогах спинного мозга. Пресинаптические волокна выходят из спинного мозга через передние корешки и входят в передние ветви спинномозговых нервов T1-L2 и в симпатические стволы через белые соединительные ветви. Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Паравертебральные ганглии существуют в виде узелков по всему симпатическому стволу, прилегающему к позвоночнику, где происходит синапс пре- и постганглионарных нейронов. Хотя количество может варьироваться в зависимости от человека, как правило, существует три шейных, 12 грудных, четыре поясничных и пять крестцовых ганглиев. Из них только шейные имеют названия верхних, средних и нижних шейных ганглиев. Нижний шейный ганглий может сливаться с первым грудным ганглием, образуя звездчатый ганглий.
Все нервы, расположенные дистальнее паравертебральных ганглиев, являются внутренностными нервами. Они передают афферентные и эфферентные волокна между ЦНС и внутренними органами. Сердечно-легочные внутренностные нервы несут постсинаптические волокна, направляющиеся в грудную полость.
Нервы, которые будут иннервировать органы брюшной полости и таза, проходят через паравертебральные нервы без образования синапсов, становясь внутрибрюшными тазовыми нервами. Эти нервы включают большой, малый, наименьший и поясничный внутренностные нервы. Пресинаптические нервы, наконец, образуют синапсы в превертебральных ганглиях, которые находятся ближе к органу-мишени. Предвертебральные ганглии входят в состав нервных сплетений, окружающих ветви аорты. К ним относятся чревный, аортокоренальный, а также верхний и нижний брыжеечные ганглии. Чревный ганглий получает вход от большого внутренностного нерва, аортокоренальный от малого и наименьшего внутренностного нерва, а верхний и нижний брыжеечные от наименьшего и поясничного внутренностного нервов. Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Общее правило двух нейронов для цепей СНС и ПНС имеет несколько заметных исключений. Симпатические и парасимпатические постганглионарные нейроны, которые образуют синапсы с ЭНС, функционально являются частью цепочки из трех или более нейронов. Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Постганглионарные симпатические нейроны высвобождают НЭ, который действует на адренергические рецепторы в ткани-мишени. Подтип рецептора, альфа-1, альфа-2, бета-1, бета-2 или бета-3, и ткани, в которых они экспрессируются, влияют на сродство НЭ к рецептору.[15] Для получения дополнительной информации см. статьи StatPearls, посвященные адренергическим рецепторам, по следующим ссылкам.[16][17][18]
Как уже говорилось, СНС позволяет организму справляться со стрессорами посредством реакции «бей или беги». Эта реакция в первую очередь регулирует кровеносные сосуды. Сосуды тонически иннервированы, и в большинстве случаев усиление симпатических сигналов приводит к вазоконстрикции и, противоположной вазодилатации. Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
СНС постоянно активна, даже в нестрессовых ситуациях. В дополнение к вышеупомянутой тонической стимуляции кровеносных сосудов, СНС активна во время нормального дыхательного цикла. Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Кроме того, СНС регулирует иммунитет посредством иннервации иммунных органов, таких как селезенка, тимус и лимфатические узлы.[15][22] Это влияние может усиливать или подавлять воспаление.[23] Клетки адаптивной иммунной системы в основном экспрессируют рецепторы бета-2, тогда как клетки врожденной иммунной системы экспрессируют их, а также адренергические рецепторы альфа-1 и альфа-2. Макрофаги активируются стимуляцией альфа-2 и подавляются активацией бета-2-адренергических рецепторов.
Большинство постганглионарных симпатических нейронов являются норадренергическими и также выделяют один или несколько пептидов, таких как нейропептид Y или соматостатин. Нейроны NE/нейропептида Y иннервируют кровеносные сосуды сердца, тем самым регулируя кровоток [25], в то время как нейроны NE/соматостатина чревного и верхнего брыжеечного ганглиев иннервируют подслизистые ганглии кишечника и участвуют в контроле моторики желудочно-кишечного тракта. Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Пептиды также связаны с холинергическими симпатическими постганглионарными нейронами. Эти нейроны чаще всего иннервируют потовые железы и прекапиллярные сосуды сопротивления в скелетных мышцах и продуцируют вазоактивный интестинальный полипептид вместе с АХ. Пептид, родственный гену кальцитонина, обладающий мощным сосудорасширяющим действием, также был обнаружен в паравертебральных симпатических нейронах.
Парасимпатическая нервная система
Парасимпатические волокна выходят из ЦНС через черепно-мозговые нервы (ЧН) III, VII, IX и X, а также через нервные корешки S2-4. Есть четыре пары парасимпатических ганглиев, и все они расположены в голове. CN III через цилиарный ганглий иннервирует радужную оболочку и ресничные мышцы глаза. CN VII иннервирует слезные, носовые, небные и глоточные железы через крылонебный ганглий, а также подъязычную и поднижнечелюстную железы через поднижнечелюстной ганглий. CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
Дорсальное ядро: обеспечивает парасимпатический выход к внутренним органам
Спинальное ядро тройничного нерва: получает информацию о прикосновении, боли и температуре наружного уха, слизистой оболочки гортани и части твердой мозговой оболочки
Кроме того, блуждающий нерв проводит сенсорную информацию от барорецепторов каротидного синуса и дуги аорты к мозговому веществу. [32]
[32]
Как упоминалось во введении, блуждающий нерв отвечает за процессы «отдыха и переваривания». Блуждающий нерв способствует сердечной релаксации в нескольких аспектах функции. Он снижает сократительную способность предсердий и в меньшей степени желудочков. Прежде всего, он снижает скорость проведения через атриовентрикулярный узел. Именно благодаря этому механизму массаж каротидного синуса ограничивает повторный вход при синдроме Вольфа-Паркинсона-Уайта.[2] Другая ключевая функция ПНС связана с пищеварением. Парасимпатические волокна, идущие к голове, способствуют слюноотделению, а те, которые соединяются с ЭНС, приводят к усилению перистальтической и секреторной активности.[4][33] Блуждающий нерв также оказывает значительное влияние на дыхательный цикл. В непатологическом состоянии парасимпатические нервы возбуждаются во время выдоха, сокращая и напрягая дыхательные пути, чтобы предотвратить коллапс. Эта функция связана с ПНС в возникновении послеоперационного острого респираторного дистресс-синдрома. [2][21]
[2][21]
Из-за широкой природы блуждающего нерва он был описан как идеальная «система раннего предупреждения» для чужеродных захватчиков, а также для наблюдения за восстановлением организма. До 80% волокон блуждающего нерва являются чувствительными и иннервируют почти все основные органы. Было обнаружено, что парасимпатические ганглии экспрессируют рецепторы интерлейкина-1, ключевого цитокина в воспалительном иммунном ответе.[34] Это, в свою очередь, активирует гипоталамо-гипофизарно-надпочечниковую ось и СНС, что приводит к высвобождению глюкокортикоидов и НЭ соответственно.[2] Исследования коррелируют ингибирование действия блуждающего нерва посредством ваготомии и холинергических ингибиторов со значительно сниженными, если не полностью устраненными, аллергическими, астматическими и воспалительными реакциями.[7]
Постганглионарные парасимпатические нейроны высвобождают АХ, который действует на мускариновые и никотиновые рецепторы, каждый из которых имеет различные субъединицы: M1, M2 и M3, а также N1 и N2, где «M» и «N» обозначают мускарин и никотин соответственно. [5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
[5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
Кишечная нервная система (ENS)
ЭНС состоит из двух ганглиозных сплетений: мышечно-кишечного (Ауэрбаха) и подслизистого (Мейснера). Межмышечное сплетение находится между продольной и круговой гладкой мускулатурой желудочно-кишечного тракта, а подслизистое сплетение находится в подслизистой оболочке. ЭНС самодостаточна, функционирует за счет локальной рефлекторной активности, но часто получает информацию от СНС и ПНС и обеспечивает обратную связь с ними. ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
Подслизистое сплетение регулирует движение воды и электролитов через стенку кишечника, в то время как мышечно-кишечное сплетение координирует сократительную способность циркулярных и продольных мышечных клеток кишечника для обеспечения перистальтики.[39]
Подвижность в ЭНС обеспечивается рефлекторной цепью, включающей круговые и продольные мышцы. Никотиновые синапсы между интернейронами опосредуют рефлекторные цепи.[39] Когда цепь активируется присутствием болюса, возбуждающие нейроны в круговой мышце и тормозные нейроны в продольной мышце возбуждаются, создавая узкий участок кишечника проксимальнее болюса; это известно как пропульсивный сегмент. Одновременно возбуждающие нейроны в продольных мышцах и тормозные нейроны в круговых мышцах возбуждают «воспринимающий сегмент» кишечника, в котором будет продолжаться болюс. Этот процесс повторяется с каждым последующим отделом кишечника. [40]
[40]
ENS имеет некоторые сходства с CNS. Как и в ЦНС, кишечные нейроны могут быть биполярными, псевдоуниполярными и мультиполярными, между которыми осуществляется нейромодуляция посредством возбуждающей и тормозной связи.[1] Точно так же нейроны ЭНС используют более 30 нейротрансмиттеров, которые аналогичны нейротрансмиттерам ЦНС, причем наиболее распространенными являются холинергические и нитрергические передатчики.
Хотя большая часть этого обсуждения была сосредоточена на эфферентных функциях ВНС, афферентные волокна отвечают за многочисленные рефлекторные действия, которые регулируют все, от частоты сердечных сокращений до иммунной системы. Обратная связь от ВНС обычно обрабатывается на подсознательном уровне для создания рефлекторных действий в висцеральных или соматических частях тела. Сознательное ощущение во внутренних органах часто интерпретируется как разлитая боль или спазмы, которые могут коррелировать с чувством голода, полноты или тошноты. Эти ощущения чаще всего возникают в результате внезапного растяжения/сокращения, химических раздражителей или патологических состояний, таких как ишемия. [41]
[41]
Эмбриология
Периферическая нервная система происходит из клеток нервного гребня. Нервный гребень аксиально делится на краниальные, блуждающие, туловищные и пояснично-крестцовые клетки нервного гребня. Клетки ствола нервного гребня вносят вклад в дорсальные корешки спинного мозга и симпатические ганглии. Парасимпатическая иннервация сердца формируется из блуждающего нервного гребня. Было показано, что большая часть парасимпатической нервной системы, включая все ганглии головы, возникает из глиальных клеток, а не из клеток нервного гребня.[42][43]
ЭНС происходит из блуждающего нервного гребня с клетками, которые мигрируют рострально-каудально через кишечную стенку, образуя сеть глии и нейронов различных подтипов. Клетки ЭНС завершают свою миграцию к 4-7 неделям развития и экспрессируют все разновидности нейротрансмиттеров ЭНС к 24-й неделе беременности. Однако моторика зрелого кишечника не реализуется, по крайней мере, до поздних сроков беременности или вскоре после рождения.
Хирургические аспекты
Синдром Горнера — это мягкое, редкое состояние, часто проявляющееся односторонним птозом, суженным, но реактивным зрачком и лицевым ангидрозом, вторичным по отношению к повреждению симпатического нерва в окулосимпатическом пути.[46] Это повреждение может иметь центральную причину, такую как инфаркт латерального продолговатого мозга, или периферическую, такую как повреждение, вторичное по отношению к торакальной хирургии или частичной/тотальной резекции щитовидной железы.[46][47] Более централизованные поражения, как правило, коррелируют с комплексом симптомов, включающим синдром Горнера.[46] Для получения дополнительной информации см. соответствующие статьи StatPearls здесь.[48][49]]
Гипергидроз — распространенное заболевание, характеризующееся повышенной потливостью, преимущественно лица, ладоней, подошв и/или подмышечных впадин. Хотя причина первичного гипергидроза до конца не выяснена, его связывают с повышенной холинергической стимуляцией. Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Клиническое значение
Из-за экстенсивного характера вегетативной нервной системы на нее может влиять широкий спектр состояний. Некоторые из них включают[53][54][55]
Унаследованные
Приобретен
Диабет-сахарный0003
Инфекции: ботулизм, болезнь Шагаса, ВИЧ, проказа, болезнь Лайма, столбняка
Аутоиммунный: Гийен-Барре, Ламберт-Этотонский миастеник-синдром 900.
 0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами ЛевиНеоплазия: опухоли головного мозга, паранеопластические синдромы
Аналогичным образом вегетативная невропатия может проявляться почти в любой системе. Ортостатическая гипотензия является наиболее распространенной вегетативной дизавтономией, но могут присутствовать и многие другие, менее изученные симптомы [53] 9.0003
Сердечно-сосудистые
Желудочно-кишечные
Дисфагия
Запоры
7 Тошнота, рвота, полноту брюшной полости
Genitourinary
PUPDDER ATONONY
9967
PUPLDER ATONONY
PUPLDER ATONONY
79967PUPLDER ATONONY
7067PUPLDER
9.
PUPLDER
.0003
Decreased pupil size
Sexual
Erectile dysfunction
Retrograde ejaculation
Sudomotor
Anhidrosis
Gustatory sweating
Вазомоторный
Похолодание конечностей (из-за потери вазомоторных реакций)
Отек (из-за потери вазомоторного тонуса и повышения проницаемости сосудов)
Наиболее распространенными симптомами ортостатической гипотензии являются головокружение, туннельное зрение и дискомфорт в голове, шее или груди. Она может проявляться одновременно с артериальной гипертензией в положении лежа из-за повышенного периферического сопротивления, что вызывает натрийурез, усугубляющий ортостатическую гипотензию. Существует множество других, более мягких стимулов, которые могут либо снижать артериальное давление (стоя, еда, Вальсальва, обезвоживание, физические упражнения, гипервентиляция и т. д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
Оценку ортостатической гипотензии обычно проводят с помощью ортостатического тестирования путем повторного измерения артериального давления и частоты сердечных сокращений в положении лежа и стоя, а также с помощью теста с наклонным столом. Однако преимущество этого последнего теста минимально по сравнению с ортостатическим тестом, при этом основным преимуществом является безопасность и удобство для пациента.
Пациенты с дизавтономией склонны к гипотонии во время анестезии[56]. Эту проблему можно надлежащим образом решить с помощью низких доз фенилэфрина, агониста альфа-1. Точно так же гипертонию в положении лежа можно контролировать с помощью трансдермальных или внутривенных нитратов. [53, 57, 58].
Известно, что симпатическая нервная система играет роль в ноцицепции. Есть предположения, что ВНС оказывает регуляторно-тормозное влияние на боль, утрата которого создает цепь положительной обратной связи, приводящую к гипервозбудимости ноцицептивных нервных волокон. Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Большинство состояний, связанных с ЭНС, имеют врожденное происхождение и проявляются в раннем детстве.[44] Энтеральные нейроны расслабляют гладкую мускулатуру кишечника. Их отсутствие приводит к тоническому сокращению кишечника, что приводит к непроходимости кишечника. К предъявляемым жалобам часто относятся гастроэзофагеальный рефлюкс, диспептические синдромы, запоры, хронические боли в животе, синдром раздраженного кишечника. Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Схема вегетативной нервной системы. Предоставлено Генри Греем (1918 г.): Анатомия человеческого тела
Ссылки
- 1.

Стернини С. Организация периферической нервной системы: вегетативные и сенсорные ганглии. J Investig Dermatol Symp Proc. 1997 авг.; 2(1):1–7. [PubMed: 9487007]
- 2.
Каремакер Дж.М. Введение в вегетативную нервную функцию. Физиол Изм. 2017 Май; 38 (5): R89-R118. [PubMed: 28304283]
- 3.
Lake JI, Heuckeroth RO. Развитие энтеральной нервной системы: миграция, дифференцировка и заболевание. Am J Physiol Gastrointest Liver Physiol. 01 июля 2013 г.; 305(1):G1-24. [Бесплатная статья PMC: PMC3725693] [PubMed: 23639815]
- 4.
Siéssere S, Vitti M, Sousa LG, Semprini M, Iyomasa MM, Regalo SC. Анатомическая вариация краниальных парасимпатических ганглиев. Браз Орал Рез. 2008 г., апрель-июнь; 22(2):101-5. [В паблике: 18622477]
- 5.
Купман Ф.А., Стооф С.П., Штрауб Р.Х., Ван Маанен М.А., Верворделдонк М.Дж., Так Р.П. Восстановление баланса вегетативной нервной системы как инновационный подход к лечению ревматоидного артрита.
 Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]
Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]- 6.
Kenney MJ, Ganta CK. Взаимодействие вегетативной нервной системы и иммунной системы. сост. физиол. 2014 июль;4(3):1177-200. [Бесплатная статья PMC: PMC4374437] [PubMed: 24944034]
- 7.
Скотт Г.Д., Фрайер А.Д. Роль парасимпатических нервов и мускариновых рецепторов при аллергии и астме. Хим Иммунол Аллергия. 2012;98:48-69. [Бесплатная статья PMC: PMC4039300] [PubMed: 22767057]
- 8.
McConalogue K, Furness JB. Нейротрансмиттеры желудочно-кишечного тракта. Baillieres Clin Endocrinol Metab. 1994 г., январь; 8 (1): 51–76. [PubMed: 7
3]
- 9.
Шихан Д., Пик Дж. Соединительные ветви у макак-резусов. Дж Анат. 1943 января; 77 (часть 2): 125–39. [PMC бесплатная статья: PMC1252749] [PubMed: 17104919]
- 10.
Лукас М., Клаассен З., Мербс В., Таббс Р.С., Гелецкий Дж.
 , Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]
, Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]- 11.
Ян Х.Дж., Гил Ю.К., Ли В.Дж., Ким Т.Дж., Ли Х.И. Анатомия грудных внутренностных нервов для хирургической резекции. Клин Анат. 2008 март; 21(2):171-7. [PubMed: 18288763]
- 12.
Беверидж Т.С., Джонсон М., Пауэр А, Пауэр Н.Е., Оллман Б.Л. Анатомия нервов и ганглиев аортального сплетения у мужчин. Дж Анат. 2015 Январь; 226 (1): 93-103. [Бесплатная статья PMC: PMC4313893] [PubMed: 25382240]
- 13.
Ehrhardt JD, Weber C, Lopez-Ojeda W. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Анатомия, грудная клетка, большие внутренностные нервы. [PubMed: 29763202]
- 14.
Бриндли Р.Л., Бауэр М.Б., Блейкли Р.Д., Карри КПМ. Серотонин и переносчики серотонина в мозговом веществе надпочечников: потенциальный узел для модуляции симпатической реакции на стресс.
 ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]
ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]- 15.
Нэнси Д.М., Сандерс В.М. Вегетативная иннервация и регуляция иммунной системы (1987-2007 гг.). Мозг Behav Immun. 2007 авг; 21 (6): 736-45. [Бесплатная статья PMC: PMC1986730] [PubMed: 17467231]
- 16.
Alhayek S, Preuss CV. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Рецепторы бета-1. [PubMed: 30422499]
- 17.
Фарзам К., Кидрон А., Лахкар А.Д. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 18 июля 2021 г. Адренергические препараты. [PubMed: 30480963]
- 18.
Халид М.М., Галуска М.А., Гамильтон Р.Дж. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 26 июля 2021 г. Токсичность бета-блокаторов. [В паблике: 28846217]
- 19.
Хойш Г., Темер В. [Значение симпатической нервной системы для коронарного кровообращения].
 З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]
З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]- 20.
Варгас Пелаес А.Ф., Гао З., Ахмад Т.А., Лойенбергер Ю.А., Проктор Д.Н., Маман С.Р., Мюллер М.Д. Влияние адреномиметиков на коронарный кровоток: лабораторное исследование на здоровых добровольцах. Physiol Rep. 2016 May;4(10) [бесплатная статья PMC: PMC4886172] [PubMed: 27225628]
- 21.
Chen IC, Kuo J, Ko WJ, Shih HC, Kuo CD. Повышенное сопротивление потоку и снижение скорости потока у пациентов с острым респираторным дистресс-синдромом: роль вегетативной нервной модуляции. J Chin Med Assoc. 2016 Январь; 79(1):17-24. [PubMed: 26589196]
- 22.
Штернберг Э.М. Нейронная регуляция врожденного иммунитета: скоординированный неспецифический ответ хозяина на патогены. Нат Рев Иммунол. 2006 апр; 6 (4): 318-28. [Бесплатная статья PMC: PMC1783839] [PubMed: 16557263]
- 23.
Еленков И.Ю., Уайлдер Р.Л., Хрусос Г.П., Визи Э.С. Симпатический нерв — интегративный интерфейс между двумя надсистемами: мозгом и иммунной системой.
 Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]
Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]- 24.
Bellinger DL, Millar BA, Perez S, Carter J, Wood C, ThyagaRajan S, Molinaro C, Lubahn C, Lorton D. Симпатическая модуляция иммунитета: отношение к болезни. Клеточный Иммунол. 2008 март-апрель; 252(1-2):27-56. [Бесплатная статья PMC: PMC3551630] [PubMed: 18308299]
- 25.
Лундберг Дж. М., Хёкфельт Т. Множественное сосуществование пептидов и классических передатчиков в периферических вегетативных и сенсорных нейронах — функциональные и фармакологические последствия. Прог Мозг Res. 1986;68:241-62. [PubMed: 2882554]
- 26.
Лундберг Дж.М., Хёкфельт Т., Шульцберг М., Увнес-Валленстен К., Келер С., Саид С.И. Возникновение иммунореактивности, подобной вазоактивному кишечному полипептиду (ВИП), в некоторых холинергических нейронах кошки: данные комбинированной иммуногистохимии и окрашивания ацетилхолинэстеразой. Неврология. 1979;4(11):1539-59. [PubMed: 3
]- 27.

Landis SC, Fredieu JR. Сосуществование пептида, родственного гену кальцитонина, и вазоактивного интестинального пептида в холинергической симпатической иннервации потовых желез крыс. Мозг Res. 1986 г., 02 июля; 377 (1): 177–81. [PubMed: 3524749]
- 28.
Lindh B, Lundberg JM, Hökfelt T, Elfvin LG, Fahrenkrug J, Fischer J. Сосуществование CGRP- и VIP-подобных иммунореактивностей в популяции нейронов звездчатых ганглиев кошек . Acta Physiol Scand. 1987 ноября; 131 (3): 475-6. [PubMed: 3321916]
- 29.
Brain SD, Williams TJ, Tippins JR, Morris HR, MacIntyre I. Пептид, родственный гену кальцитонина, является мощным сосудорасширяющим средством. Природа. 1985 г., 3–9 января; 313 (5997): 54–6. [PubMed: 3
4]- 30.
Berthoud HR, Neuhuber WL. Функциональная и химическая анатомия афферентной системы блуждающего нерва. Автон Нейроски. 2000 г., 20 декабря; 85 (1–3): 1–17. [PubMed: 11189015]
- 31.

Павлов В.А., Ван Х., Чура С.Дж., Фридман С.Г., Трейси К.Дж. Холинергический противовоспалительный путь: недостающее звено в нейроиммуномодуляции. Мол Мед. 2003 май-август 9(5-8):125-34. [Бесплатная статья PMC: PMC1430829] [PubMed: 14571320]
- 32.
Цучихаси К., Ёсихиро Т., Айкава Т., Нио К., Такаёси К., Ёкояма Т., Фуката М., Арита С., Арияма Х., Симидзу Й. Yoshida Y, Torisu T, Esaki M, Odashiro K, Kusaba H, Akashi K, Baba E. Метастатический рак пищевода, представляющий собой шок от повреждения блуждающего нерва, имитирующего барорецепторный рефлекс: клинический случай. Медицина (Балтимор). 2017 Декабрь;96(49):e8987. [Бесплатная статья PMC: PMC5728886] [PubMed: 271]
- 33.
Вуд JD. Применение классификационных схем к энтеральной нервной системе. J Auton Nerv Syst. 1994 г., июнь; 48 (1): 17–29. [PubMed: 8027516]
- 34.
Thayer JF, Sternberg EM. Невральные аспекты иммуномодуляции: фокус на блуждающий нерв.
 Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]
Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]- 35.
Лундберг Дж. М., Хёкфельт Т., Ангард А., Увнес-Валленстен К., Бримиджоин С., Бродин Э., Фаренкруг Дж. Периферийное распределение аксона: транспорт и некоторые аспекты возможного функционирования. Adv Biochem Psychopharmacol. 1980;22:25-36. [PubMed: 6156578]
- 36.
Leblanc GG, Trimmer BA, Landis SC. Нейропептид Y-подобная иммунореактивность в черепных парасимпатических нейронах крыс: сосуществование с вазоактивным кишечным пептидом и холин-ацетилтрансферазой. Proc Natl Acad Sci USA. 1987 May; 84(10):3511-5. [Бесплатная статья PMC: PMC304901] [PubMed: 3554241]
- 37.
Carlson AB, Kraus GP. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 23 августа 2021 г. Физиология, холинергические рецепторы. [В паблике: 30252390]
- 38.
Миллион М, Ларош М. Стресс, секс и кишечная нервная система.
 Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]
Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]- 39.
Хансен МБ. Энтеральная нервная система I: организация и классификация. Фармакол Токсикол. 2003 март; 92(3):105-13. [PubMed: 12753424]
- 40.
Вуд JD. Энтеральная нервная система: нейропатическая моторика желудочно-кишечного тракта. Dig Dis Sci. 2016 июль; 61 (7): 1803-16. [В паблике: 27142673]
- 41.
Сарна SK. Подвижность толстой кишки: от скамейки к постели. Морган и Клейпул Лайф Сайенсиз; Сан-Рафаэль (Калифорния): 2010. [PubMed: 21452445]
- 42.
Батлер С.Дж., Броннер М.Э. От классики к современности: анализ происхождения и судьбы периферической нервной системы и спинного мозга. Дев биол. 2015 15 февраля; 398 (2): 135-46. [Бесплатная статья PMC: PMC4845735] [PubMed: 25446276]
- 43.
Дьячук В., Фурлан А., Шахиди М.К., Джовенко М., Каукуа Н.
 , Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]
, Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]- 44.
Gariepy CE. Нарушения моторики кишечника и развитие энтеральной нервной системы. Педиатр рез. 2001 г., май; 49(5):605-13. [PubMed: 11328941]
- 45.
Сасселли В., Пахнис В., Бернс А.Дж. Энтеральная нервная система. Дев биол. 01 июня 2012 г .; 366 (1): 64–73. [PubMed: 222
]- 46.
Канагалингам С., Миллер Н.Р. Синдром Горнера: клинические перспективы. Глазной мозг. 2015;7:35-46. [Бесплатная статья PMC: PMC5398733] [PubMed: 28539793]
- 47.
Diamantis E, Farmaki P, Savvanis S, Athanasiadis G, Troupis T, Damaskos C. Повреждение симпатического нерва при раке щитовидной железы. Acta Medica (Градец Кралове).
 2017;60(4):135-139. [PubMed: 29716678]
2017;60(4):135-139. [PubMed: 29716678]- 48.
Хан З., Боллу ПК. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 4 мая 2021 г. Синдром Хорнера. [PubMed: 29763176]
- 49.
Lykstad J, Reddy V, Hanna A. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, путь расширения зрачков. [В паблике: 30571042]
- 50.
Делорт С., Марчи Э., Корреа М.А. Оксибутинин как альтернативное лечение гипергидроза. Бюстгальтеры Дерматол. 2017 март-апрель;92(2):217-220. [Бесплатная статья PMC: PMC5429108] [PubMed: 28538882]
- 51.
del Boz J. Системное лечение гипергидроза. Actas Дермосифилиогр. 2015 май; 106(4):271-7. [PubMed: 25638324]
- 52.
Haam SJ, Park SY, Paik HC, Lee DY. Реконструкция симпатического нерва при компенсаторном гипергидрозе после симпатической операции по поводу первичного гипергидроза.
 J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]
J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]- 53.
Mustafa HI, Fessel JP, Barwise J, Shannon JR, Raj SR, Diedrich A, Biaggioni I, Robertson D. Dysautonomia: периоперационные последствия. Анестезиология. 2012 Январь; 116 (1): 205-15. [Бесплатная статья PMC: PMC3296831] [PubMed: 22143168]
- 54.
McLeod JG. Исследование периферической нейропатии. J Neurol Нейрохирург Психиатрия. 1995 март; 58(3):274-83. [Бесплатная статья PMC: PMC1073360] [PubMed: 7897405]
- 55.
Ludwig PE, Reddy V, Varacallo M. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, центральная нервная система (ЦНС) [PubMed: 28723039]
- 56.
Санчес-Мансо Дж. К., Гуджарати Р., Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 октября 2021 г. Вегетативная дисфункция. [PubMed: 28613638]
- 57.

Беван Д.Р. Синдром Шай-Дрейгера. Обзор и описание анестезиологического обеспечения. Анестезия. 1979 октября; 34 (9): 866-73. [PubMed: 532923]
- 58.
Stirt JA, Frantz RA, Gunz EF, Conolly ME. Анестезия, катехоламины и гемодинамика при вегетативной дисфункции. Анест Анальг. 1982 г., август; 61 (8): 701-4. [PubMed: 7201274]
- 59.
Gunduz OH, Kenis-Coskun O. Блокада ганглиев как лечение боли: текущие перспективы. Джей Боль Рез. 2017;10:2815-2826. [Бесплатная статья PMC: PMC5734237] [PubMed: 2
02]
- 60.
Джон Р.С., Диксон Б., Шиенбаум Р. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 31 июля 2021 г. Блокада чревного сплетения. [PubMed: 30285364]
- 61.
Пираччини Э., Мунакоми С., Чанг К.В. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 августа 2021 г. Блоки звездчатого ганглия. [PubMed: 29939575]
- 62.

Александр К.Э., Де Хесус О, Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 30 августа 2021 г. Симпатическая блокада поясничного отдела. [В паблике: 28613759]
Copyright © 2022, StatPearls Publishing LLC.
Эта книга распространяется в соответствии с международной лицензией Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает использование, дублирование, адаптацию, распространение и воспроизведение на любом носителе или формате, при условии, что вы укажете автора(ов) оригинала и источник, будет дана ссылка на лицензию Creative Commons и указаны любые внесенные изменения.
ID книжной полки: NBK539845PMID: 30969667
Анатомия, вегетативная нервная система — StatPearls
Книжная полка NCBI. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2022 янв.
StatPearls [Интернет].
Показать подробности
Критерий поиска
Джошуа А. Ваксенбаум; Вамси Редди; Мэтью Варакалло.
Информация об авторе
Последнее обновление: 29 июля 2021 г.
Введение
Вегетативная нервная система — это компонент периферической нервной системы, который регулирует непроизвольные физиологические процессы, включая частоту сердечных сокращений, кровяное давление, дыхание, пищеварение и половое возбуждение. Он состоит из трех анатомически различных отделов: симпатического, парасимпатического и энтерального отделов.
Симпатическая нервная система (СНС) и парасимпатическая нервная система (ПНС) содержат как афферентные, так и эфферентные волокна, которые обеспечивают сенсорный вход и двигательный выход, соответственно, в центральную нервную систему (ЦНС). Как правило, двигательные пути СНС и ПНС состоят из серии из двух нейронов: преганглионарного нейрона с телом клетки в ЦНС и постганглионарного нейрона с телом клетки на периферии, иннервирующих ткани-мишени. Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Активация СНС приводит к состоянию общей повышенной активности и внимания: реакция «бей или беги». При этом повышается артериальное давление и частота сердечных сокращений, происходит гликогенолиз, прекращается перистальтика желудочно-кишечного тракта и т.д.[5] СНС иннервирует почти все живые ткани в организме. ПНС способствует процессам «отдыха и переваривания»; снижается частота сердечных сокращений и артериальное давление, возобновляется перистальтика желудочно-кишечного тракта / пищеварение и т. д. [5] [6] ПНС иннервирует только голову, внутренние органы и наружные гениталии, в значительной степени вакантна в большей части костно-мышечной системы и кожи, что делает ее значительно меньше, чем СНС. [7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
[7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
Пресинаптические нейроны как СНС, так и ПНС используют ацетилхолин (АХ) в качестве нейротрансмиттера. Постсинаптические симпатические нейроны обычно продуцируют норадреналин (НЭ) в качестве своего эффекторного передатчика для воздействия на ткани-мишени, в то время как постсинаптические парасимпатические нейроны повсеместно используют АХ. Известно, что энтеральные нейроны используют несколько основных нейротрансмиттеров, таких как АХ, закись азота и серотонин, и это лишь некоторые из них.[8]
Структура и функция
Симпатическая нервная система
Симпатические нейроны имеют клеточные тела, расположенные в промежуточных латеральных столбах или латеральных рогах спинного мозга. Пресинаптические волокна выходят из спинного мозга через передние корешки и входят в передние ветви спинномозговых нервов T1-L2 и в симпатические стволы через белые соединительные ветви. Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Паравертебральные ганглии существуют в виде узелков по всему симпатическому стволу, прилегающему к позвоночнику, где происходит синапс пре- и постганглионарных нейронов. Хотя количество может варьироваться в зависимости от человека, как правило, существует три шейных, 12 грудных, четыре поясничных и пять крестцовых ганглиев. Из них только шейные имеют названия верхних, средних и нижних шейных ганглиев. Нижний шейный ганглий может сливаться с первым грудным ганглием, образуя звездчатый ганглий.
Все нервы, расположенные дистальнее паравертебральных ганглиев, являются внутренностными нервами. Они передают афферентные и эфферентные волокна между ЦНС и внутренними органами. Сердечно-легочные внутренностные нервы несут постсинаптические волокна, направляющиеся в грудную полость.
Нервы, которые будут иннервировать органы брюшной полости и таза, проходят через паравертебральные нервы без образования синапсов, становясь внутрибрюшными тазовыми нервами. Эти нервы включают большой, малый, наименьший и поясничный внутренностные нервы. Пресинаптические нервы, наконец, образуют синапсы в превертебральных ганглиях, которые находятся ближе к органу-мишени. Предвертебральные ганглии входят в состав нервных сплетений, окружающих ветви аорты. К ним относятся чревный, аортокоренальный, а также верхний и нижний брыжеечные ганглии. Чревный ганглий получает вход от большого внутренностного нерва, аортокоренальный от малого и наименьшего внутренностного нерва, а верхний и нижний брыжеечные от наименьшего и поясничного внутренностного нервов. Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Общее правило двух нейронов для цепей СНС и ПНС имеет несколько заметных исключений. Симпатические и парасимпатические постганглионарные нейроны, которые образуют синапсы с ЭНС, функционально являются частью цепочки из трех или более нейронов. Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Постганглионарные симпатические нейроны высвобождают НЭ, который действует на адренергические рецепторы в ткани-мишени. Подтип рецептора, альфа-1, альфа-2, бета-1, бета-2 или бета-3, и ткани, в которых они экспрессируются, влияют на сродство НЭ к рецептору.[15] Для получения дополнительной информации см. статьи StatPearls, посвященные адренергическим рецепторам, по следующим ссылкам.[16][17][18]
Как уже говорилось, СНС позволяет организму справляться со стрессорами посредством реакции «бей или беги». Эта реакция в первую очередь регулирует кровеносные сосуды. Сосуды тонически иннервированы, и в большинстве случаев усиление симпатических сигналов приводит к вазоконстрикции и, противоположной вазодилатации. Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
СНС постоянно активна, даже в нестрессовых ситуациях. В дополнение к вышеупомянутой тонической стимуляции кровеносных сосудов, СНС активна во время нормального дыхательного цикла. Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Кроме того, СНС регулирует иммунитет посредством иннервации иммунных органов, таких как селезенка, тимус и лимфатические узлы.[15][22] Это влияние может усиливать или подавлять воспаление.[23] Клетки адаптивной иммунной системы в основном экспрессируют рецепторы бета-2, тогда как клетки врожденной иммунной системы экспрессируют их, а также адренергические рецепторы альфа-1 и альфа-2. Макрофаги активируются стимуляцией альфа-2 и подавляются активацией бета-2-адренергических рецепторов.
Большинство постганглионарных симпатических нейронов являются норадренергическими и также выделяют один или несколько пептидов, таких как нейропептид Y или соматостатин. Нейроны NE/нейропептида Y иннервируют кровеносные сосуды сердца, тем самым регулируя кровоток [25], в то время как нейроны NE/соматостатина чревного и верхнего брыжеечного ганглиев иннервируют подслизистые ганглии кишечника и участвуют в контроле моторики желудочно-кишечного тракта. Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Пептиды также связаны с холинергическими симпатическими постганглионарными нейронами. Эти нейроны чаще всего иннервируют потовые железы и прекапиллярные сосуды сопротивления в скелетных мышцах и продуцируют вазоактивный интестинальный полипептид вместе с АХ. Пептид, родственный гену кальцитонина, обладающий мощным сосудорасширяющим действием, также был обнаружен в паравертебральных симпатических нейронах.
Парасимпатическая нервная система
Парасимпатические волокна выходят из ЦНС через черепно-мозговые нервы (ЧН) III, VII, IX и X, а также через нервные корешки S2-4. Есть четыре пары парасимпатических ганглиев, и все они расположены в голове. CN III через цилиарный ганглий иннервирует радужную оболочку и ресничные мышцы глаза. CN VII иннервирует слезные, носовые, небные и глоточные железы через крылонебный ганглий, а также подъязычную и поднижнечелюстную железы через поднижнечелюстной ганглий. CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
Дорсальное ядро: обеспечивает парасимпатический выход к внутренним органам
Спинальное ядро тройничного нерва: получает информацию о прикосновении, боли и температуре наружного уха, слизистой оболочки гортани и части твердой мозговой оболочки
Кроме того, блуждающий нерв проводит сенсорную информацию от барорецепторов каротидного синуса и дуги аорты к мозговому веществу. [32]
[32]
Как упоминалось во введении, блуждающий нерв отвечает за процессы «отдыха и переваривания». Блуждающий нерв способствует сердечной релаксации в нескольких аспектах функции. Он снижает сократительную способность предсердий и в меньшей степени желудочков. Прежде всего, он снижает скорость проведения через атриовентрикулярный узел. Именно благодаря этому механизму массаж каротидного синуса ограничивает повторный вход при синдроме Вольфа-Паркинсона-Уайта.[2] Другая ключевая функция ПНС связана с пищеварением. Парасимпатические волокна, идущие к голове, способствуют слюноотделению, а те, которые соединяются с ЭНС, приводят к усилению перистальтической и секреторной активности.[4][33] Блуждающий нерв также оказывает значительное влияние на дыхательный цикл. В непатологическом состоянии парасимпатические нервы возбуждаются во время выдоха, сокращая и напрягая дыхательные пути, чтобы предотвратить коллапс. Эта функция связана с ПНС в возникновении послеоперационного острого респираторного дистресс-синдрома. [2][21]
[2][21]
Из-за широкой природы блуждающего нерва он был описан как идеальная «система раннего предупреждения» для чужеродных захватчиков, а также для наблюдения за восстановлением организма. До 80% волокон блуждающего нерва являются чувствительными и иннервируют почти все основные органы. Было обнаружено, что парасимпатические ганглии экспрессируют рецепторы интерлейкина-1, ключевого цитокина в воспалительном иммунном ответе.[34] Это, в свою очередь, активирует гипоталамо-гипофизарно-надпочечниковую ось и СНС, что приводит к высвобождению глюкокортикоидов и НЭ соответственно.[2] Исследования коррелируют ингибирование действия блуждающего нерва посредством ваготомии и холинергических ингибиторов со значительно сниженными, если не полностью устраненными, аллергическими, астматическими и воспалительными реакциями.[7]
Постганглионарные парасимпатические нейроны высвобождают АХ, который действует на мускариновые и никотиновые рецепторы, каждый из которых имеет различные субъединицы: M1, M2 и M3, а также N1 и N2, где «M» и «N» обозначают мускарин и никотин соответственно. [5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
[5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
Кишечная нервная система (ENS)
ЭНС состоит из двух ганглиозных сплетений: мышечно-кишечного (Ауэрбаха) и подслизистого (Мейснера). Межмышечное сплетение находится между продольной и круговой гладкой мускулатурой желудочно-кишечного тракта, а подслизистое сплетение находится в подслизистой оболочке. ЭНС самодостаточна, функционирует за счет локальной рефлекторной активности, но часто получает информацию от СНС и ПНС и обеспечивает обратную связь с ними. ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
Подслизистое сплетение регулирует движение воды и электролитов через стенку кишечника, в то время как мышечно-кишечное сплетение координирует сократительную способность циркулярных и продольных мышечных клеток кишечника для обеспечения перистальтики.[39]
Подвижность в ЭНС обеспечивается рефлекторной цепью, включающей круговые и продольные мышцы. Никотиновые синапсы между интернейронами опосредуют рефлекторные цепи.[39] Когда цепь активируется присутствием болюса, возбуждающие нейроны в круговой мышце и тормозные нейроны в продольной мышце возбуждаются, создавая узкий участок кишечника проксимальнее болюса; это известно как пропульсивный сегмент. Одновременно возбуждающие нейроны в продольных мышцах и тормозные нейроны в круговых мышцах возбуждают «воспринимающий сегмент» кишечника, в котором будет продолжаться болюс. Этот процесс повторяется с каждым последующим отделом кишечника. [40]
[40]
ENS имеет некоторые сходства с CNS. Как и в ЦНС, кишечные нейроны могут быть биполярными, псевдоуниполярными и мультиполярными, между которыми осуществляется нейромодуляция посредством возбуждающей и тормозной связи.[1] Точно так же нейроны ЭНС используют более 30 нейротрансмиттеров, которые аналогичны нейротрансмиттерам ЦНС, причем наиболее распространенными являются холинергические и нитрергические передатчики.
Хотя большая часть этого обсуждения была сосредоточена на эфферентных функциях ВНС, афферентные волокна отвечают за многочисленные рефлекторные действия, которые регулируют все, от частоты сердечных сокращений до иммунной системы. Обратная связь от ВНС обычно обрабатывается на подсознательном уровне для создания рефлекторных действий в висцеральных или соматических частях тела. Сознательное ощущение во внутренних органах часто интерпретируется как разлитая боль или спазмы, которые могут коррелировать с чувством голода, полноты или тошноты. Эти ощущения чаще всего возникают в результате внезапного растяжения/сокращения, химических раздражителей или патологических состояний, таких как ишемия. [41]
[41]
Эмбриология
Периферическая нервная система происходит из клеток нервного гребня. Нервный гребень аксиально делится на краниальные, блуждающие, туловищные и пояснично-крестцовые клетки нервного гребня. Клетки ствола нервного гребня вносят вклад в дорсальные корешки спинного мозга и симпатические ганглии. Парасимпатическая иннервация сердца формируется из блуждающего нервного гребня. Было показано, что большая часть парасимпатической нервной системы, включая все ганглии головы, возникает из глиальных клеток, а не из клеток нервного гребня.[42][43]
ЭНС происходит из блуждающего нервного гребня с клетками, которые мигрируют рострально-каудально через кишечную стенку, образуя сеть глии и нейронов различных подтипов. Клетки ЭНС завершают свою миграцию к 4-7 неделям развития и экспрессируют все разновидности нейротрансмиттеров ЭНС к 24-й неделе беременности. Однако моторика зрелого кишечника не реализуется, по крайней мере, до поздних сроков беременности или вскоре после рождения.
Хирургические аспекты
Синдром Горнера — это мягкое, редкое состояние, часто проявляющееся односторонним птозом, суженным, но реактивным зрачком и лицевым ангидрозом, вторичным по отношению к повреждению симпатического нерва в окулосимпатическом пути.[46] Это повреждение может иметь центральную причину, такую как инфаркт латерального продолговатого мозга, или периферическую, такую как повреждение, вторичное по отношению к торакальной хирургии или частичной/тотальной резекции щитовидной железы.[46][47] Более централизованные поражения, как правило, коррелируют с комплексом симптомов, включающим синдром Горнера.[46] Для получения дополнительной информации см. соответствующие статьи StatPearls здесь.[48][49]]
Гипергидроз — распространенное заболевание, характеризующееся повышенной потливостью, преимущественно лица, ладоней, подошв и/или подмышечных впадин. Хотя причина первичного гипергидроза до конца не выяснена, его связывают с повышенной холинергической стимуляцией. Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Клиническое значение
Из-за экстенсивного характера вегетативной нервной системы на нее может влиять широкий спектр состояний. Некоторые из них включают[53][54][55]
Унаследованные
Приобретен
Диабет-сахарный0003
Инфекции: ботулизм, болезнь Шагаса, ВИЧ, проказа, болезнь Лайма, столбняка
Аутоиммунный: Гийен-Барре, Ламберт-Этотонский миастеник-синдром 900.
 0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами ЛевиНеоплазия: опухоли головного мозга, паранеопластические синдромы
Аналогичным образом вегетативная невропатия может проявляться почти в любой системе. Ортостатическая гипотензия является наиболее распространенной вегетативной дизавтономией, но могут присутствовать и многие другие, менее изученные симптомы [53] 9.0003
Сердечно-сосудистые
Желудочно-кишечные
Дисфагия
Запоры
7 Тошнота, рвота, полноту брюшной полости
Genitourinary
PUPDDER ATONONY
9967
PUPLDER ATONONY
PUPLDER ATONONY
79967PUPLDER ATONONY
7067PUPLDER
9.
PUPLDER
.0003
Decreased pupil size
Sexual
Erectile dysfunction
Retrograde ejaculation
Sudomotor
Anhidrosis
Gustatory sweating
Вазомоторный
Похолодание конечностей (из-за потери вазомоторных реакций)
Отек (из-за потери вазомоторного тонуса и повышения проницаемости сосудов)
Наиболее распространенными симптомами ортостатической гипотензии являются головокружение, туннельное зрение и дискомфорт в голове, шее или груди. Она может проявляться одновременно с артериальной гипертензией в положении лежа из-за повышенного периферического сопротивления, что вызывает натрийурез, усугубляющий ортостатическую гипотензию. Существует множество других, более мягких стимулов, которые могут либо снижать артериальное давление (стоя, еда, Вальсальва, обезвоживание, физические упражнения, гипервентиляция и т. д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
Оценку ортостатической гипотензии обычно проводят с помощью ортостатического тестирования путем повторного измерения артериального давления и частоты сердечных сокращений в положении лежа и стоя, а также с помощью теста с наклонным столом. Однако преимущество этого последнего теста минимально по сравнению с ортостатическим тестом, при этом основным преимуществом является безопасность и удобство для пациента.
Пациенты с дизавтономией склонны к гипотонии во время анестезии[56]. Эту проблему можно надлежащим образом решить с помощью низких доз фенилэфрина, агониста альфа-1. Точно так же гипертонию в положении лежа можно контролировать с помощью трансдермальных или внутривенных нитратов. [53, 57, 58].
Известно, что симпатическая нервная система играет роль в ноцицепции. Есть предположения, что ВНС оказывает регуляторно-тормозное влияние на боль, утрата которого создает цепь положительной обратной связи, приводящую к гипервозбудимости ноцицептивных нервных волокон. Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Большинство состояний, связанных с ЭНС, имеют врожденное происхождение и проявляются в раннем детстве.[44] Энтеральные нейроны расслабляют гладкую мускулатуру кишечника. Их отсутствие приводит к тоническому сокращению кишечника, что приводит к непроходимости кишечника. К предъявляемым жалобам часто относятся гастроэзофагеальный рефлюкс, диспептические синдромы, запоры, хронические боли в животе, синдром раздраженного кишечника. Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Схема вегетативной нервной системы. Предоставлено Генри Греем (1918 г.): Анатомия человеческого тела
Ссылки
- 1.

Стернини С. Организация периферической нервной системы: вегетативные и сенсорные ганглии. J Investig Dermatol Symp Proc. 1997 авг.; 2(1):1–7. [PubMed: 9487007]
- 2.
Каремакер Дж.М. Введение в вегетативную нервную функцию. Физиол Изм. 2017 Май; 38 (5): R89-R118. [PubMed: 28304283]
- 3.
Lake JI, Heuckeroth RO. Развитие энтеральной нервной системы: миграция, дифференцировка и заболевание. Am J Physiol Gastrointest Liver Physiol. 01 июля 2013 г.; 305(1):G1-24. [Бесплатная статья PMC: PMC3725693] [PubMed: 23639815]
- 4.
Siéssere S, Vitti M, Sousa LG, Semprini M, Iyomasa MM, Regalo SC. Анатомическая вариация краниальных парасимпатических ганглиев. Браз Орал Рез. 2008 г., апрель-июнь; 22(2):101-5. [В паблике: 18622477]
- 5.
Купман Ф.А., Стооф С.П., Штрауб Р.Х., Ван Маанен М.А., Верворделдонк М.Дж., Так Р.П. Восстановление баланса вегетативной нервной системы как инновационный подход к лечению ревматоидного артрита.
 Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]
Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]- 6.
Kenney MJ, Ganta CK. Взаимодействие вегетативной нервной системы и иммунной системы. сост. физиол. 2014 июль;4(3):1177-200. [Бесплатная статья PMC: PMC4374437] [PubMed: 24944034]
- 7.
Скотт Г.Д., Фрайер А.Д. Роль парасимпатических нервов и мускариновых рецепторов при аллергии и астме. Хим Иммунол Аллергия. 2012;98:48-69. [Бесплатная статья PMC: PMC4039300] [PubMed: 22767057]
- 8.
McConalogue K, Furness JB. Нейротрансмиттеры желудочно-кишечного тракта. Baillieres Clin Endocrinol Metab. 1994 г., январь; 8 (1): 51–76. [PubMed: 7
3]
- 9.
Шихан Д., Пик Дж. Соединительные ветви у макак-резусов. Дж Анат. 1943 января; 77 (часть 2): 125–39. [PMC бесплатная статья: PMC1252749] [PubMed: 17104919]
- 10.
Лукас М., Клаассен З., Мербс В., Таббс Р.С., Гелецкий Дж.
 , Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]
, Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]- 11.
Ян Х.Дж., Гил Ю.К., Ли В.Дж., Ким Т.Дж., Ли Х.И. Анатомия грудных внутренностных нервов для хирургической резекции. Клин Анат. 2008 март; 21(2):171-7. [PubMed: 18288763]
- 12.
Беверидж Т.С., Джонсон М., Пауэр А, Пауэр Н.Е., Оллман Б.Л. Анатомия нервов и ганглиев аортального сплетения у мужчин. Дж Анат. 2015 Январь; 226 (1): 93-103. [Бесплатная статья PMC: PMC4313893] [PubMed: 25382240]
- 13.
Ehrhardt JD, Weber C, Lopez-Ojeda W. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Анатомия, грудная клетка, большие внутренностные нервы. [PubMed: 29763202]
- 14.
Бриндли Р.Л., Бауэр М.Б., Блейкли Р.Д., Карри КПМ. Серотонин и переносчики серотонина в мозговом веществе надпочечников: потенциальный узел для модуляции симпатической реакции на стресс.
 ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]
ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]- 15.
Нэнси Д.М., Сандерс В.М. Вегетативная иннервация и регуляция иммунной системы (1987-2007 гг.). Мозг Behav Immun. 2007 авг; 21 (6): 736-45. [Бесплатная статья PMC: PMC1986730] [PubMed: 17467231]
- 16.
Alhayek S, Preuss CV. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Рецепторы бета-1. [PubMed: 30422499]
- 17.
Фарзам К., Кидрон А., Лахкар А.Д. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 18 июля 2021 г. Адренергические препараты. [PubMed: 30480963]
- 18.
Халид М.М., Галуска М.А., Гамильтон Р.Дж. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 26 июля 2021 г. Токсичность бета-блокаторов. [В паблике: 28846217]
- 19.
Хойш Г., Темер В. [Значение симпатической нервной системы для коронарного кровообращения].
 З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]
З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]- 20.
Варгас Пелаес А.Ф., Гао З., Ахмад Т.А., Лойенбергер Ю.А., Проктор Д.Н., Маман С.Р., Мюллер М.Д. Влияние адреномиметиков на коронарный кровоток: лабораторное исследование на здоровых добровольцах. Physiol Rep. 2016 May;4(10) [бесплатная статья PMC: PMC4886172] [PubMed: 27225628]
- 21.
Chen IC, Kuo J, Ko WJ, Shih HC, Kuo CD. Повышенное сопротивление потоку и снижение скорости потока у пациентов с острым респираторным дистресс-синдромом: роль вегетативной нервной модуляции. J Chin Med Assoc. 2016 Январь; 79(1):17-24. [PubMed: 26589196]
- 22.
Штернберг Э.М. Нейронная регуляция врожденного иммунитета: скоординированный неспецифический ответ хозяина на патогены. Нат Рев Иммунол. 2006 апр; 6 (4): 318-28. [Бесплатная статья PMC: PMC1783839] [PubMed: 16557263]
- 23.
Еленков И.Ю., Уайлдер Р.Л., Хрусос Г.П., Визи Э.С. Симпатический нерв — интегративный интерфейс между двумя надсистемами: мозгом и иммунной системой.
 Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]
Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]- 24.
Bellinger DL, Millar BA, Perez S, Carter J, Wood C, ThyagaRajan S, Molinaro C, Lubahn C, Lorton D. Симпатическая модуляция иммунитета: отношение к болезни. Клеточный Иммунол. 2008 март-апрель; 252(1-2):27-56. [Бесплатная статья PMC: PMC3551630] [PubMed: 18308299]
- 25.
Лундберг Дж. М., Хёкфельт Т. Множественное сосуществование пептидов и классических передатчиков в периферических вегетативных и сенсорных нейронах — функциональные и фармакологические последствия. Прог Мозг Res. 1986;68:241-62. [PubMed: 2882554]
- 26.
Лундберг Дж.М., Хёкфельт Т., Шульцберг М., Увнес-Валленстен К., Келер С., Саид С.И. Возникновение иммунореактивности, подобной вазоактивному кишечному полипептиду (ВИП), в некоторых холинергических нейронах кошки: данные комбинированной иммуногистохимии и окрашивания ацетилхолинэстеразой. Неврология. 1979;4(11):1539-59. [PubMed: 3
]- 27.

Landis SC, Fredieu JR. Сосуществование пептида, родственного гену кальцитонина, и вазоактивного интестинального пептида в холинергической симпатической иннервации потовых желез крыс. Мозг Res. 1986 г., 02 июля; 377 (1): 177–81. [PubMed: 3524749]
- 28.
Lindh B, Lundberg JM, Hökfelt T, Elfvin LG, Fahrenkrug J, Fischer J. Сосуществование CGRP- и VIP-подобных иммунореактивностей в популяции нейронов звездчатых ганглиев кошек . Acta Physiol Scand. 1987 ноября; 131 (3): 475-6. [PubMed: 3321916]
- 29.
Brain SD, Williams TJ, Tippins JR, Morris HR, MacIntyre I. Пептид, родственный гену кальцитонина, является мощным сосудорасширяющим средством. Природа. 1985 г., 3–9 января; 313 (5997): 54–6. [PubMed: 3
4]- 30.
Berthoud HR, Neuhuber WL. Функциональная и химическая анатомия афферентной системы блуждающего нерва. Автон Нейроски. 2000 г., 20 декабря; 85 (1–3): 1–17. [PubMed: 11189015]
- 31.

Павлов В.А., Ван Х., Чура С.Дж., Фридман С.Г., Трейси К.Дж. Холинергический противовоспалительный путь: недостающее звено в нейроиммуномодуляции. Мол Мед. 2003 май-август 9(5-8):125-34. [Бесплатная статья PMC: PMC1430829] [PubMed: 14571320]
- 32.
Цучихаси К., Ёсихиро Т., Айкава Т., Нио К., Такаёси К., Ёкояма Т., Фуката М., Арита С., Арияма Х., Симидзу Й. Yoshida Y, Torisu T, Esaki M, Odashiro K, Kusaba H, Akashi K, Baba E. Метастатический рак пищевода, представляющий собой шок от повреждения блуждающего нерва, имитирующего барорецепторный рефлекс: клинический случай. Медицина (Балтимор). 2017 Декабрь;96(49):e8987. [Бесплатная статья PMC: PMC5728886] [PubMed: 271]
- 33.
Вуд JD. Применение классификационных схем к энтеральной нервной системе. J Auton Nerv Syst. 1994 г., июнь; 48 (1): 17–29. [PubMed: 8027516]
- 34.
Thayer JF, Sternberg EM. Невральные аспекты иммуномодуляции: фокус на блуждающий нерв.
 Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]
Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]- 35.
Лундберг Дж. М., Хёкфельт Т., Ангард А., Увнес-Валленстен К., Бримиджоин С., Бродин Э., Фаренкруг Дж. Периферийное распределение аксона: транспорт и некоторые аспекты возможного функционирования. Adv Biochem Psychopharmacol. 1980;22:25-36. [PubMed: 6156578]
- 36.
Leblanc GG, Trimmer BA, Landis SC. Нейропептид Y-подобная иммунореактивность в черепных парасимпатических нейронах крыс: сосуществование с вазоактивным кишечным пептидом и холин-ацетилтрансферазой. Proc Natl Acad Sci USA. 1987 May; 84(10):3511-5. [Бесплатная статья PMC: PMC304901] [PubMed: 3554241]
- 37.
Carlson AB, Kraus GP. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 23 августа 2021 г. Физиология, холинергические рецепторы. [В паблике: 30252390]
- 38.
Миллион М, Ларош М. Стресс, секс и кишечная нервная система.
 Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]
Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]- 39.
Хансен МБ. Энтеральная нервная система I: организация и классификация. Фармакол Токсикол. 2003 март; 92(3):105-13. [PubMed: 12753424]
- 40.
Вуд JD. Энтеральная нервная система: нейропатическая моторика желудочно-кишечного тракта. Dig Dis Sci. 2016 июль; 61 (7): 1803-16. [В паблике: 27142673]
- 41.
Сарна SK. Подвижность толстой кишки: от скамейки к постели. Морган и Клейпул Лайф Сайенсиз; Сан-Рафаэль (Калифорния): 2010. [PubMed: 21452445]
- 42.
Батлер С.Дж., Броннер М.Э. От классики к современности: анализ происхождения и судьбы периферической нервной системы и спинного мозга. Дев биол. 2015 15 февраля; 398 (2): 135-46. [Бесплатная статья PMC: PMC4845735] [PubMed: 25446276]
- 43.
Дьячук В., Фурлан А., Шахиди М.К., Джовенко М., Каукуа Н.
 , Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]
, Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]- 44.
Gariepy CE. Нарушения моторики кишечника и развитие энтеральной нервной системы. Педиатр рез. 2001 г., май; 49(5):605-13. [PubMed: 11328941]
- 45.
Сасселли В., Пахнис В., Бернс А.Дж. Энтеральная нервная система. Дев биол. 01 июня 2012 г .; 366 (1): 64–73. [PubMed: 222
]- 46.
Канагалингам С., Миллер Н.Р. Синдром Горнера: клинические перспективы. Глазной мозг. 2015;7:35-46. [Бесплатная статья PMC: PMC5398733] [PubMed: 28539793]
- 47.
Diamantis E, Farmaki P, Savvanis S, Athanasiadis G, Troupis T, Damaskos C. Повреждение симпатического нерва при раке щитовидной железы. Acta Medica (Градец Кралове).
 2017;60(4):135-139. [PubMed: 29716678]
2017;60(4):135-139. [PubMed: 29716678]- 48.
Хан З., Боллу ПК. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 4 мая 2021 г. Синдром Хорнера. [PubMed: 29763176]
- 49.
Lykstad J, Reddy V, Hanna A. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, путь расширения зрачков. [В паблике: 30571042]
- 50.
Делорт С., Марчи Э., Корреа М.А. Оксибутинин как альтернативное лечение гипергидроза. Бюстгальтеры Дерматол. 2017 март-апрель;92(2):217-220. [Бесплатная статья PMC: PMC5429108] [PubMed: 28538882]
- 51.
del Boz J. Системное лечение гипергидроза. Actas Дермосифилиогр. 2015 май; 106(4):271-7. [PubMed: 25638324]
- 52.
Haam SJ, Park SY, Paik HC, Lee DY. Реконструкция симпатического нерва при компенсаторном гипергидрозе после симпатической операции по поводу первичного гипергидроза.
 J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]
J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]- 53.
Mustafa HI, Fessel JP, Barwise J, Shannon JR, Raj SR, Diedrich A, Biaggioni I, Robertson D. Dysautonomia: периоперационные последствия. Анестезиология. 2012 Январь; 116 (1): 205-15. [Бесплатная статья PMC: PMC3296831] [PubMed: 22143168]
- 54.
McLeod JG. Исследование периферической нейропатии. J Neurol Нейрохирург Психиатрия. 1995 март; 58(3):274-83. [Бесплатная статья PMC: PMC1073360] [PubMed: 7897405]
- 55.
Ludwig PE, Reddy V, Varacallo M. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, центральная нервная система (ЦНС) [PubMed: 28723039]
- 56.
Санчес-Мансо Дж. К., Гуджарати Р., Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 октября 2021 г. Вегетативная дисфункция. [PubMed: 28613638]
- 57.

Беван Д.Р. Синдром Шай-Дрейгера. Обзор и описание анестезиологического обеспечения. Анестезия. 1979 октября; 34 (9): 866-73. [PubMed: 532923]
- 58.
Stirt JA, Frantz RA, Gunz EF, Conolly ME. Анестезия, катехоламины и гемодинамика при вегетативной дисфункции. Анест Анальг. 1982 г., август; 61 (8): 701-4. [PubMed: 7201274]
- 59.
Gunduz OH, Kenis-Coskun O. Блокада ганглиев как лечение боли: текущие перспективы. Джей Боль Рез. 2017;10:2815-2826. [Бесплатная статья PMC: PMC5734237] [PubMed: 2
02]
- 60.
Джон Р.С., Диксон Б., Шиенбаум Р. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 31 июля 2021 г. Блокада чревного сплетения. [PubMed: 30285364]
- 61.
Пираччини Э., Мунакоми С., Чанг К.В. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 августа 2021 г. Блоки звездчатого ганглия. [PubMed: 29939575]
- 62.

Александр К.Э., Де Хесус О, Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 30 августа 2021 г. Симпатическая блокада поясничного отдела. [В паблике: 28613759]
Copyright © 2022, StatPearls Publishing LLC.
Эта книга распространяется в соответствии с международной лицензией Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает использование, дублирование, адаптацию, распространение и воспроизведение на любом носителе или формате, при условии, что вы укажете автора(ов) оригинала и источник, будет дана ссылка на лицензию Creative Commons и указаны любые внесенные изменения.
ID книжной полки: NBK539845PMID: 30969667
Анатомия, вегетативная нервная система — StatPearls
Книжная полка NCBI. Служба Национальной медицинской библиотеки, Национальных институтов здоровья.
StatPearls [Интернет]. Остров сокровищ (Флорида): StatPearls Publishing; 2022 янв.
StatPearls [Интернет].
Показать подробности
Критерий поиска
Джошуа А. Ваксенбаум; Вамси Редди; Мэтью Варакалло.
Информация об авторе
Последнее обновление: 29 июля 2021 г.
Введение
Вегетативная нервная система — это компонент периферической нервной системы, который регулирует непроизвольные физиологические процессы, включая частоту сердечных сокращений, кровяное давление, дыхание, пищеварение и половое возбуждение. Он состоит из трех анатомически различных отделов: симпатического, парасимпатического и энтерального отделов.
Симпатическая нервная система (СНС) и парасимпатическая нервная система (ПНС) содержат как афферентные, так и эфферентные волокна, которые обеспечивают сенсорный вход и двигательный выход, соответственно, в центральную нервную систему (ЦНС). Как правило, двигательные пути СНС и ПНС состоят из серии из двух нейронов: преганглионарного нейрона с телом клетки в ЦНС и постганглионарного нейрона с телом клетки на периферии, иннервирующих ткани-мишени. Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Энтеральная нервная система (ЭНС) представляет собой обширную паутинную структуру, способную функционировать независимо от остальной части нервной системы.[1][2] Он содержит более 100 миллионов нейронов более 15 морфологий, что больше, чем сумма всех других периферических ганглиев, и в основном отвечает за регуляцию пищеварительных процессов.
Активация СНС приводит к состоянию общей повышенной активности и внимания: реакция «бей или беги». При этом повышается артериальное давление и частота сердечных сокращений, происходит гликогенолиз, прекращается перистальтика желудочно-кишечного тракта и т.д.[5] СНС иннервирует почти все живые ткани в организме. ПНС способствует процессам «отдыха и переваривания»; снижается частота сердечных сокращений и артериальное давление, возобновляется перистальтика желудочно-кишечного тракта / пищеварение и т. д. [5] [6] ПНС иннервирует только голову, внутренние органы и наружные гениталии, в значительной степени вакантна в большей части костно-мышечной системы и кожи, что делает ее значительно меньше, чем СНС. [7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
[7] ЭНС состоит из рефлекторных путей, которые контролируют пищеварительные функции сокращения/расслабления мышц, секреции/абсорбции и кровотока.[3]
Пресинаптические нейроны как СНС, так и ПНС используют ацетилхолин (АХ) в качестве нейротрансмиттера. Постсинаптические симпатические нейроны обычно продуцируют норадреналин (НЭ) в качестве своего эффекторного передатчика для воздействия на ткани-мишени, в то время как постсинаптические парасимпатические нейроны повсеместно используют АХ. Известно, что энтеральные нейроны используют несколько основных нейротрансмиттеров, таких как АХ, закись азота и серотонин, и это лишь некоторые из них.[8]
Структура и функция
Симпатическая нервная система
Симпатические нейроны имеют клеточные тела, расположенные в промежуточных латеральных столбах или латеральных рогах спинного мозга. Пресинаптические волокна выходят из спинного мозга через передние корешки и входят в передние ветви спинномозговых нервов T1-L2 и в симпатические стволы через белые соединительные ветви. Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Отсюда волокна могут подниматься или спускаться по симпатическому стволу к верхнему или нижнему паравертебральному узлу, соответственно, проходить к соседним передним ветвям спинномозгового нерва через серые коммуникантные ветви или пересекать ствол без синапсов и продолжаться через брюшно-тазовый внутренностный нерв, чтобы достичь превертебральные ганглии. Из-за центрального расположения симпатических ганглиев пресинаптические волокна, как правило, короче, чем их постсинаптические аналоги.]
Паравертебральные ганглии существуют в виде узелков по всему симпатическому стволу, прилегающему к позвоночнику, где происходит синапс пре- и постганглионарных нейронов. Хотя количество может варьироваться в зависимости от человека, как правило, существует три шейных, 12 грудных, четыре поясничных и пять крестцовых ганглиев. Из них только шейные имеют названия верхних, средних и нижних шейных ганглиев. Нижний шейный ганглий может сливаться с первым грудным ганглием, образуя звездчатый ганглий.
Все нервы, расположенные дистальнее паравертебральных ганглиев, являются внутренностными нервами. Они передают афферентные и эфферентные волокна между ЦНС и внутренними органами. Сердечно-легочные внутренностные нервы несут постсинаптические волокна, направляющиеся в грудную полость.
Нервы, которые будут иннервировать органы брюшной полости и таза, проходят через паравертебральные нервы без образования синапсов, становясь внутрибрюшными тазовыми нервами. Эти нервы включают большой, малый, наименьший и поясничный внутренностные нервы. Пресинаптические нервы, наконец, образуют синапсы в превертебральных ганглиях, которые находятся ближе к органу-мишени. Предвертебральные ганглии входят в состав нервных сплетений, окружающих ветви аорты. К ним относятся чревный, аортокоренальный, а также верхний и нижний брыжеечные ганглии. Чревный ганглий получает вход от большого внутренностного нерва, аортокоренальный от малого и наименьшего внутренностного нерва, а верхний и нижний брыжеечные от наименьшего и поясничного внутренностного нервов. Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Чревный ганглий иннервирует органы, производные от передней кишки: дистальный отдел пищевода, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочную железу, печень, билиарную систему, селезенку и надпочечники. Верхний брыжеечный ганглий иннервирует производные средней кишки: дистальный отдел двенадцатиперстной кишки, тощую кишку, подвздошную кишку, слепую кишку, аппендикс, восходящую ободочную кишку и проксимальный отдел поперечной ободочной кишки. Наконец, нижний брыжеечный ганглий обеспечивает симпатическую иннервацию структур, развившихся из задней кишки: дистального отдела поперечной, нисходящей и сигмовидной кишки; прямая кишка и верхний анальный канал; а также мочевой пузырь, наружные половые органы и гонады. Для получения дополнительной информации см. соответствующую статью StatPearls по этой ссылке.[13]
Общее правило двух нейронов для цепей СНС и ПНС имеет несколько заметных исключений. Симпатические и парасимпатические постганглионарные нейроны, которые образуют синапсы с ЭНС, функционально являются частью цепочки из трех или более нейронов. Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Пресинаптические симпатические волокна, предназначенные для мозгового вещества надпочечников, проходят через чревные ганглии и образуют синапс непосредственно на хромаффинных клетках. Эти уникальные клетки функционируют как постганглионарные волокна, секретирующие адреналин непосредственно в венозную систему.[1][2][14]
Постганглионарные симпатические нейроны высвобождают НЭ, который действует на адренергические рецепторы в ткани-мишени. Подтип рецептора, альфа-1, альфа-2, бета-1, бета-2 или бета-3, и ткани, в которых они экспрессируются, влияют на сродство НЭ к рецептору.[15] Для получения дополнительной информации см. статьи StatPearls, посвященные адренергическим рецепторам, по следующим ссылкам.[16][17][18]
Как уже говорилось, СНС позволяет организму справляться со стрессорами посредством реакции «бей или беги». Эта реакция в первую очередь регулирует кровеносные сосуды. Сосуды тонически иннервированы, и в большинстве случаев усиление симпатических сигналов приводит к вазоконстрикции и, противоположной вазодилатации. Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
Исключения составляют коронарные сосуды и сосуды, снабжающие скелетные мышцы и наружные половые органы, для которых возникает обратная реакция.[2] Этот противоречивый эффект опосредуется балансом активности альфа- и бета-рецепторов. В физиологическом состоянии стимуляция бета-рецепторов увеличивает расширение коронарных сосудов, но этот эффект притупляется опосредованной альфа-рецептором вазоконстрикцией. В патологическом состоянии, например при ишемической болезни сердца, активность альфа-рецепторов повышается, а бета-активность притупляется. Таким образом, коронарные артерии могут сужаться при симпатической стимуляции [19].] Симпатическая активация увеличивает частоту сердечных сокращений и сократительную силу, что, однако, увеличивает метаболические потребности и, таким образом, наносит ущерб сердечной функции у людей с нарушениями.[20]
СНС постоянно активна, даже в нестрессовых ситуациях. В дополнение к вышеупомянутой тонической стимуляции кровеносных сосудов, СНС активна во время нормального дыхательного цикла. Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Симпатическая активация дополняет ПНС, действуя во время вдоха, расширяя дыхательные пути, обеспечивая соответствующий приток воздуха.[2][21]
Кроме того, СНС регулирует иммунитет посредством иннервации иммунных органов, таких как селезенка, тимус и лимфатические узлы.[15][22] Это влияние может усиливать или подавлять воспаление.[23] Клетки адаптивной иммунной системы в основном экспрессируют рецепторы бета-2, тогда как клетки врожденной иммунной системы экспрессируют их, а также адренергические рецепторы альфа-1 и альфа-2. Макрофаги активируются стимуляцией альфа-2 и подавляются активацией бета-2-адренергических рецепторов.
Большинство постганглионарных симпатических нейронов являются норадренергическими и также выделяют один или несколько пептидов, таких как нейропептид Y или соматостатин. Нейроны NE/нейропептида Y иннервируют кровеносные сосуды сердца, тем самым регулируя кровоток [25], в то время как нейроны NE/соматостатина чревного и верхнего брыжеечного ганглиев иннервируют подслизистые ганглии кишечника и участвуют в контроле моторики желудочно-кишечного тракта. Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Предполагается, что эти пептиды служат для модуляции реакции постсинаптического нейрона на первичный нейротрансмиттер.[1]
Пептиды также связаны с холинергическими симпатическими постганглионарными нейронами. Эти нейроны чаще всего иннервируют потовые железы и прекапиллярные сосуды сопротивления в скелетных мышцах и продуцируют вазоактивный интестинальный полипептид вместе с АХ. Пептид, родственный гену кальцитонина, обладающий мощным сосудорасширяющим действием, также был обнаружен в паравертебральных симпатических нейронах.
Парасимпатическая нервная система
Парасимпатические волокна выходят из ЦНС через черепно-мозговые нервы (ЧН) III, VII, IX и X, а также через нервные корешки S2-4. Есть четыре пары парасимпатических ганглиев, и все они расположены в голове. CN III через цилиарный ганглий иннервирует радужную оболочку и ресничные мышцы глаза. CN VII иннервирует слезные, носовые, небные и глоточные железы через крылонебный ганглий, а также подъязычную и поднижнечелюстную железы через поднижнечелюстной ганглий. CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
CN IX иннервирует околоушные железы через слуховой ганглий. Синапсы всех остальных пресинаптических парасимпатических волокон в ганглиях вблизи или на стенке ткани-мишени; это приводит к тому, что пресинаптические волокна значительно длиннее постсинаптических. Расположение этих ганглиев дало ПНС ее название: «пара-» означает рядом с, следовательно, «парасимпатическим». большая часть органов грудной и брюшной полости, а крестцовые парасимпатические волокна иннервируют нисходящую и сигмовидную кишку и прямую кишку. Блуждающий нерв состоит из четырех клеточных тел в продолговатом мозге. К ним относятся следующие[2][4][30][31]:
Дорсальное ядро: обеспечивает парасимпатический выход к внутренним органам
Спинальное ядро тройничного нерва: получает информацию о прикосновении, боли и температуре наружного уха, слизистой оболочки гортани и части твердой мозговой оболочки
Кроме того, блуждающий нерв проводит сенсорную информацию от барорецепторов каротидного синуса и дуги аорты к мозговому веществу. [32]
[32]
Как упоминалось во введении, блуждающий нерв отвечает за процессы «отдыха и переваривания». Блуждающий нерв способствует сердечной релаксации в нескольких аспектах функции. Он снижает сократительную способность предсердий и в меньшей степени желудочков. Прежде всего, он снижает скорость проведения через атриовентрикулярный узел. Именно благодаря этому механизму массаж каротидного синуса ограничивает повторный вход при синдроме Вольфа-Паркинсона-Уайта.[2] Другая ключевая функция ПНС связана с пищеварением. Парасимпатические волокна, идущие к голове, способствуют слюноотделению, а те, которые соединяются с ЭНС, приводят к усилению перистальтической и секреторной активности.[4][33] Блуждающий нерв также оказывает значительное влияние на дыхательный цикл. В непатологическом состоянии парасимпатические нервы возбуждаются во время выдоха, сокращая и напрягая дыхательные пути, чтобы предотвратить коллапс. Эта функция связана с ПНС в возникновении послеоперационного острого респираторного дистресс-синдрома. [2][21]
[2][21]
Из-за широкой природы блуждающего нерва он был описан как идеальная «система раннего предупреждения» для чужеродных захватчиков, а также для наблюдения за восстановлением организма. До 80% волокон блуждающего нерва являются чувствительными и иннервируют почти все основные органы. Было обнаружено, что парасимпатические ганглии экспрессируют рецепторы интерлейкина-1, ключевого цитокина в воспалительном иммунном ответе.[34] Это, в свою очередь, активирует гипоталамо-гипофизарно-надпочечниковую ось и СНС, что приводит к высвобождению глюкокортикоидов и НЭ соответственно.[2] Исследования коррелируют ингибирование действия блуждающего нерва посредством ваготомии и холинергических ингибиторов со значительно сниженными, если не полностью устраненными, аллергическими, астматическими и воспалительными реакциями.[7]
Постганглионарные парасимпатические нейроны высвобождают АХ, который действует на мускариновые и никотиновые рецепторы, каждый из которых имеет различные субъединицы: M1, M2 и M3, а также N1 и N2, где «M» и «N» обозначают мускарин и никотин соответственно. [5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
[5] ] Постганглионарные рецепторы АХ и рецепторы мозгового вещества надпочечников относятся к N-типу, тогда как парасимпатические эффекторы и потовые железы относятся к М-типу [2]. Как и в симпатических нейронах, несколько пептидов, таких как вазоактивный кишечный пептид (VIP), нейропептид Y (NPY) и пептид, связанный с геном кальцитонина (CGRP), экспрессируются в парасимпатических нейронах и высвобождаются из них. 35][36] Для получения дополнительной информации см. статью StatPearls о холинергических рецепторах здесь.[37]
Кишечная нервная система (ENS)
ЭНС состоит из двух ганглиозных сплетений: мышечно-кишечного (Ауэрбаха) и подслизистого (Мейснера). Межмышечное сплетение находится между продольной и круговой гладкой мускулатурой желудочно-кишечного тракта, а подслизистое сплетение находится в подслизистой оболочке. ЭНС самодостаточна, функционирует за счет локальной рефлекторной активности, но часто получает информацию от СНС и ПНС и обеспечивает обратную связь с ними. ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
ЭНС может получать входные данные от постганглионарных симпатических нейронов или преганглионарных парасимпатических нейронов.
Подслизистое сплетение регулирует движение воды и электролитов через стенку кишечника, в то время как мышечно-кишечное сплетение координирует сократительную способность циркулярных и продольных мышечных клеток кишечника для обеспечения перистальтики.[39]
Подвижность в ЭНС обеспечивается рефлекторной цепью, включающей круговые и продольные мышцы. Никотиновые синапсы между интернейронами опосредуют рефлекторные цепи.[39] Когда цепь активируется присутствием болюса, возбуждающие нейроны в круговой мышце и тормозные нейроны в продольной мышце возбуждаются, создавая узкий участок кишечника проксимальнее болюса; это известно как пропульсивный сегмент. Одновременно возбуждающие нейроны в продольных мышцах и тормозные нейроны в круговых мышцах возбуждают «воспринимающий сегмент» кишечника, в котором будет продолжаться болюс. Этот процесс повторяется с каждым последующим отделом кишечника. [40]
[40]
ENS имеет некоторые сходства с CNS. Как и в ЦНС, кишечные нейроны могут быть биполярными, псевдоуниполярными и мультиполярными, между которыми осуществляется нейромодуляция посредством возбуждающей и тормозной связи.[1] Точно так же нейроны ЭНС используют более 30 нейротрансмиттеров, которые аналогичны нейротрансмиттерам ЦНС, причем наиболее распространенными являются холинергические и нитрергические передатчики.
Хотя большая часть этого обсуждения была сосредоточена на эфферентных функциях ВНС, афферентные волокна отвечают за многочисленные рефлекторные действия, которые регулируют все, от частоты сердечных сокращений до иммунной системы. Обратная связь от ВНС обычно обрабатывается на подсознательном уровне для создания рефлекторных действий в висцеральных или соматических частях тела. Сознательное ощущение во внутренних органах часто интерпретируется как разлитая боль или спазмы, которые могут коррелировать с чувством голода, полноты или тошноты. Эти ощущения чаще всего возникают в результате внезапного растяжения/сокращения, химических раздражителей или патологических состояний, таких как ишемия. [41]
[41]
Эмбриология
Периферическая нервная система происходит из клеток нервного гребня. Нервный гребень аксиально делится на краниальные, блуждающие, туловищные и пояснично-крестцовые клетки нервного гребня. Клетки ствола нервного гребня вносят вклад в дорсальные корешки спинного мозга и симпатические ганглии. Парасимпатическая иннервация сердца формируется из блуждающего нервного гребня. Было показано, что большая часть парасимпатической нервной системы, включая все ганглии головы, возникает из глиальных клеток, а не из клеток нервного гребня.[42][43]
ЭНС происходит из блуждающего нервного гребня с клетками, которые мигрируют рострально-каудально через кишечную стенку, образуя сеть глии и нейронов различных подтипов. Клетки ЭНС завершают свою миграцию к 4-7 неделям развития и экспрессируют все разновидности нейротрансмиттеров ЭНС к 24-й неделе беременности. Однако моторика зрелого кишечника не реализуется, по крайней мере, до поздних сроков беременности или вскоре после рождения.
Хирургические аспекты
Синдром Горнера — это мягкое, редкое состояние, часто проявляющееся односторонним птозом, суженным, но реактивным зрачком и лицевым ангидрозом, вторичным по отношению к повреждению симпатического нерва в окулосимпатическом пути.[46] Это повреждение может иметь центральную причину, такую как инфаркт латерального продолговатого мозга, или периферическую, такую как повреждение, вторичное по отношению к торакальной хирургии или частичной/тотальной резекции щитовидной железы.[46][47] Более централизованные поражения, как правило, коррелируют с комплексом симптомов, включающим синдром Горнера.[46] Для получения дополнительной информации см. соответствующие статьи StatPearls здесь.[48][49]]
Гипергидроз — распространенное заболевание, характеризующееся повышенной потливостью, преимущественно лица, ладоней, подошв и/или подмышечных впадин. Хотя причина первичного гипергидроза до конца не выяснена, его связывают с повышенной холинергической стимуляцией. Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Лечение может быть клиническим или хирургическим.[50] Лечение с клинической точки зрения сосредоточено на антихолинергических средствах, таких как местный гликопирролат или пероральный оксибутинин, или, реже, на альфа-адренергических агонистах, таких как клонидин, блокаторы кальциевых каналов или габапентин. Наиболее распространенным и постоянным хирургическим методом является резекция, абляция или клипирование грудной симпатической цепи. Несмотря на то, что эта процедура необратима, у небольшого числа людей она может привести к компенсаторному гипергидрозу. Эти симптомы гипергидроза такие же, если не более тяжелые, чем до процедуры, из-за возможной гиперкомпенсации гипоталамусом. Исследования показали, что хирургическая реконструкция симпатической цепи может уменьшить эту компенсаторную реакцию.[52]
Клиническое значение
Из-за экстенсивного характера вегетативной нервной системы на нее может влиять широкий спектр состояний. Некоторые из них включают[53][54][55]
Унаследованные
Приобретен
Диабет-сахарный0003
Инфекции: ботулизм, болезнь Шагаса, ВИЧ, проказа, болезнь Лайма, столбняка
Аутоиммунный: Гийен-Барре, Ламберт-Этотонский миастеник-синдром 900.
 0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами ЛевиНеоплазия: опухоли головного мозга, паранеопластические синдромы
Аналогичным образом вегетативная невропатия может проявляться почти в любой системе. Ортостатическая гипотензия является наиболее распространенной вегетативной дизавтономией, но могут присутствовать и многие другие, менее изученные симптомы [53] 9.0003
Сердечно-сосудистые
Желудочно-кишечные
Дисфагия
Запоры
7 Тошнота, рвота, полноту брюшной полости
Genitourinary
PUPDDER ATONONY
9967
PUPLDER ATONONY
PUPLDER ATONONY
79967PUPLDER ATONONY
7067PUPLDER
9.
PUPLDER
.0003
Decreased pupil size
Sexual
Erectile dysfunction
Retrograde ejaculation
Sudomotor
Anhidrosis
Gustatory sweating
Вазомоторный
Похолодание конечностей (из-за потери вазомоторных реакций)
Отек (из-за потери вазомоторного тонуса и повышения проницаемости сосудов)
Наиболее распространенными симптомами ортостатической гипотензии являются головокружение, туннельное зрение и дискомфорт в голове, шее или груди. Она может проявляться одновременно с артериальной гипертензией в положении лежа из-за повышенного периферического сопротивления, что вызывает натрийурез, усугубляющий ортостатическую гипотензию. Существует множество других, более мягких стимулов, которые могут либо снижать артериальное давление (стоя, еда, Вальсальва, обезвоживание, физические упражнения, гипервентиляция и т. д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
д.), либо повышать артериальное давление (лежа на спине, прием воды, кофе, наклон головы вниз, гиповентиляция и т. д.). и др.).[53]
Оценку ортостатической гипотензии обычно проводят с помощью ортостатического тестирования путем повторного измерения артериального давления и частоты сердечных сокращений в положении лежа и стоя, а также с помощью теста с наклонным столом. Однако преимущество этого последнего теста минимально по сравнению с ортостатическим тестом, при этом основным преимуществом является безопасность и удобство для пациента.
Пациенты с дизавтономией склонны к гипотонии во время анестезии[56]. Эту проблему можно надлежащим образом решить с помощью низких доз фенилэфрина, агониста альфа-1. Точно так же гипертонию в положении лежа можно контролировать с помощью трансдермальных или внутривенных нитратов. [53, 57, 58].
Известно, что симпатическая нервная система играет роль в ноцицепции. Есть предположения, что ВНС оказывает регуляторно-тормозное влияние на боль, утрата которого создает цепь положительной обратной связи, приводящую к гипервозбудимости ноцицептивных нервных волокон. Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Тот факт, что эффект симпатической блокады часто сохраняется после продолжительности действия анестетиков, подтверждает эту гипотезу.[59] Местные блокады симпатических нервов использовались для лечения различных менее распространенных болевых состояний, включая комплексный регионарный болевой синдром, фантомную боль в конечностях и герпетическую боль. Точно так же висцеральную боль можно лечить более центральным доступом через блокаду чревного сплетения. Из-за широкого спектра функций, выполняемых ВНС, блокады зарезервированы для непреодолимой боли, не контролируемой более традиционными анальгетиками.] Дополнительную информацию см. в соответствующих статьях StatPearls здесь.[60][61][62]
Большинство состояний, связанных с ЭНС, имеют врожденное происхождение и проявляются в раннем детстве.[44] Энтеральные нейроны расслабляют гладкую мускулатуру кишечника. Их отсутствие приводит к тоническому сокращению кишечника, что приводит к непроходимости кишечника. К предъявляемым жалобам часто относятся гастроэзофагеальный рефлюкс, диспептические синдромы, запоры, хронические боли в животе, синдром раздраженного кишечника. Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Заметным опасным для жизни нарушением ЭНС является болезнь Гиршпрунга. Это состояние представляет собой неспособность эмбриологических клеток ЭНС колонизировать дистальный отдел кишечника. Когда ЭНС отсутствует (аганглиоз) или недоразвита, у детей возникают ранние запоры, рвота, возможная задержка роста и возможная смерть.[3][44] Исследования выявили шесть генов в причинно-следственной связи с болезнью Гиршпрунга.[44] Синдром Дауна является наиболее распространенным генетическим заболеванием, которое предрасполагает человека к болезни Гиршпрунга, несмотря на то, что гены, связанные с развитием ЭНС, не были идентифицированы на хромосоме 21. [3]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Схема вегетативной нервной системы. Предоставлено Генри Греем (1918 г.): Анатомия человеческого тела
Ссылки
- 1.

Стернини С. Организация периферической нервной системы: вегетативные и сенсорные ганглии. J Investig Dermatol Symp Proc. 1997 авг.; 2(1):1–7. [PubMed: 9487007]
- 2.
Каремакер Дж.М. Введение в вегетативную нервную функцию. Физиол Изм. 2017 Май; 38 (5): R89-R118. [PubMed: 28304283]
- 3.
Lake JI, Heuckeroth RO. Развитие энтеральной нервной системы: миграция, дифференцировка и заболевание. Am J Physiol Gastrointest Liver Physiol. 01 июля 2013 г.; 305(1):G1-24. [Бесплатная статья PMC: PMC3725693] [PubMed: 23639815]
- 4.
Siéssere S, Vitti M, Sousa LG, Semprini M, Iyomasa MM, Regalo SC. Анатомическая вариация краниальных парасимпатических ганглиев. Браз Орал Рез. 2008 г., апрель-июнь; 22(2):101-5. [В паблике: 18622477]
- 5.
Купман Ф.А., Стооф С.П., Штрауб Р.Х., Ван Маанен М.А., Верворделдонк М.Дж., Так Р.П. Восстановление баланса вегетативной нервной системы как инновационный подход к лечению ревматоидного артрита.
 Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]
Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]- 6.
Kenney MJ, Ganta CK. Взаимодействие вегетативной нервной системы и иммунной системы. сост. физиол. 2014 июль;4(3):1177-200. [Бесплатная статья PMC: PMC4374437] [PubMed: 24944034]
- 7.
Скотт Г.Д., Фрайер А.Д. Роль парасимпатических нервов и мускариновых рецепторов при аллергии и астме. Хим Иммунол Аллергия. 2012;98:48-69. [Бесплатная статья PMC: PMC4039300] [PubMed: 22767057]
- 8.
McConalogue K, Furness JB. Нейротрансмиттеры желудочно-кишечного тракта. Baillieres Clin Endocrinol Metab. 1994 г., январь; 8 (1): 51–76. [PubMed: 7
3]
- 9.
Шихан Д., Пик Дж. Соединительные ветви у макак-резусов. Дж Анат. 1943 января; 77 (часть 2): 125–39. [PMC бесплатная статья: PMC1252749] [PubMed: 17104919]
- 10.
Лукас М., Клаассен З., Мербс В., Таббс Р.С., Гелецкий Дж.
 , Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]
, Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]- 11.
Ян Х.Дж., Гил Ю.К., Ли В.Дж., Ким Т.Дж., Ли Х.И. Анатомия грудных внутренностных нервов для хирургической резекции. Клин Анат. 2008 март; 21(2):171-7. [PubMed: 18288763]
- 12.
Беверидж Т.С., Джонсон М., Пауэр А, Пауэр Н.Е., Оллман Б.Л. Анатомия нервов и ганглиев аортального сплетения у мужчин. Дж Анат. 2015 Январь; 226 (1): 93-103. [Бесплатная статья PMC: PMC4313893] [PubMed: 25382240]
- 13.
Ehrhardt JD, Weber C, Lopez-Ojeda W. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Анатомия, грудная клетка, большие внутренностные нервы. [PubMed: 29763202]
- 14.
Бриндли Р.Л., Бауэр М.Б., Блейкли Р.Д., Карри КПМ. Серотонин и переносчики серотонина в мозговом веществе надпочечников: потенциальный узел для модуляции симпатической реакции на стресс.
 ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]
ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]- 15.
Нэнси Д.М., Сандерс В.М. Вегетативная иннервация и регуляция иммунной системы (1987-2007 гг.). Мозг Behav Immun. 2007 авг; 21 (6): 736-45. [Бесплатная статья PMC: PMC1986730] [PubMed: 17467231]
- 16.
Alhayek S, Preuss CV. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Рецепторы бета-1. [PubMed: 30422499]
- 17.
Фарзам К., Кидрон А., Лахкар А.Д. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 18 июля 2021 г. Адренергические препараты. [PubMed: 30480963]
- 18.
Халид М.М., Галуска М.А., Гамильтон Р.Дж. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 26 июля 2021 г. Токсичность бета-блокаторов. [В паблике: 28846217]
- 19.
Хойш Г., Темер В. [Значение симпатической нервной системы для коронарного кровообращения].
 З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]
З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]- 20.
Варгас Пелаес А.Ф., Гао З., Ахмад Т.А., Лойенбергер Ю.А., Проктор Д.Н., Маман С.Р., Мюллер М.Д. Влияние адреномиметиков на коронарный кровоток: лабораторное исследование на здоровых добровольцах. Physiol Rep. 2016 May;4(10) [бесплатная статья PMC: PMC4886172] [PubMed: 27225628]
- 21.
Chen IC, Kuo J, Ko WJ, Shih HC, Kuo CD. Повышенное сопротивление потоку и снижение скорости потока у пациентов с острым респираторным дистресс-синдромом: роль вегетативной нервной модуляции. J Chin Med Assoc. 2016 Январь; 79(1):17-24. [PubMed: 26589196]
- 22.
Штернберг Э.М. Нейронная регуляция врожденного иммунитета: скоординированный неспецифический ответ хозяина на патогены. Нат Рев Иммунол. 2006 апр; 6 (4): 318-28. [Бесплатная статья PMC: PMC1783839] [PubMed: 16557263]
- 23.
Еленков И.Ю., Уайлдер Р.Л., Хрусос Г.П., Визи Э.С. Симпатический нерв — интегративный интерфейс между двумя надсистемами: мозгом и иммунной системой.
 Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]
Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]- 24.
Bellinger DL, Millar BA, Perez S, Carter J, Wood C, ThyagaRajan S, Molinaro C, Lubahn C, Lorton D. Симпатическая модуляция иммунитета: отношение к болезни. Клеточный Иммунол. 2008 март-апрель; 252(1-2):27-56. [Бесплатная статья PMC: PMC3551630] [PubMed: 18308299]
- 25.
Лундберг Дж. М., Хёкфельт Т. Множественное сосуществование пептидов и классических передатчиков в периферических вегетативных и сенсорных нейронах — функциональные и фармакологические последствия. Прог Мозг Res. 1986;68:241-62. [PubMed: 2882554]
- 26.
Лундберг Дж.М., Хёкфельт Т., Шульцберг М., Увнес-Валленстен К., Келер С., Саид С.И. Возникновение иммунореактивности, подобной вазоактивному кишечному полипептиду (ВИП), в некоторых холинергических нейронах кошки: данные комбинированной иммуногистохимии и окрашивания ацетилхолинэстеразой. Неврология. 1979;4(11):1539-59. [PubMed: 3
]- 27.

Landis SC, Fredieu JR. Сосуществование пептида, родственного гену кальцитонина, и вазоактивного интестинального пептида в холинергической симпатической иннервации потовых желез крыс. Мозг Res. 1986 г., 02 июля; 377 (1): 177–81. [PubMed: 3524749]
- 28.
Lindh B, Lundberg JM, Hökfelt T, Elfvin LG, Fahrenkrug J, Fischer J. Сосуществование CGRP- и VIP-подобных иммунореактивностей в популяции нейронов звездчатых ганглиев кошек . Acta Physiol Scand. 1987 ноября; 131 (3): 475-6. [PubMed: 3321916]
- 29.
Brain SD, Williams TJ, Tippins JR, Morris HR, MacIntyre I. Пептид, родственный гену кальцитонина, является мощным сосудорасширяющим средством. Природа. 1985 г., 3–9 января; 313 (5997): 54–6. [PubMed: 3
4]- 30.
Berthoud HR, Neuhuber WL. Функциональная и химическая анатомия афферентной системы блуждающего нерва. Автон Нейроски. 2000 г., 20 декабря; 85 (1–3): 1–17. [PubMed: 11189015]
- 31.

Павлов В.А., Ван Х., Чура С.Дж., Фридман С.Г., Трейси К.Дж. Холинергический противовоспалительный путь: недостающее звено в нейроиммуномодуляции. Мол Мед. 2003 май-август 9(5-8):125-34. [Бесплатная статья PMC: PMC1430829] [PubMed: 14571320]
- 32.
Цучихаси К., Ёсихиро Т., Айкава Т., Нио К., Такаёси К., Ёкояма Т., Фуката М., Арита С., Арияма Х., Симидзу Й. Yoshida Y, Torisu T, Esaki M, Odashiro K, Kusaba H, Akashi K, Baba E. Метастатический рак пищевода, представляющий собой шок от повреждения блуждающего нерва, имитирующего барорецепторный рефлекс: клинический случай. Медицина (Балтимор). 2017 Декабрь;96(49):e8987. [Бесплатная статья PMC: PMC5728886] [PubMed: 271]
- 33.
Вуд JD. Применение классификационных схем к энтеральной нервной системе. J Auton Nerv Syst. 1994 г., июнь; 48 (1): 17–29. [PubMed: 8027516]
- 34.
Thayer JF, Sternberg EM. Невральные аспекты иммуномодуляции: фокус на блуждающий нерв.
 Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]
Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]- 35.
Лундберг Дж. М., Хёкфельт Т., Ангард А., Увнес-Валленстен К., Бримиджоин С., Бродин Э., Фаренкруг Дж. Периферийное распределение аксона: транспорт и некоторые аспекты возможного функционирования. Adv Biochem Psychopharmacol. 1980;22:25-36. [PubMed: 6156578]
- 36.
Leblanc GG, Trimmer BA, Landis SC. Нейропептид Y-подобная иммунореактивность в черепных парасимпатических нейронах крыс: сосуществование с вазоактивным кишечным пептидом и холин-ацетилтрансферазой. Proc Natl Acad Sci USA. 1987 May; 84(10):3511-5. [Бесплатная статья PMC: PMC304901] [PubMed: 3554241]
- 37.
Carlson AB, Kraus GP. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 23 августа 2021 г. Физиология, холинергические рецепторы. [В паблике: 30252390]
- 38.
Миллион М, Ларош М. Стресс, секс и кишечная нервная система.
 Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]
Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]- 39.
Хансен МБ. Энтеральная нервная система I: организация и классификация. Фармакол Токсикол. 2003 март; 92(3):105-13. [PubMed: 12753424]
- 40.
Вуд JD. Энтеральная нервная система: нейропатическая моторика желудочно-кишечного тракта. Dig Dis Sci. 2016 июль; 61 (7): 1803-16. [В паблике: 27142673]
- 41.
Сарна SK. Подвижность толстой кишки: от скамейки к постели. Морган и Клейпул Лайф Сайенсиз; Сан-Рафаэль (Калифорния): 2010. [PubMed: 21452445]
- 42.
Батлер С.Дж., Броннер М.Э. От классики к современности: анализ происхождения и судьбы периферической нервной системы и спинного мозга. Дев биол. 2015 15 февраля; 398 (2): 135-46. [Бесплатная статья PMC: PMC4845735] [PubMed: 25446276]
- 43.
Дьячук В., Фурлан А., Шахиди М.К., Джовенко М., Каукуа Н.
 , Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]
, Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]- 44.
Gariepy CE. Нарушения моторики кишечника и развитие энтеральной нервной системы. Педиатр рез. 2001 г., май; 49(5):605-13. [PubMed: 11328941]
- 45.
Сасселли В., Пахнис В., Бернс А.Дж. Энтеральная нервная система. Дев биол. 01 июня 2012 г .; 366 (1): 64–73. [PubMed: 222
]- 46.
Канагалингам С., Миллер Н.Р. Синдром Горнера: клинические перспективы. Глазной мозг. 2015;7:35-46. [Бесплатная статья PMC: PMC5398733] [PubMed: 28539793]
- 47.
Diamantis E, Farmaki P, Savvanis S, Athanasiadis G, Troupis T, Damaskos C. Повреждение симпатического нерва при раке щитовидной железы. Acta Medica (Градец Кралове).
 2017;60(4):135-139. [PubMed: 29716678]
2017;60(4):135-139. [PubMed: 29716678]- 48.
Хан З., Боллу ПК. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 4 мая 2021 г. Синдром Хорнера. [PubMed: 29763176]
- 49.
Lykstad J, Reddy V, Hanna A. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, путь расширения зрачков. [В паблике: 30571042]
- 50.
Делорт С., Марчи Э., Корреа М.А. Оксибутинин как альтернативное лечение гипергидроза. Бюстгальтеры Дерматол. 2017 март-апрель;92(2):217-220. [Бесплатная статья PMC: PMC5429108] [PubMed: 28538882]
- 51.
del Boz J. Системное лечение гипергидроза. Actas Дермосифилиогр. 2015 май; 106(4):271-7. [PubMed: 25638324]
- 52.
Haam SJ, Park SY, Paik HC, Lee DY. Реконструкция симпатического нерва при компенсаторном гипергидрозе после симпатической операции по поводу первичного гипергидроза.
 J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]
J Korean Med Sci. 2010 апр;25(4):597-601. [Бесплатная статья PMC: PMC2844605] [PubMed: 20358004]- 53.
Mustafa HI, Fessel JP, Barwise J, Shannon JR, Raj SR, Diedrich A, Biaggioni I, Robertson D. Dysautonomia: периоперационные последствия. Анестезиология. 2012 Январь; 116 (1): 205-15. [Бесплатная статья PMC: PMC3296831] [PubMed: 22143168]
- 54.
McLeod JG. Исследование периферической нейропатии. J Neurol Нейрохирург Психиатрия. 1995 март; 58(3):274-83. [Бесплатная статья PMC: PMC1073360] [PubMed: 7897405]
- 55.
Ludwig PE, Reddy V, Varacallo M. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 11 августа 2021 г. Нейроанатомия, центральная нервная система (ЦНС) [PubMed: 28723039]
- 56.
Санчес-Мансо Дж. К., Гуджарати Р., Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 октября 2021 г. Вегетативная дисфункция. [PubMed: 28613638]
- 57.

Беван Д.Р. Синдром Шай-Дрейгера. Обзор и описание анестезиологического обеспечения. Анестезия. 1979 октября; 34 (9): 866-73. [PubMed: 532923]
- 58.
Stirt JA, Frantz RA, Gunz EF, Conolly ME. Анестезия, катехоламины и гемодинамика при вегетативной дисфункции. Анест Анальг. 1982 г., август; 61 (8): 701-4. [PubMed: 7201274]
- 59.
Gunduz OH, Kenis-Coskun O. Блокада ганглиев как лечение боли: текущие перспективы. Джей Боль Рез. 2017;10:2815-2826. [Бесплатная статья PMC: PMC5734237] [PubMed: 2
02]
- 60.
Джон Р.С., Диксон Б., Шиенбаум Р. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 31 июля 2021 г. Блокада чревного сплетения. [PubMed: 30285364]
- 61.
Пираччини Э., Мунакоми С., Чанг К.В. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 9 августа 2021 г. Блоки звездчатого ганглия. [PubMed: 29939575]
- 62.

Александр К.Э., Де Хесус О, Варакалло М. StatPearls [Интернет]. Издательство StatPearls; Остров сокровищ (Флорида): 30 августа 2021 г. Симпатическая блокада поясничного отдела. [В паблике: 28613759]
Copyright © 2022, StatPearls Publishing LLC.
Эта книга распространяется в соответствии с международной лицензией Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает использование, дублирование, адаптацию, распространение и воспроизведение на любом носителе или формате, при условии, что вы укажете автора(ов) оригинала и источник, будет дана ссылка на лицензию Creative Commons и указаны любые внесенные изменения.
Идентификатор книжной полки: NBK539845PMID: 30969667
Вегетативная нервная система — Scholarpedia
Bill Blessing and Ian Gibbins (2008), Scholarpedia, 3(7):2787. | doi:10.4249/scholarpedia.2787 | , редакция № 150512 [ссылка на эту статью/цитирование этой статьи] |
Постпубликационная деятельность
Куратор: Ян Гиббинс
Авторы:
0,43 —
Билл Блессинг
0,29 —
Ижикевич Евгений Михайлович
0,14 —
Бенджамин Броннер
0,07 —
Мишель Л. Джонс
Джон Б. Фернесс
Шривас Ченну
Джон Хорн
Д-р Билл Блессинг, Центр неврологии, Университет Флиндерс, Аделаида, АВСТРАЛИЯ
Проф. Ян Гиббинс, Центр неврологии, Университет Флиндерс, Аделаида, Южная Австралия, Австралия
Рисунок 1: Краткий обзор симпатических (А) и парасимпатических (В) вегетативных нервных оттоков из центральной нервной системы. Рисунок, нарисованный авторами, включает материалы из Gray’s Anatomy 31st Edition 1954 и из Cannon and Rosenblueth Physiology of the Autonomic Nervous System , 1937.
Рисунок, нарисованный авторами, включает материалы из Gray’s Anatomy 31st Edition 1954 и из Cannon and Rosenblueth Physiology of the Autonomic Nervous System , 1937.
нейроны (ганглии), расположенные в голове, шее, грудной клетке, брюшной полости и тазу, и к аксональным соединениям этих нейронов (рис. 1). Вегетативные пути вместе с соматическими двигательными путями к скелетным мышцам и нейроэндокринными путями являются средствами, с помощью которых центральная нервная система (ЦНС) посылает команды остальному телу. Существуют также компоненты ЦНС ВНС, в том числе стволовые и спинальные вегетативные преганглионарные нейроны, которые проецируются на вегетативные двигательные нейроны в периферических ганглиях. В этом отношении преганглионарные вегетативные мотонейроны четко отличаются от соматических мотонейронов, которые проецируются из ЦНС непосредственно в иннервируемую ткань (скелетные мышцы) без промежуточных ганглиев.
Постганглионарные аксональные отростки мотонейронов вегетативных ганглиев иннервируют органы и ткани по всему телу (глаза, слюнные железы, сердце, желудок, мочевой пузырь, сосуды и др. ). Моторные нейроны вегетативных ганглиев иногда называют «постганглионарными нейронами». Эта традиционная терминология сбивает с толку, и мы используем термин «автономные мотонейроны» или «конечные мотонейроны» для ганглиозных клеток.
). Моторные нейроны вегетативных ганглиев иногда называют «постганглионарными нейронами». Эта традиционная терминология сбивает с толку, и мы используем термин «автономные мотонейроны» или «конечные мотонейроны» для ганглиозных клеток.
Комплекс вегетативных ганглиев в стенках желудка и тонкой кишки отдельно классифицируется как энтеральная нервная система. Большинство нервных путей в энтеральных сплетениях не имеют прямых преганглионарных входов и могут работать независимо от центрального контроля. Действительно, только в ВНС кишечные сплетения содержат первичные сенсорные нейроны, которые соединяются с обширными сетями интернейронов, а также возбуждающие и тормозящие кишечные моторные нейроны.
Содержимое
|
История определения и функциональной концепции ВНС
Эмоциональное чувство традиционно считалось отличным от рационального мышления. Мозг, запертый в своем костяном футляре, считался ответственным за рациональное мышление и за идеи, управляющие поведенческими взаимодействиями с внешней средой. Эмоции, скорее висцеральные, чем рациональные, были связаны с функциями внутренних органов тела. У нас есть «интуитивные чувства», сердце — это «место любви», и мы «выпускаем нашу селезенку». Биша (1771-1802) разделил жизнь на две отдельные формы, одна из которых (реляционная жизнь) управляется мозгом, а другая (органическая, вегетативная жизнь) — ганглиями брюшной полости. Вегетативная жизнь рассматривалась как связанная со страстями и независимая от образования, управляемая самостоятельно функционирующими брюшными ганглиями, цепью «маленьких мозгов». Филипп Пинель, один из основателей психиатрии и учитель Биша, даже считал, что психические заболевания вызываются аномальной функцией этих ганглиев, а современная психиатрия до сих пор ссылается на «вегетативные функции».
Лэнгли (1852-1925) ввел термин вегетативная нервная система. Лэнгли отметил отсутствие чувствительных (афферентных) тел нервных клеток в вегетативных ганглиях и определил ВНС как чисто двигательную систему. Тем не менее, он продолжил традицию, в соответствии с которой ВНС рассматривается как функционирующая сама по себе, независимая от ЦНС. Следует отметить, что Лэнгли не полностью придерживался этого упрощения. Во введении к ВНС (1903) он писал, что можно «рассматривать как афферентные вегетативные волокна те, которые вызывают рефлексы в вегетативных тканях и которые не способны непосредственно давать начало ощущениям». Более того, открытие первичных афферентных нейронов, которые являются частью ВНС, но полностью лежат вне ЦНС и не имеют прямой связи с ЦНС, затрудняет представление ВНС как полностью эфферентной системы (Furness 2006; см. далее). ниже).
Современные эксперименты показали, что нейроны вегетативных ганглиев не имеют встроенных паттернов разряда, достаточно интегрированных для регуляции физиологических функций, за возможным исключением нейронов энтеральной нервной системы тонкого и толстого кишечника. Классическое описание гексаметония человека резюмирует состояние человека после лекарственно-опосредованного выведения ВНС из-под функционального контроля со стороны головного мозга. Точно так же, когда мозговой контроль спинальных вегетативных преганглионарных нейронов удаляется (как при квадриплегии), сердечно-сосудистые функции, функции кишечника и мочевого пузыря серьезно нарушаются. Таким образом, ВНС лучше всего рассматривать как один из оттоков, посредством которых ЦНС контролирует органы тела, так что термин «периферические вегетативные пути» является более подходящим, но термин «вегетативная нервная система» является общепринятым.
Классическое описание гексаметония человека резюмирует состояние человека после лекарственно-опосредованного выведения ВНС из-под функционального контроля со стороны головного мозга. Точно так же, когда мозговой контроль спинальных вегетативных преганглионарных нейронов удаляется (как при квадриплегии), сердечно-сосудистые функции, функции кишечника и мочевого пузыря серьезно нарушаются. Таким образом, ВНС лучше всего рассматривать как один из оттоков, посредством которых ЦНС контролирует органы тела, так что термин «периферические вегетативные пути» является более подходящим, но термин «вегетативная нервная система» является общепринятым.
Пути ВНС делятся на симпатические и парасимпатические (вокруг симпатических) отделы и кишечные сплетения. Тела преганглионарных клеток симпатического оттока находятся в грудном отделе спинного мозга. Тела преганглионарных клеток для парасимпатического оттока находятся в стволе головного мозга (краниальные) и в крестцовом отделе спинного мозга (крестцовые). Представление о том, что подразделения противостоят друг другу, является вводящим в заблуждение упрощением. Ни одно из подразделений никогда не активируется целиком. Скорее, каждое подразделение состоит из ряда дискретных функциональных путей, которые могут активироваться из ЦНС либо независимо, либо по схемам, в соответствии с конкретными требованиями конкретной повседневной деятельности, которая способствует гомеостазу организма. Приоритет интегративного контроля мозга над всеми телесными функциями был признан Уолтером Кэнноном, но его идея о том, что мозг диффузно и неспецифически активирует симпатические нервы во время телесных чрезвычайных ситуаций («реакция борьбы или бегства»), является чрезмерным упрощением. Разные экстренные состояния требуют разных паттернов вегетативной активности, и нормальная повседневная жизнь (кроме чрезвычайных ситуаций) также требует паттернов вегетативной активности. Индивидуум функционирует как единое целое: есть только одна нервная система.
Представление о том, что подразделения противостоят друг другу, является вводящим в заблуждение упрощением. Ни одно из подразделений никогда не активируется целиком. Скорее, каждое подразделение состоит из ряда дискретных функциональных путей, которые могут активироваться из ЦНС либо независимо, либо по схемам, в соответствии с конкретными требованиями конкретной повседневной деятельности, которая способствует гомеостазу организма. Приоритет интегративного контроля мозга над всеми телесными функциями был признан Уолтером Кэнноном, но его идея о том, что мозг диффузно и неспецифически активирует симпатические нервы во время телесных чрезвычайных ситуаций («реакция борьбы или бегства»), является чрезмерным упрощением. Разные экстренные состояния требуют разных паттернов вегетативной активности, и нормальная повседневная жизнь (кроме чрезвычайных ситуаций) также требует паттернов вегетативной активности. Индивидуум функционирует как единое целое: есть только одна нервная система.
Сенсорная информация (висцеральная афферентная информация), относящаяся к вегетативному контролю (например, степень наполнения мочевого пузыря или уровень артериального давления), проходит по висцеральным афферентным нервам и поступает в ЦНС через спинномозговые афферентные пути или через блуждающие или языкоглоточные афферентные пути, которые проецируются в нижние отделы ствол мозга (см. черные стрелки с белой заливкой на рис. 1).
черные стрелки с белой заливкой на рис. 1).
Вегетативные нейротрансмиттеры
Все преганглионарные вегетативные нейроны, как симпатические, так и парасимпатические, используют ацетилхолин (АХ) в качестве своего быстрого медиатора возбуждения. В ганглиях АХ действует на подкласс никотиновых рецепторов, отличный от никотиновых рецепторов в нервно-мышечном соединении скелетных мышц. Многие преганглионарные вегетативные нейроны также содержат нейропептиды, обычно действующие как ко-трансмиттеры, которые опосредуют медленные возбуждающие постсинаптические потенциалы, облегчая холинергическую передачу.
Большинство симпатических конечных моторных нейронов используют норадреналин (норэпинефрин) в качестве основного медиатора вместе с комедиаторами, такими как аденозинтрифосфат (АТФ) и пептиды, включая нейропептид Y (NPY), галанин, соматостатин или опиоидные пептиды. Некоторые симпатические конечные моторные нейроны (особенно те, которые иннервируют потовые железы) используют АХ в качестве своего основного непептидного передатчика. Парасимпатические конечные пути двигательных нейронов обычно используют АХ, оксид азота или оба в качестве непептидных передатчиков, а также широкий спектр пептидов-котрансмиттеров, включая вазоактивный интестинальный пептид (VIP), пептид, родственный гену кальцитонина (CGRP), соматостатин и опиоидные пептиды. Никакие парасимпатические нейроны не используют норадреналин в качестве передатчика. АХ также является основным возбуждающим передатчиком, используемым кишечными нейронами. Другие энтеральные нейротрансмиттеры включают оксид азота (вероятно, основной тормозной медиатор мышц кишечника), субстанцию P, VIP, энкефалин, серотонин (5-гидрокситриптамин, 5-HT) и АТФ.
Аксоны конечных моторных нейронов разветвляются по тканям-мишеням, обычно гладкой мускулатуре, секреторной ткани или сердечной мышце. Аксонные окончания специализированы для нейротрансмиссии, но обычно им не хватает структур, характерных для обычных синаптических контактов. Многие ткани-мишени иннервируются как симпатическими, так и парасимпатическими нервами (например, сердце, радужная оболочка, некоторые слюнные железы, желудочно-кишечный тракт и органы таза).
Парасимпатические конечные пути двигательных нейронов обычно используют АХ, оксид азота или оба в качестве непептидных передатчиков, а также широкий спектр пептидов-котрансмиттеров, включая вазоактивный интестинальный пептид (VIP), пептид, родственный гену кальцитонина (CGRP), соматостатин и опиоидные пептиды. Никакие парасимпатические нейроны не используют норадреналин в качестве передатчика. АХ также является основным возбуждающим передатчиком, используемым кишечными нейронами. Другие энтеральные нейротрансмиттеры включают оксид азота (вероятно, основной тормозной медиатор мышц кишечника), субстанцию P, VIP, энкефалин, серотонин (5-гидрокситриптамин, 5-HT) и АТФ.
Аксоны конечных моторных нейронов разветвляются по тканям-мишеням, обычно гладкой мускулатуре, секреторной ткани или сердечной мышце. Аксонные окончания специализированы для нейротрансмиссии, но обычно им не хватает структур, характерных для обычных синаптических контактов. Многие ткани-мишени иннервируются как симпатическими, так и парасимпатическими нервами (например, сердце, радужная оболочка, некоторые слюнные железы, желудочно-кишечный тракт и органы таза).
Краниальные парасимпатические пути
Краниальные парасимпатические пути проецируются на широкий спектр целей в голове, шее, грудной клетке и брюшной полости (рис. 1). Пути связаны с четырьмя черепными нервами: глазодвигательным (III), лицевым (VII), языкоглоточным (IX) и блуждающим (X). Большинство конечных мотонейронов в этих краниальных вегетативных путях находится в четырех парах основных ганглиев: цилиарных ганглиях (III), клиновидно-небных или крылонебных ганглиях (VII), поднижнечелюстных ганглиях (VII) и слуховых ганглиях (IX). Конечные мотонейроны вагусных вегетативных путей лежат в основном в микроганглиях, расположенных вблизи органов-мишеней или внутри них.
Основной мишенью краниальных парасимпатических путей являются секреторные железы, связанные с глазами (слезы), ртом (слюна) и носом (слизь). Они стимулируют секрецию водянистой жидкости, часто с сопутствующей вазодилатацией. Парасимпатические пути также играют важную роль в фокусировке глаза и регулировании диаметра зрачка. Кровеносные сосуды в головном мозге также получают парасимпатическую сосудорасширяющую иннервацию, но реальная физиологическая функция этих нервов изучена недостаточно.
Блуждающий нерв иннервирует микроганглии шеи, грудной клетки и брюшной полости, включая дыхательные пути, сердце, щитовидную железу, поджелудочную железу, желчный пузырь и верхние отделы желудочно-кишечного тракта. Следовательно, блуждающий нерв имеет широкий спектр действий. Он изменяет сопротивление воздушному потоку и увеличивает секрецию слизи из верхних дыхательных путей; замедляет сердце; стимулирует секрецию пищеварительных ферментов и бикарбоната поджелудочной железой; он либо увеличивает, либо снижает как секреторную активность, так и сократимость гладкой мускулатуры желудка.
Некоторые парасимпатические пути имеют тенденцию быть тонически активными (например, пути блуждающего нерва, которые поддерживают низкую частоту сердечных сокращений, когда мы не тренируемся), тогда как другие активируются только при необходимости, например секреция слюны во время еды; расслабление гладкой мускулатуры желудка; или вблизи фокуса глаз при чтении.
Кровеносные сосуды в головном мозге также получают парасимпатическую сосудорасширяющую иннервацию, но реальная физиологическая функция этих нервов изучена недостаточно.
Блуждающий нерв иннервирует микроганглии шеи, грудной клетки и брюшной полости, включая дыхательные пути, сердце, щитовидную железу, поджелудочную железу, желчный пузырь и верхние отделы желудочно-кишечного тракта. Следовательно, блуждающий нерв имеет широкий спектр действий. Он изменяет сопротивление воздушному потоку и увеличивает секрецию слизи из верхних дыхательных путей; замедляет сердце; стимулирует секрецию пищеварительных ферментов и бикарбоната поджелудочной железой; он либо увеличивает, либо снижает как секреторную активность, так и сократимость гладкой мускулатуры желудка.
Некоторые парасимпатические пути имеют тенденцию быть тонически активными (например, пути блуждающего нерва, которые поддерживают низкую частоту сердечных сокращений, когда мы не тренируемся), тогда как другие активируются только при необходимости, например секреция слюны во время еды; расслабление гладкой мускулатуры желудка; или вблизи фокуса глаз при чтении.
Симпатические пути
Нейроны симпатического отдела вегетативной нервной системы объединены в две основные группы ганглиев: паравертебральные ганглии, образующие симпатическую цепь с каждой стороны позвоночного столба, и превертебральные ганглии, лежащие вокруг начала чревная и брыжеечная артерии (рис. 1). Симпатические нейроны проецируются на большинство тканей тела, обычно достигая их, путешествуя с крупными нервами, содержащими преимущественно чувствительные и соматические двигательные нервные волокна.
Симпатические проводящие пути имеют разнообразный спектр активности. Многие из них активны почти все время, например, сосудосуживающие пути к мышцам, которые поддерживают центральное кровяное давление, сосудосуживающие пути к коже, которые помогают предотвратить чрезмерную потерю тепла, или превертебральные пути к желудочно-кишечному тракту, которые помогают предотвратить чрезмерную потерю воды из кишечника. Другие симпатические пути активируются только по требованию, например те, которые увеличивают частоту сердечных сокращений во время физической нагрузки; судомоторные нейроны, стимулирующие потоотделение при высокой температуре тела; или те, которые стимулируют эякуляцию во время сексуальной активности. В некоторых случаях симпатические и парасимпатические пути к ткани-мишени активируются совместно, например, симпатические пути к слюнным железам активируются совместно с парасимпатическими путями, когда мы едим что-то потенциально вредное, например, острый перец чили. Симпатическая коактивация приводит к образованию более густой и вязкой слюны.
В некоторых случаях симпатические и парасимпатические пути к ткани-мишени активируются совместно, например, симпатические пути к слюнным железам активируются совместно с парасимпатическими путями, когда мы едим что-то потенциально вредное, например, острый перец чили. Симпатическая коактивация приводит к образованию более густой и вязкой слюны.
В норме симпатические пути никогда не активируются одновременно. Несмотря на широко распространенное мнение, что они активируются только во время стрессовых ситуаций, постоянная активность определенных симпатических путей необходима для нашего повседневного здоровья и благополучия. Даже когда мы сталкиваемся с сильным стрессом, задействована будет только часть симпатических путей.
Тазовые вегетативные пути
Регуляция деятельности многих тазовых органов требует скоординированного контроля как симпатическими, так и крестцовыми парасимпатическими путями, часто в сочетании с соответствующими соматическими двигательными путями. Действительно, многие ганглии в тазовых путях содержат смесь нейронов, некоторые из которых получают преганглионарные входы от поясничных уровней спинного мозга (по определению, симпатические), а другие получают преганглионарные входы от крестцовых уровней спинного мозга (по определению, парасимпатические). Некоторые отдельные нейроны получают конвергентные входы как от поясничных, так и от крестцовых преганглионарных нейронов, и их можно считать относящимися как к симпатическим, так и к парасимпатическим путям.
Действительно, многие ганглии в тазовых путях содержат смесь нейронов, некоторые из которых получают преганглионарные входы от поясничных уровней спинного мозга (по определению, симпатические), а другие получают преганглионарные входы от крестцовых уровней спинного мозга (по определению, парасимпатические). Некоторые отдельные нейроны получают конвергентные входы как от поясничных, так и от крестцовых преганглионарных нейронов, и их можно считать относящимися как к симпатическим, так и к парасимпатическим путям.
Контроль функции мочевого пузыря требует симпатической активности для расслабления стенки мочевого пузыря и комбинированной симпатической и соматической двигательной активности для удержания сфинктеров закрытыми во время удержания мочи. Напротив, мочеиспускание (мочеиспускание) включает парасимпатическую активацию для сокращения стенки мочевого пузыря и расслабления сфинктеров, наряду с соматическими двигательными путями для повышения внутрибрюшного давления. Во время сексуальной активности эрекция требует скоординированной активности парасимпатических и соматических путей, в то время как эякуляция является результатом скоординированной симпатической и соматической двигательной активности.
Пути головного и спинного мозга, регулирующие отток вегетативной нервной системы
Преганглионарные нейроны, отвечающие за парасимпатический и симпатический вегетативный отток, расположены в стволе головного мозга, а также в грудном, верхнепоясничном и крестцовом отделах спинного мозга (рис. 1). Несколько разных мозговых центров контролируют эти преганглионарные нейроны. Для симпатического оттока области мозга, содержащие премоторные нейроны, включают продолговатый мозг, мост и гипоталамус. Многие из этих премоторных нейронов синтезируют моноамин (норадреналин, адреналин, дофамин или серотонин). Для парасимпатических оттоков премоторные нейроны встречаются в основном в стволе мозга и гипоталамусе. Сами премоторные нейроны контролируются входами из различных областей мозга, включая другие области ствола мозга и гипоталамуса, миндалевидное тело, базальные ганглии, переднюю поясную кору, островковую кору, зрительные центры и центры префронтальной коры, участвующие в обработке эмоций. , Например.
, Например.
Афферентные входы к вегетативным путям
Почти вся нервная связь от одного органа к другому (например, от кишечника или легких к сердцу) осуществляется через афферентные нейроны с клеточными телами в ганглиях задних корешков (около спинного мозга) или в узловых и каменистых ганглиях нижних черепных нервов (расположены в области шеи), как показано на рис. 1. Эти висцеральные афферентные нейроны имеют центральный отросток, который проецируется в задние рога спинного мозга или в афферентные ядра в стволе головного мозга (например, ядро одиночного пути в дорсальной части продолговатого мозга).
Сначала Лэнгли ожидал найти тела афферентных клеток в вегетативных ганглиях с проекциями на другие ганглии. Он считал, что активация этих «автономных афферентов» должна приводить к чисто вегетативным реакциям. Однако собственная тщательная работа Лэнгли показала, что таких нейронов не существует.
Сложные нейронные сети внутри желудочно-кишечного тракта и тесно связанные с ним, регулируют пищеварительную, всасывающую и выделительную функции. Эта энтеральная нервная система структурно и функционально организована в виде афферентных нейронов, интернейронов и мотонейронов с характерными проекциями и нейрохимическими профилями. Есть некоторые проекции от тел афферентных клеток внутри энтеральной нервной системы к нейронам вегетативных ганглиев, которые проецируются обратно в кишечник, но проекции к другим частям вегетативной нервной системы редки или отсутствуют.
Эта энтеральная нервная система структурно и функционально организована в виде афферентных нейронов, интернейронов и мотонейронов с характерными проекциями и нейрохимическими профилями. Есть некоторые проекции от тел афферентных клеток внутри энтеральной нервной системы к нейронам вегетативных ганглиев, которые проецируются обратно в кишечник, но проекции к другим частям вегетативной нервной системы редки или отсутствуют.
Таким образом, вместо «автономных афферентов» (или симпатических или парасимпатических афферентов) мы предпочитаем термин «висцеральные афференты». Принципиально важным моментом является то, что интегративные процессы, ответственные за организацию висцеральной функции, происходят преимущественно в центральной нервной системе (головной и/или спинной мозг). Как соматические, так и висцеральные афференты приводят к сложным реакциям, опосредованным мозгом, которые включают соматическую и висцеральную функции. Вегетативная двигательная активность может генерироваться как соматическими, так и висцеральными входами в ЦНС, а висцеральные входы в ЦНС инициируют как соматические, так и вегетативные ответы. Естественное телесное функционирование не включает «чисто вегетативные» или «чисто соматические» реакции, так же как оно не включает «чисто симпатические» или «чисто парасимпатические» реакции. Лучше всего иллюстрировать эту мысль примерами.
Естественное телесное функционирование не включает «чисто вегетативные» или «чисто соматические» реакции, так же как оно не включает «чисто симпатические» или «чисто парасимпатические» реакции. Лучше всего иллюстрировать эту мысль примерами.
Ноцицептивные висцеральные афференты (боль от внутренних органов)
Вероятно, все внутренние органы иннервируются немиелинизированными аксонами нейронов ганглиев задних корешков, которые реагируют на ряд вредных раздражителей, таких как воспаление тканей, низкий рН или ишемия. При активации эти болевые афференты производят сознательное восприятие боли, разумно локализованной в органе. Эти висцеральные афферентные нейроны могут вызывать симпатико-опосредованные реакции (например, повышение кровяного давления), но они также активируют соматическую двигательную активность, такую как спазм лицевых мышц (гримасничанье), а также брюшных мышц («сгибание пополам от боли»). и дыхательные мышцы (учащенное дыхание).
Барорецепторы и хеморецепторы
Барорецепторы измеряют артериальное давление через специальные сенсорные окончания в сонных артериях непосредственно перед тем, как они входят в череп. Изменения активности барорецепторов через афференты в IX (языкоглоточном) и X (блуждающем) черепных нервах активируют мозговые центры, что приводит к изменению симпатического двигательного оттока к сердцу и кровеносным сосудам. Эта реакция помогает поддерживать приток крови к мозгу в самых разных обстоятельствах. Мы плохо осознаем эти действия, если только они не работают должным образом, например, когда мы чувствуем головокружение после слишком быстрого вставания.
Изменения активности барорецепторов через афференты в IX (языкоглоточном) и X (блуждающем) черепных нервах активируют мозговые центры, что приводит к изменению симпатического двигательного оттока к сердцу и кровеносным сосудам. Эта реакция помогает поддерживать приток крови к мозгу в самых разных обстоятельствах. Мы плохо осознаем эти действия, если только они не работают должным образом, например, когда мы чувствуем головокружение после слишком быстрого вставания.
Другие специализированные рецепторы (хеморецепторы) каротидного синуса сигнализируют мозгу об изменениях уровня кислорода в крови. Помимо изменений артериального давления и частоты сердечных сокращений, реакции на низкий уровень кислорода в крови включают учащение дыхания и движения головой и лицом, чтобы очистить дыхательные пути. Таким образом, у медицинского и сестринского персонала, ухаживающего за младенцами, есть правило: «беспокойный младенец находится в состоянии гипоксии, пока не доказано обратное».
Контроль аккомодации и диаметра зрачка
Под аккомодацией понимается способность глаза фокусироваться на близлежащих объектах путем изменения формы хрусталика. Это парасимпатическая двигательная функция, которая в значительной степени находится под сознательным контролем, а сенсорная информация поступает от зрительной системы. Изменения диаметра зрачка регулируют количество света, попадающего на сетчатку, и позволяют глазу адаптироваться к различным уровням окружающего света. Диаметр зрачка регулируется сочетанием парасимпатической и симпатической иннервации гладких мышц радужной оболочки в ответ на общий уровень падающего света. Общий уровень освещенности определяется специальным набором светочувствительных ганглиозных клеток сетчатки. Таким образом, «соматический» стимул вызывает «вегетативную реакцию». Если свет очень яркий, мы также можем прищурить веки (косить), и это «соматическая» реакция.
Это парасимпатическая двигательная функция, которая в значительной степени находится под сознательным контролем, а сенсорная информация поступает от зрительной системы. Изменения диаметра зрачка регулируют количество света, попадающего на сетчатку, и позволяют глазу адаптироваться к различным уровням окружающего света. Диаметр зрачка регулируется сочетанием парасимпатической и симпатической иннервации гладких мышц радужной оболочки в ответ на общий уровень падающего света. Общий уровень освещенности определяется специальным набором светочувствительных ганглиозных клеток сетчатки. Таким образом, «соматический» стимул вызывает «вегетативную реакцию». Если свет очень яркий, мы также можем прищурить веки (косить), и это «соматическая» реакция.
Слезы на глазах
Если мы грустим или расстроены, или, может быть, испытываем невероятное облегчение или безумно счастливы, мы можем плакать. Слезотечение, производство слез, опосредовано чисто парасимпатической двигательной активностью. В норме наблюдается низкий уровень выработки слезы, которая смазывает глаза, когда мы моргаем. Слезотечение также возникает в ответ на механическое раздражение глаза (например, песчинкой) или химическое раздражение (например, капля лимонного сока). Мы также можем «плакать» после болезненного механического раздражения лица (например, удара по переносице). Психологический визуальный стимул, например, грустная сцена в фильме, также может вызвать плач. В повышенном эмоциональном состоянии или после определенных ударов мы можем плакать в отсутствие какого-либо непосредственного внешнего раздражителя. Во всех этих ситуациях повышенная парасимпатическая активность может сопровождаться характерными паттернами соматической двигательной активности, такими как вокализация (например, плач) и мимика.
В норме наблюдается низкий уровень выработки слезы, которая смазывает глаза, когда мы моргаем. Слезотечение также возникает в ответ на механическое раздражение глаза (например, песчинкой) или химическое раздражение (например, капля лимонного сока). Мы также можем «плакать» после болезненного механического раздражения лица (например, удара по переносице). Психологический визуальный стимул, например, грустная сцена в фильме, также может вызвать плач. В повышенном эмоциональном состоянии или после определенных ударов мы можем плакать в отсутствие какого-либо непосредственного внешнего раздражителя. Во всех этих ситуациях повышенная парасимпатическая активность может сопровождаться характерными паттернами соматической двигательной активности, такими как вокализация (например, плач) и мимика.
Входной сигнал слуховой системы для сердечно-сосудистой системы и кожных терморегуляторов
Многие типы слухового входа могут активировать симпатический выход к сердцу и кровеносным сосудам. Внезапный неожиданный звук может вызвать учащение пульса и сужение сосудов кожи (мы бледнеем от испуга). С другой стороны, музыка с особым эмоциональным резонансом может «вызывать мурашки по коже» и «мурашки по коже». Мурашки по коже возникают в результате симпатической активации специальных гладких мышц, связанных с каждым волосяным фолликулом, что является эволюционным пережитком того времени, когда мы, по-видимому, обладали гораздо более пышной шерстью.
Внезапный неожиданный звук может вызвать учащение пульса и сужение сосудов кожи (мы бледнеем от испуга). С другой стороны, музыка с особым эмоциональным резонансом может «вызывать мурашки по коже» и «мурашки по коже». Мурашки по коже возникают в результате симпатической активации специальных гладких мышц, связанных с каждым волосяным фолликулом, что является эволюционным пережитком того времени, когда мы, по-видимому, обладали гораздо более пышной шерстью.
В самом деле, если нам действительно нужно повысить температуру тела, либо из-за того, что окружающая среда холодная (определяется кожными терморецепторами), либо из-за лихорадки, генерируемой терморегуляторными областями гипоталамуса, мы будем дрожать (соматическая двигательная реакция) и уменьшить приток крови к коже (симпатическая реакция).
Сексуальная активность
Сексуальная активность требует скоординированной двигательной активности парасимпатических, симпатических и соматических двигательных путей. У мужчин эрекция поддерживается в основном за счет парасимпатической активности, в то время как эякуляция контролируется в основном за счет симпатической активности. В обоих этих компонентах соматическая двигательная активность необходима для управления, например, мышцами тазового дна и наружными сфинктерами, а также всеми различными движениями тела, участвующими в половом акте. Как известно, эрекцию можно вызвать либо соответствующей кожной механической стимуляцией, которая активирует особый набор кожных механорецепторов в коже гениталий, либо психогенными средствами.
У мужчин эрекция поддерживается в основном за счет парасимпатической активности, в то время как эякуляция контролируется в основном за счет симпатической активности. В обоих этих компонентах соматическая двигательная активность необходима для управления, например, мышцами тазового дна и наружными сфинктерами, а также всеми различными движениями тела, участвующими в половом акте. Как известно, эрекцию можно вызвать либо соответствующей кожной механической стимуляцией, которая активирует особый набор кожных механорецепторов в коже гениталий, либо психогенными средствами.
Нервозность
Одним из наиболее известных, но наиболее неправильно истолковываемых вегетативных двигательных паттернов является реакция на стресс. Как правило, это связано с увеличением симпатической активности в отдельных проводящих путях, например, в сердечно-сосудистой системе, вызывая учащение пульса, побледнение кожи и, возможно, повышение артериального давления, а также увеличение симпатической активности в потовых железах лица, подмышек. и руки. Этот паттерн вегетативной продукции имеет психогенное (т. е. «мозгогенное») происхождение, даже если он вызывается зрительными, слуховыми или тактильными соматическими воздействиями: неужели это паук ползает по моей шее сзади?
и руки. Этот паттерн вегетативной продукции имеет психогенное (т. е. «мозгогенное») происхождение, даже если он вызывается зрительными, слуховыми или тактильными соматическими воздействиями: неужели это паук ползает по моей шее сзади?
Тошнота
Архетипические «висцеральные афференты» исходят из желудочно-кишечного тракта. Различные функциональные классы этих афферентных нервов реагируют на растяжение кишечника; или на изменения содержимого кишечника, а другие реагируют на воспаление или повреждение стенки кишечника. Двигательные выходы от мозга к кишечнику используют парасимпатические или симпатические пути. При пищевом отравлении активация кишечных афферентов вызывает вегетативную двигательную активность в дополнение к скоординированной соматической двигательной активности. Рвота включает активацию соматических двигательных путей к мышцам глотки и живота. К вегетативным путям относятся те, которые регулируют сокращение и расслабление желудка и пищевода, секрецию слюны основными слюнными железами и, возможно, сердечно-сосудистой системой. Интересно, что мы можем генерировать один и тот же скоординированный набор реакций исключительно из центральных путей, например, когда мы наблюдаем эмоционально отвратительное событие, которое буквально «делает нас больными», или если мы «больны от беспокойства».
Интересно, что мы можем генерировать один и тот же скоординированный набор реакций исключительно из центральных путей, например, когда мы наблюдаем эмоционально отвратительное событие, которое буквально «делает нас больными», или если мы «больны от беспокойства».
Ссылки
- Ackerknecht, EH (1974). История открытия вегетативной (вегетативной) нервной системы. История болезни 18: 1-8.
- Благословение, W W (1997). Нижний отдел ствола мозга и телесный гомеостаз. Нью-Йорк: Издательство Оксфордского университета.
- Фернесс, Дж. Б. (2006a). Кишечная нервная система. Оксфорд: Издательство Блэквелл.
- Фернесс, Дж. Б. (2006b). Организация вегетативной нервной системы: Периферические связи. Autonomic Neuroscience 130: 1-5.
- Гиббинс, И.Л. (2004). Периферические вегетативные пути. В: Г. Паксинос и Дж. К. Май (ред.), Нервная система человека, второе издание (стр.
 134-189). Амстердам: Elsevier Academic Press.
134-189). Амстердам: Elsevier Academic Press.
- Яниг, В.В. (2006). Интегративное действие вегетативной нервной системы: нейробиология гомеостаза. Кембридж: Издательство Кембриджского университета.
- Лэнгли, Дж. Н. (1903). Вегетативная нервная система. Мозг 26: 1-26.
- Лоуи, А.Д. и Спайер, К.М. (1990). Центральная регуляция вегетативной функции. Нью-Йорк: Издательство Оксфордского университета.
Внутренние ссылки
- Брайтенберг, В. (2007). Мозг. Scholarpedia 2(11): 2918. http://www.scholarpedia.org/article/Brain.
- Берк, RE (2008). Спинной мозг. Scholarpedia 3(4): 1925. http://www.scholarpedia.org/article/Spinal_cord.
- Corringer, PJ и Changeux, JP (2008). Никотиновые ацетилхолиновые рецепторы. Scholarpedia 3(1): 3468.
- Даулинг, Дж. (2007). Сетчатка. Scholarpedia 2(12): 3487.
 http://www.scholarpedia.org/article/Retina.
http://www.scholarpedia.org/article/Retina.
- Фернесс, Дж. Б. (2007). Энтеральная нервная система. Scholarpedia 2(10): 4064. http://www.scholarpedia.org/article/Enteric_nervous_system.
- Майерс, Д. (2007). Психология счастья. Scholarpedia 2(8): 3149. http://www.scholarpedia.org/article/Psychology_of_happiness.
- Шюц, А (2008). Нейроанатомия. Scholarpedia 3(3): 3158. http://www.scholarpedia.org/article/Neuroanatomy.
См. также
Мозг, нейроанатомия
Что это такое и как оно работает
Вегетативная нервная система представляет собой сложную сеть клеток, контролирующих внутреннее состояние организма. Он регулирует и поддерживает множество различных внутренних процессов, часто находящихся вне сознания человека.
В этой статье рассказывается об автономной нервной системе, или ВНС, о том, как она работает, и о нарушениях, которые могут повлиять на ее работу.
Нервная система представляет собой совокупность клеток, которые посылают и принимают электрические и химические сигналы по всему телу.
Нервная система состоит из двух основных частей:
- Центральная нервная система : Состоит из головного и спинного мозга.
- Периферическая нервная система : Содержит все нейроны за пределами центральной нервной системы.
ВНС является частью периферической нервной системы. Это совокупность нейронов, которые влияют на деятельность многих различных органов, включая желудок, сердце и легкие.
В ВНС есть две подсистемы, которые имеют в основном противоположные эффекты:
- Симпатическая нервная система (СНС) : Нейроны в СНС обычно подготавливают тело к реакции на что-либо в окружающей среде. Например, СНС может увеличить частоту сердечных сокращений, чтобы подготовить человека к побегу от опасности.

- Парасимпатическая нервная система (ПНС) : Парасимпатические нейроны в основном регулируют функции организма, когда человек находится в состоянии покоя.
Нервная система регулирует внутреннюю среду организма. Это необходимо для поддержания гомеостаза.
Гомеостаз относится к относительно стабильным и сбалансированным условиям внутри организма, которые необходимы для поддержания жизни. Некоторые из тех, которые регулирует гомеостаз, включают:
- температуру тела
- Гровяное давление
- Частота сердечных сокращений
- Дыхание
- Метаболизм
- Уровни глюкозы в крови
- Уровни кислотности в крови
- . деятельность органов соответственно.
ВНС также участвует в следующих функциях организма:
- производство телесных жидкостей, таких как пот
- мочеиспускание
- сексуальные реакции
Одной из важнейших функций ВНС является подготовка тела к действию посредством реакции «бей или беги».

Если организм воспринимает угрозу окружающей среде, симпатические нейроны ВНС реагируют:
- учащением пульса
- расширением дыхательных путей для облегчения дыхания
- высвобождением накопленной энергии
- увеличением силы мышц
- замедление пищеварения и других процессов в организме, которые менее важны для принятия мер
Эти изменения подготавливают организм к адекватному реагированию на угрозу в окружающей среде.
Реакция ВНС «бей или беги» развилась для защиты тела от опасностей вокруг него. Однако многие стрессовые аспекты повседневной жизни также могут вызвать эту реакцию.
Примеры включают:
- стресс, связанный с работой
- финансовые проблемы
- проблемы в отношениях
Хронический стресс может привести к тому, что вегетативная нервная система будет запускать реакцию борьбы или бегства в течение длительного времени. Это продолжение в конечном итоге нанесет вред организму.

Некоторые лекарства также могут влиять на работу ВНС. Примеры включают:
- кофеин
- фенилэфрин, который врачи используют для лечения низкого кровяного давления или гипотонии
- клонидин, который врачи используют для лечения высокого кровяного давления или гипертонии приступ астмы
- бета-адреноблокаторы эсмолол и лабеталол
Вегетативные расстройства влияют на функционирование ВНС. Иногда они могут возникать в результате следующего:
- старение
- повреждение нейронов ВНС
- повреждение определенных частей головного мозга
Некоторые медицинские состояния также могут влиять на ВНС. Некоторые распространенные причины вегетативных расстройств включают:
- диабет
- заболевание периферических нервов
- болезнь Паркинсона
Менее распространенные причины вегетативных расстройств включают:0070
- синдром Ламберта-Итона
- ботулизм
- вирусные инфекции
- поражение нервов шеи
Вегетативные расстройства могут вызывать широкий спектр симптомов, включая: значительное падение артериального давления при вставании после сидения
Вегетативные расстройства могут быть серьезными. Люди, которые испытывают симптомы вегетативного расстройства, должны обратиться к врачу для полной диагностики.
Люди, которые испытывают симптомы вегетативного расстройства, должны обратиться к врачу для полной диагностики.
Беседа с врачом особенно важна для людей с диабетом или другими состояниями, которые могут повысить вероятность вегетативных расстройств.
Чтобы диагностировать причину симптомов ВНС, врач сначала оценивает историю болезни человека на наличие факторов риска.
Врач также может запросить одно или несколько из следующих:
- Тесты для выявления ортостатической гипотензии : Врач может измерить ОГ с помощью теста с наклонным столом. В этом тесте человек лежит на кровати, которая наклоняет его тело под разными углами, в то время как машина записывает его частоту сердечных сокращений и артериальное давление.
- Электрокардиограмма : Этот тест измеряет электрическую активность в сердце.
- Тест пота : Этот тест позволяет оценить, правильно ли функционируют потовые железы. Врач использует электроды для стимуляции потовых желез и измеряет объем пота, который они выделяют в ответ на раздражитель.


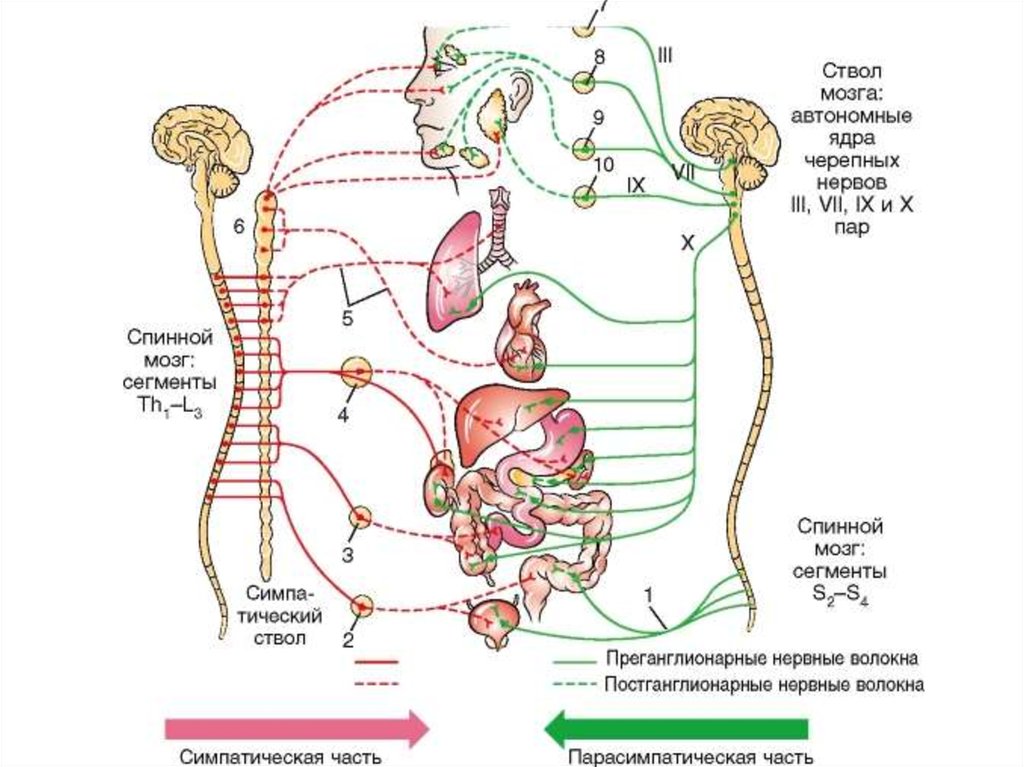
 Следовательно, эти системы являются антагонистами.
Следовательно, эти системы являются антагонистами.

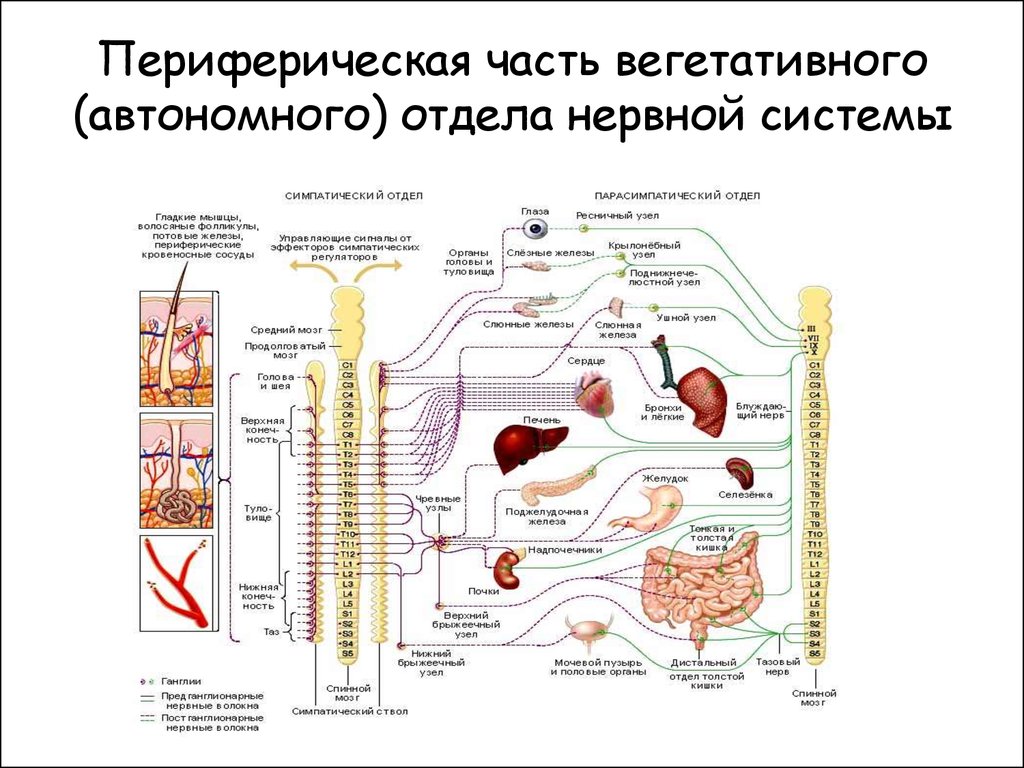 У здорового человека при этом возникает кратковременное побледнение раздражаемого участка кожи. При высокой возбудимости вегетативной нервной системы на месте раздражения появляется красная полоса, окаймленная бледными полосами суженных сосудов, а при еще более высокой чувствительности в этом месте образуется отек. Появление отёка кожи служит признаком вегетативной дисфункции. По разным данным, от 12 до 29% подростков страдают этим заболеванием. Необходимо понимать, что дисфункция может быть связана с периодом усиленного роста организма и может пройти сама собой с окончанием подросткового периода. А может стать предвестником другого более серьёзного заболевания. В любом случае консультация врача необходима.
У здорового человека при этом возникает кратковременное побледнение раздражаемого участка кожи. При высокой возбудимости вегетативной нервной системы на месте раздражения появляется красная полоса, окаймленная бледными полосами суженных сосудов, а при еще более высокой чувствительности в этом месте образуется отек. Появление отёка кожи служит признаком вегетативной дисфункции. По разным данным, от 12 до 29% подростков страдают этим заболеванием. Необходимо понимать, что дисфункция может быть связана с периодом усиленного роста организма и может пройти сама собой с окончанием подросткового периода. А может стать предвестником другого более серьёзного заболевания. В любом случае консультация врача необходима. 0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-летний 700-лепеологический аромат 900-лепеологический синдром 9003.0-йалосол. системная атрофия/синдром Шай-Дрейгера, болезнь Паркинсона, деменция с тельцами Леви
 Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]
Мол Мед. 2011 сен-октябрь;17(9-10):937-48. [Бесплатная статья PMC: PMC3188868] [PubMed: 21607292]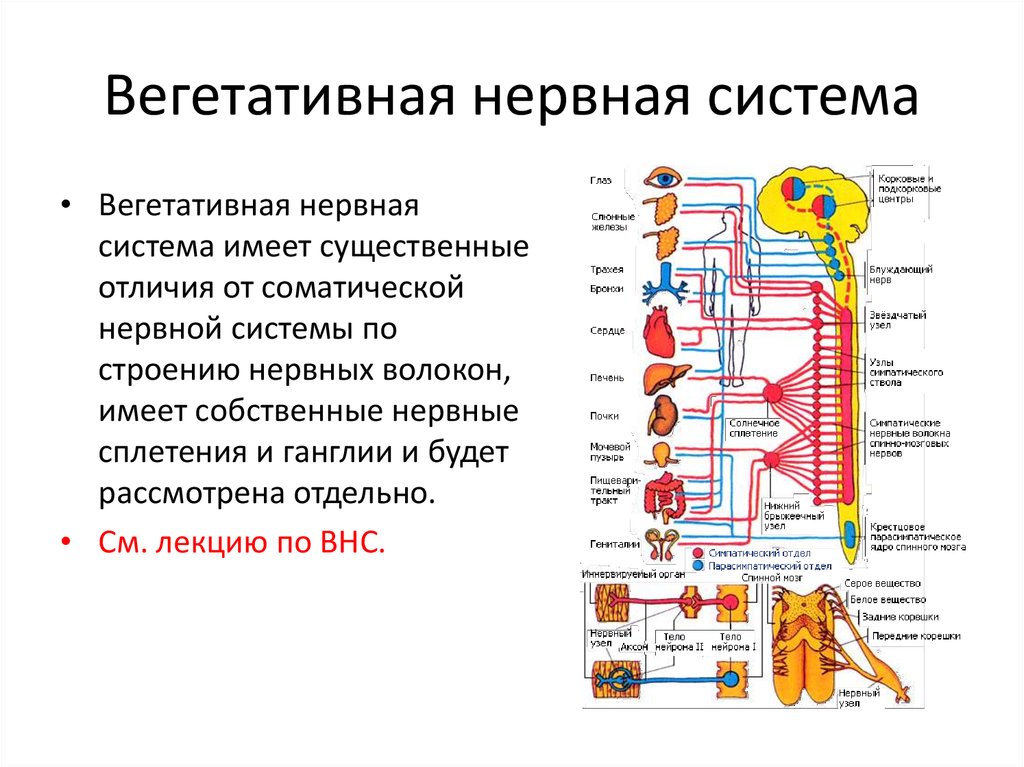 , Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]
, Зурада А. Обзор грудных чревных нервов и чревных ганглиев. Клин Анат. 2010 июль; 23 (5): 512-22. [PubMed: 20235178]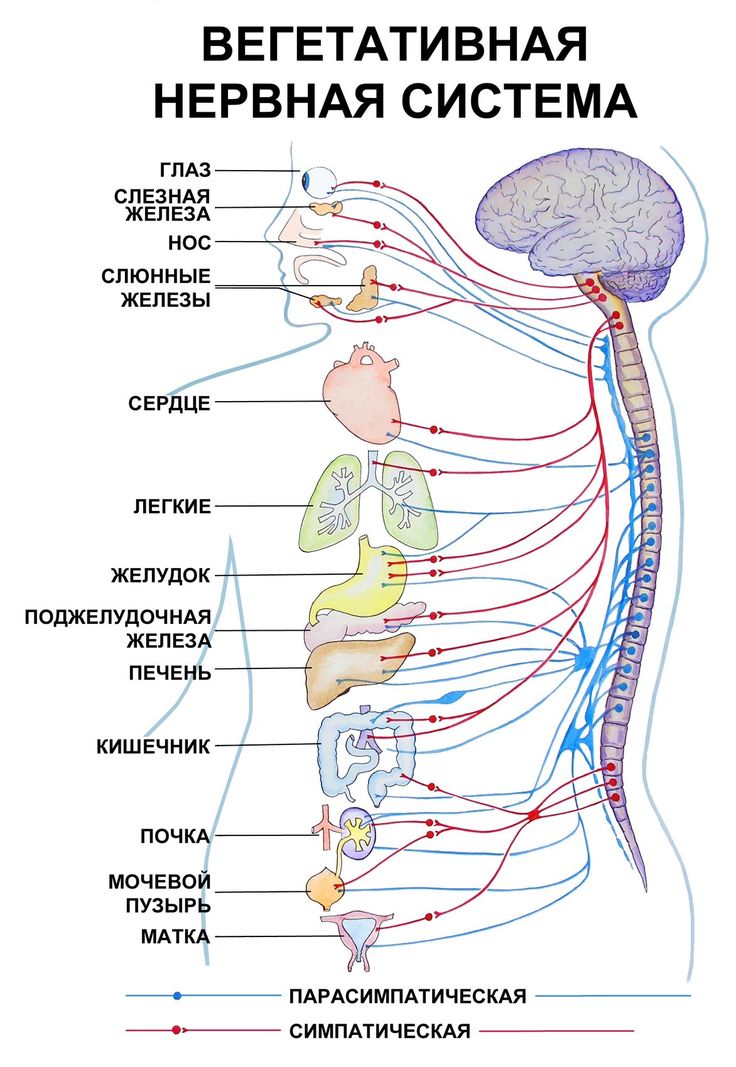 ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]
ACS Chem Neurosci. 2017 17 мая; 8 (5): 943-954. [Бесплатная статья PMC: PMC5541362] [PubMed: 28406285]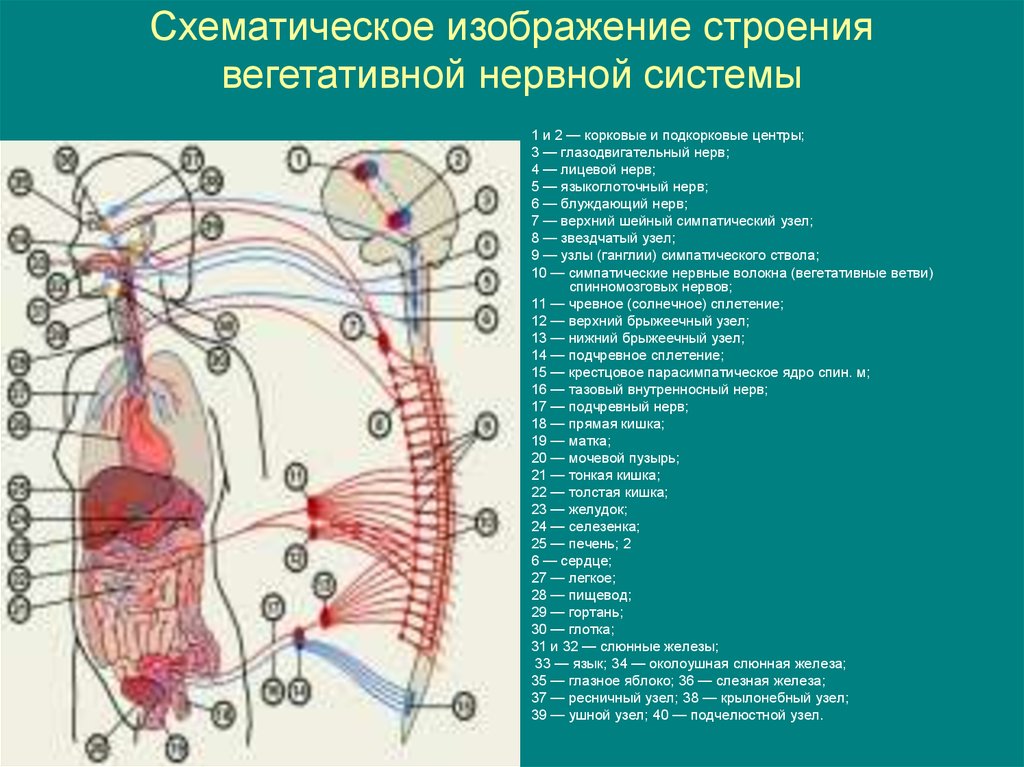 З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839]
З Кардиол. 1984 г., сен; 73 (9): 543-51. [PubMed: 6506839] Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]
Pharmacol Rev. 2000 Dec; 52(4):595-638. [PubMed: 11121511]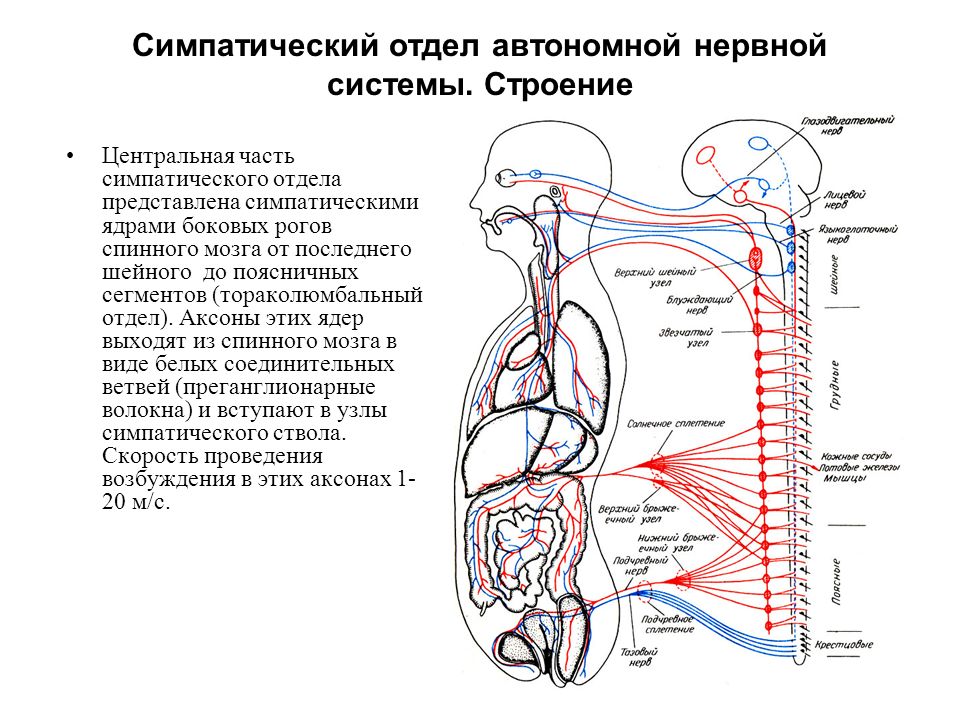

 Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737]
Мозг Behav Immun. 2010 ноябрь; 24(8):1223-8. [Бесплатная статья PMC: PMC2949498] [PubMed: 20674737] Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]
Нейрогастроэнтерол Мотил. 2016 сен; 28 (9): 1283-9. [Бесплатная статья PMC: PMC5003424] [PubMed: 27561694]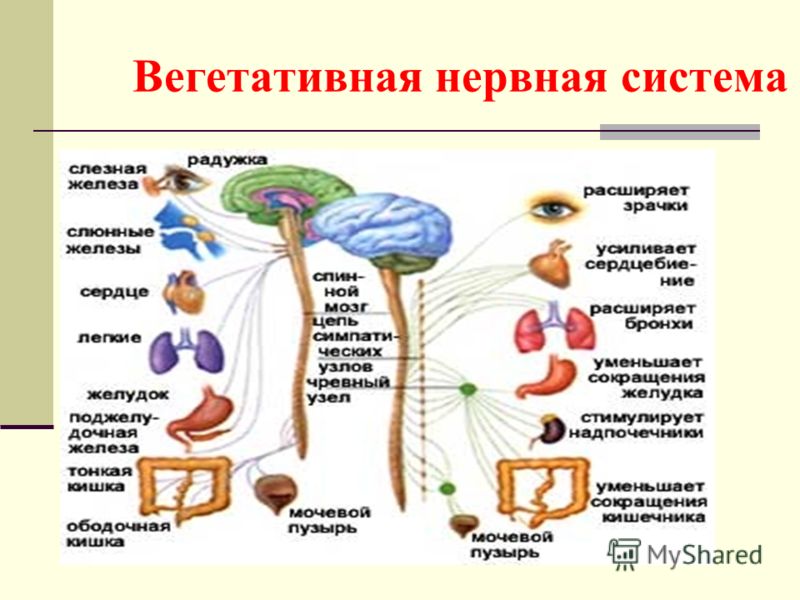 , Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]
, Константиниду С., Пахнис В., Мемик Ф., Марклунд У., Мюллер Т., Бирчмайер С., Фрид К., Эрнфорс П., Адамейко И. Нейроразвитие. Парасимпатические нейроны происходят от связанных с нервами периферических глиальных предшественников. Наука. 2014 июль 04;345(6192):82-7. [PubMed: 249]